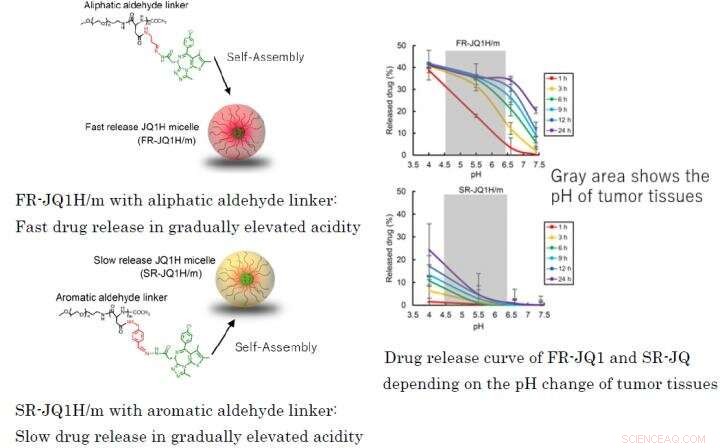
Fig. 1:Perfil de liberación de fármaco diferente según el enlazador utilizado para copolímeros de bloque de nano-micelas FR-JQ1H / m con enlazador de aldehído alifático:Liberación rápida del fármaco en acidez gradualmente elevada SR-JQ1H / m con enlazador de aldehído aromático:Liberación lenta del fármaco en acidez gradualmente elevada Curva de liberación de fármacos de FR-JQ1 y SR-JQ dependiendo del cambio de pH de los tejidos tumorales Crédito:2021 Innovación. Centro de NanoMedicina
El Centro de Innovación de NanoMedicina informó en ACS Nano junto con el grupo del Prof. Yu Matsumoto de Otorrinolaringología y Cirugía de Cabeza y Cuello y el grupo del Prof. Horacio Cabral del Departamento de Bioingeniería de la Universidad de Tokio que la eficacia de las nano-micelas poliméricas con diferente perfil de activación de fármacos depende de la nivel de expresión de c-Myc, uno de los principales protooncogenes, ha sido desarrollado.
Se sabe que c-Myc está involucrado en la proliferación de células cancerosas y la angiogénesis y cambia el ciclo celular, suprime la diferenciación celular normal, y promueve la metástasis del cáncer. Es un protooncogén típico que regula muchos genes relacionados con los factores de crecimiento y se sabe que participa en el desarrollo de muchos cánceres. como la translocación cromosómica en el linfoma de Burkitt. Por lo tanto, La investigación de descubrimiento de fármacos se está llevando a cabo en todo el mundo como un fármaco contra el cáncer dirigido a este factor de transcripción que puede atacar directamente las células madre del cáncer. Sin embargo, Dado que la letalidad embrionaria ocurre en ratones knockout para c-Myc, c-Myc se considera un gen esencial para las células vivas, y la entrega selectiva a los tejidos cancerosos es una clave importante para desarrollar sus inhibidores. Además, c-Myc también se conoce como un factor necesario para la inducción inicial de células iPS. En el futuro, se puede esperar que esta inhibición se aplique como una tecnología que también se puede utilizar para suprimir la carcinogénesis derivada de células iPS.
En este estudio, JQ1H, que es un análogo estructural de JQ1H, un inhibidor indirecto típico de c-Myc, fue encapsulado dentro de nano-micelas funcionales, y se evaluó su eficacia. JQ1 se une a una proteína de bromodominio llamada BRD4, que participa en la activación de la ARN polimerasa II que regula la expresión de c-Myc, para inhibir esta corriente fuertemente. Como resultado, la actividad de la ARN polimerasa se debilita y la expresión de c-Myc está regulada negativamente. Aunque se esperaba que JQ1 fuera un fármaco epigenómico prometedor debido a su fuerte inhibición de la expresión génica, tiene una vida media extremadamente corta in vivo debido a su rápida excreción renal y rápido aclaramiento después de la administración. Adicionalmente, JQ1 es casi insoluble en agua. Estas propiedades de JQ1 se convirtieron en un gran problema para desarrollarlo como un fármaco eficaz. Las nano-micelas poliméricas desarrolladas hasta ahora en el Centro de Innovación de NanoMedicina (iCONM), para la terapia contra el cáncer, demostró (1) estabilización de fármacos encapsulados, (2) supresión de la excreción renal, (3) EPR (administración selectiva de fármacos a tejidos cancerosos) mediada por acumulación de tumores, y (4) liberación de fármacos basada en la acidosis tumoral. Esta vez, confirmamos una buena actividad antitumoral en ratones trasplantados con cáncer de lengua, melanoma y cáncer de páncreas utilizando nano-micelas equipadas con JQ1.
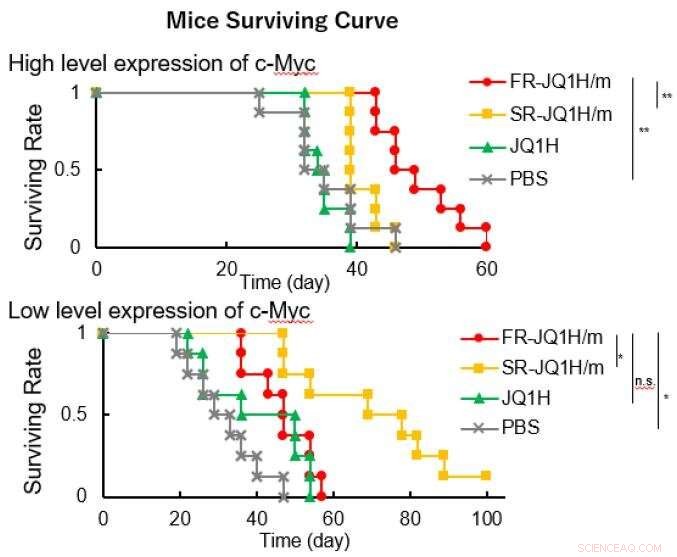
superior:cáncer de lengua, inferior:cáncer de páncreas. Crédito:Centro de Innovación 2021 de NanoMedicina
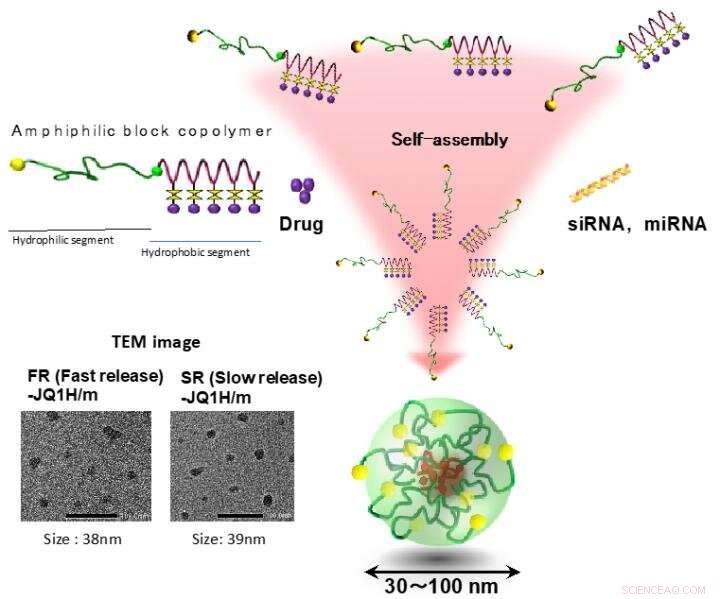
Las micelas poliméricas fueron uno de los primeros autoensamblajes de polímeros reportados como nano-DDS, y se componen de dos dominios distintos, un núcleo de carga de fármaco y una capa hidrófila. Copolímeros de bloque anfifílicos, que contiene un bloque hidrofílico y un bloque hidrofóbico, En primer lugar, se revela que construyen esos dominios distintos en una estructura de micelas a través del autoensamblaje espontáneo como resultado de interacciones hidrófobas en agua. H. Cabral, K. Miyata, K. Osada, K. Kataoka, "Micelas de copolímeros en bloque en aplicaciones de nanomedicina" Chem. Rev.2018, 118 6844-6892. (DOI:10.1021 / acs.chemrev.8b00199). Crédito:Centro de Innovación 2021 de NanoMedicina
Las nano-micelas que contienen JQ1H se filtran al tejido tumoral desde los vasos sanguíneos después de la administración sistémica debido al llamado efecto EPR. Los tejidos tumorales son ricos en ácido láctico debido a su glucólisis mejorada y son más ácidos que los tejidos normales. En este trabajo, se prepararon dos tipos de nano-micelas; uno en el que JQ1H hidrófobo se unió a un polímero de bloque anfifílico compuesto por un bloque de polietilenglicol hidrófilo y un bloque de poliaminoácido hidrófobo usando un enlazador 3-aminopropionaldehído (aldehído alifático) y la otra micela en la que JQ1H se unió con un polímero a través de p-aminometilbenzaldehído ( aldehído aromático) enlazador. Se sintetizó un polímero de bloque anfifílico y se utilizó como material base para nano-micelas. Cuando se autoensambló en agua a una estructura micelar y se administró a ratones portadores de cáncer, Se logró actividad antitumoral.
Cuando el enlazador es un aldehído alifático o cuando es un aldehído aromático, el patrón de liberación del fármaco difiere en gran medida depende de la acidez. El primero libera la droga rápidamente, y este último libera la droga lentamente. Por lo tanto, la primera nanomedicina se denominó FR-JQ1H / my la última se denominó SR-JQ1H / m. La actividad antitumoral de estas nano-micelas difiere mucho según el nivel de expresión de c-Myc. Tiempo, FR-JQ1H / m es más eficaz para tumores con alta expresión de c-Myc, SR-JQ1H / m es más eficaz para tumores con baja expresión de c-Myc.
En el futuro, Creemos que la selección de nano-micelas de acuerdo con el nivel de expresión de los biomarcadores será un paso importante hacia la realización de la medicina personalizada y los hospitales corporales.