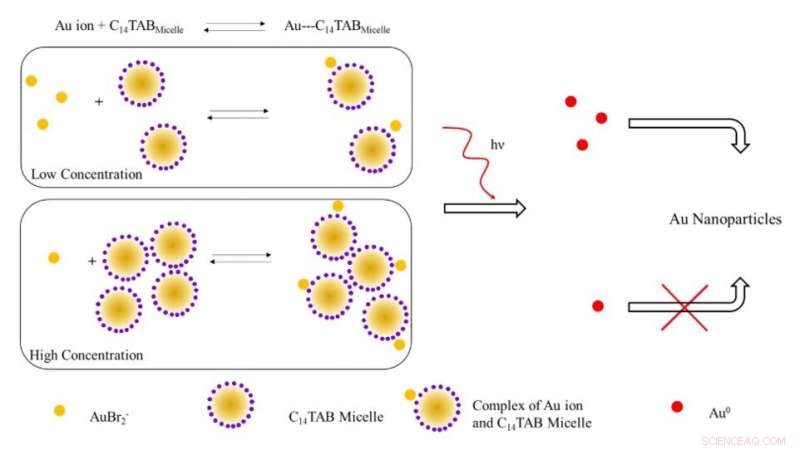
Ilustración esquemática del mecanismo propuesto para la formación de nanopartículas de oro tras la irradiación con radiación ionizante. A bajas concentraciones de tensioactivo, la mayoría de los iones de oro (AuBr2- / Au1 +) probablemente estén libres en solución (no unidos a micelas). Al aumentar la concentración de tensioactivo, el equilibrio se desplaza hacia la derecha con una disminución de los iones de oro libres. Tras la irradiación, el número de átomos de Au ^ 0 formados debido a la reducción a baja concentración de tensioactivo es mayor debido a la presencia de un mayor número de iones de oro libres en contraste con el sistema a alta concentración de tensioactivo. El mayor número de átomos de oro libres conduce a un mayor rendimiento de nanopartículas de oro debido a la reducción asistida por la superficie con iones de oro sin reaccionar. Crédito:Science Advances, doi:10.1126 / sciadv.aaw8704.
La medición de rutina de las dosis de radiación puede ser un desafío clínico debido a las limitaciones de los dosímetros convencionales que se utilizan para medir la absorción de la dosis de radiación ionizante externa. En un nuevo estudio, Karthik Pushpavanam y un equipo interdisciplinario de investigadores en los departamentos de Ingeniería Química, Ciencias Moleculares, Banner MD Anderson Cancer Center y Arizona Veterinary Oncology en los EE. UU. Han descrito un nuevo nanosensor basado en gel. La tecnología permite la detección colorimétrica y la cuantificación de los perfiles de dosis de radiación topográfica durante la radioterapia.
Tras la exposición a radiación ionizante, los científicos convirtieron los iones de oro del gel en nanopartículas de oro (AuNP) acompañadas de un cambio visual en el color del gel debido a las propiedades plasmónicas. Utilizaron la intensidad del color formado en el gel como un indicador cuantitativo de la radiación ionizante y primero utilizaron el nanosensor de gel para detectar patrones de dosis topográficos complejos después de la administración a modelos fantasmas antropomórficos, seguidos de aplicaciones con pacientes caninos vivos sometidos a radioterapia clínica. La facilidad de fabricación, operación, lectura rápida, La detección colorimétrica y el costo relativamente bajo de la tecnología implicaron un potencial traslacional para el mapeo topográfico de dosis durante las aplicaciones de radioterapia clínica. El trabajo de investigación se publica ahora en Avances de la ciencia .
Los avances en la radioterapia han dado lugar a una notable sofisticación y un software de planificación de última generación para administrar altas dosis de radiación conformada a los pacientes para mejorar la calidad de vida después del tratamiento. Durante la radioterapia, normalmente se administra una dosis alta a un tumor diana mientras se minimiza la dosis de radiación administrada al tejido circundante. Durante los cuidados paliativos, a los pacientes se les administran dosis fraccionadas más grandes para concluir el tratamiento en un período corto de tiempo. Sin embargo, Los errores de software durante dichos procedimientos pueden provocar una sobredosis y morbilidad posterior.
Para minimizar la sobreexposición accidental, Los investigadores buscan verificar de forma independiente la dosis de radiación administrada en o cerca del tejido objetivo para la seguridad avanzada del paciente. Técnicamente, tanto los nanosensores como los moleculares pueden superar los límites presentes en los sistemas convencionales para formar alternativas prácticas como sensores fáciles. Sin embargo, sus límites existentes deben abordarse y mitigarse para desarrollar sensores robustos y eficaces que determinen cuantitativa y cualitativamente los perfiles de dosis topográficos durante la radioterapia clínica.

Imágenes digitales y espectros UV-visible de diferentes formulaciones de nanosensores de gel expuestas a dosis terapéuticas de rayos X (A) Imágenes de nanosensores de gel fabricados en placas de cultivo celular de 24 pocillos y que contienen diferentes concentraciones de C14TAB (24,5 a 73,5 mM) tras la exposición a varias dosis de radiación ionizante (rayos X de 0 a 10 Gy); El tiempo de espera de Na2S fue de 5 minutos después de la irradiación, y el tiempo de incubación fue de 10 min. Las imágenes se adquirieron 1 hora después de la irradiación. Se observa un aumento visible en la intensidad del color granate con dosis crecientes de radiación ionizante para la mayoría de las concentraciones de C14TAB utilizadas durante el desarrollo del sensor de gel. (B a F) Espectros de absorbancia (300 a 990 nm) de los mismos nanosensores de gel que contienen (B) 24,5 mM, (C) 31 mM, (D) 37 mM, (E) 49 mM, y (F) 73,5 mM irradiados usando diferentes dosis de radiación. Los picos de absorbancia característicos entre longitudes de onda de 500 y 600 nm son indicativos de nanopartículas de oro formadas en los geles. Las dosis de radiación correspondientes se mencionan en la leyenda al aumentar la dosis de radiación (de arriba a abajo). A.U., unidades arbitrarias. Crédito de la foto:Sahil Inamdar, Universidad del estado de Arizona. Crédito:Science Advances, doi:10.1126 / sciadv.aaw8704
Dado que las nanopartículas de oro (AuNP) tienen características físicas y químicas únicas que brindan una excelente plataforma para desarrollar sensores. Pushpavanam y col. diseñó un sensor colorimétrico donde la radiación ionizante causaba la formación de AuNP a partir de precursores de sal incoloros. La formación de un nanosensor a base de gel puede permitir un fácil manejo y aplicaciones durante la radioterapia clínica.
En el presente trabajo, El equipo demostró la detección colorimétrica y la cuantificación de los perfiles de distribución de dosis utilizando un nanosensor de gel para mapear topográficamente las dosis de radiación a lo largo de las superficies de los tejidos. Durante las evaluaciones preclínicas, el equipo administró la tecnología de nanosensores de gel en pacientes caninos vivos sometidos a radioterapia. En total, los resultados indicaron el alcance de la tecnología para la traducción clínica en pacientes humanos y la capacidad de determinar dosis topográficas para planificar tratamientos y verificar dosis durante la radioterapia del cáncer.
Durante los experimentos, la conversión de iones de oro en nanopartículas fue acompañada por un desarrollo de color marrón en la región irradiada del nanosensor de gel. Si bien el oro existe en un estado trivalente en general (AuCl 4 - ) se puede reducir a un estado de valencia +1 metaestable (AuBr 2 - ) a temperatura ambiente utilizando ácido ascórbico (vitamina C). La irradiación de geles que contienen niveles terapéuticos de radiación estimuló la radiólisis o la división de moléculas de agua en radicales libres altamente reactivos. Los electrones hidratados generados por radiólisis a su vez redujeron el oro monovalente para formar átomos de oro en su estado zerovalente (Au 0 ) que nuclearon y maduraron en AuNP de color granate. La intensidad varió con la dosis de radiación y el equipo utilizó el rango de respuestas lineales para calibrar el nanosensor de gel. Basado en este principio, Pushpavanam y col. determinó la respuesta de los geles completamente irradiados para calibrar la absorbancia con la dosis de radiación.
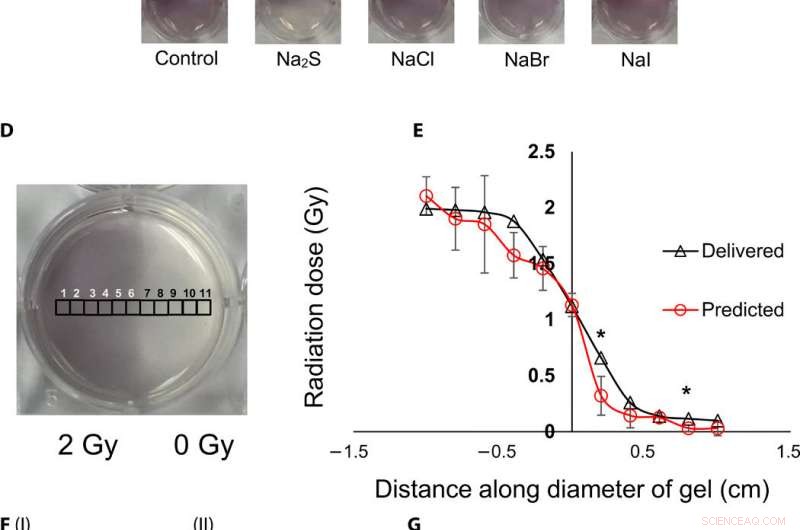
Visualización topográfica y cuantificación de dosis de radiación mediante nanosensores de gel. (A) Gel nanosensor (izquierda) antes de la irradiación, (centro) mitad superior irradiada con 4 Gy e imagen adquirida 2 min después de la irradiación, y (derecha) imagen adquirida 1 hora después de la irradiación. Un aumento visible en la intensidad del color en la mitad inferior no irradiada indica una hemorragia de color y pérdida de información topográfica. (B) I:gel de agarosa al 1,5% (p / v) (izquierda) 2 min después de la irradiación y (derecha) 1 hora después de la irradiación; II:2% (w/v) agarose gel (left) 2 min after irradiation and (right) 1 hour after irradiation indicates that the increase in agarose weight percentage does not preserve topographical dose information. (C) Gel nanosensor incubated with 5 mM sodium sulfide (Na2S) and various sodium halides with a wait time of 10 min and incubation time of 10 min; images were acquired after 1 hour. No loss of topographical information is observed upon incubation with sodium sulfide. All gels were fabricated in 24-well plates. (D) Colorimetric response of the gel nanosenor irradiated on one-half with a 2-Gy x-ray dose. A visible appearance of maroon color in the irradiated region illustrates the ability of the gel nanosensor to visualize topographical dose profiles. Each black square box (labeled 1 to 11) on the gel nanosensor corresponds to a grid of size ≈2 × 2 mm, whose absorbance at 540 nm is determined. Grids starting from 1 to 5 are regions exposed to ionizing radiation, 6 is the grid at the edge of the irradiation field, and grids from 7 to 11 are regions outside the field of irradiation. (E) Dose fall-off profile for the gel nanosensor irradiated by 2 Gy on one-half. The delivered and predicted radiation doses are comparable, which indicates the efficacy of the gel nanosensor in visualizing and retaining topographical information. In all cases, Na2S was added for 10-min incubation time after a wait time of 30 min. Radiation doses predicted by the gel nanosensor as compared with the delivered radiation dose as obtained from the treatment planning system. Asterisks indicate statistically significant differences (P <0.05) between the delivered dose and the dose predicted by the gel nanosensor (n =3 independent experiments). (F) Representative image of a petri dish containing the gel nanosensor formulation (≈3 mm thick and ≈10 cm diameter) irradiated with a 1 cm × 1 cm square field of x-ray radiation. Desde la izquierda, each square indicates increasing radiation dose from (I) 0.5 Gy (red box), 1 Gy, and 1.5 Gy; (II) 2, 2,5, 3, and 3.5 Gy; and (III) 4, 4.5, and 5 Gy; the black box in image (II) shows 0 Gy. (G) Visualization of a complex topographical dose pattern (ASU letters) generated using a 2-Gy x-ray dose. The petri dish has a diameter of ≈10 cm. In (F) and (G), the gel nanosensors contain 24.5 mM C14TAB, and Na2S was added after a wait time of 30 min and incubation time of 10 min; a representative image from three independent experiments is shown. Photo credit:Sahil Inamdar, Arizona State University. Crédito:Science Advances, doi:10.1126/sciadv.aaw8704.
To determine intensity of the color and dose delivered within gels after irradiation, the researchers used absorbance spectroscopy and observed a decrease in the spectral profile width, with increasing radiation dose for decreased polydispersity (ratio of the percentage of the standard deviation to the average value) of the nanoparticles. The peak absorbance intensity increased with increasing radiation dose to corroborate the observed increase in color intensity.
To understand the gel nanosensor's ability to detect topographical distribution of the radiation dose, the scientists irradiated half of the gel nanosensor with a 4 gray (Gy) dose. The maroon-color only appeared in the irradiated area confirming AuNP formation, but after one hour of exposure, the color bled into the irradiated region showing loss of topographic information in the gel with time. The team observed the phenomenon to arise from reaction-controlled conditions and not based on the gel composition. By incubating the gel with sodium sulfide (Na 2 S) for 10 minutes, they suppressed the color bleed-over and reasoned that to the ability to quench unreacted gold ions in the nonirradiated region and preserve dose information accurately for dose visualization and dosimetry. The scientists adopted the sensor for wide dose ranges by modulating the time of Na 2 S addition; to achieve a level of flexibility hitherto unavailable in clinical dose detection systems.
The research team then used the gel nanosensor to visualize diverse topographical radiation patterns, where the intensity of the color increased with increasing dose while preserving topographical integrity. Como prueba de concepto, they showed the gel nanosensor's ability to detect complex radiation patterns with a model dose patterned to form "ASU" (after Arizona State University). Then using transmission electron microscopy (TEM), the scientists characterized the generated gold nanoparticles as a function of dose to observe reduced average nanoparticle diameter and polydispersity at higher doses of radiation. They followed this with energy dispersive X-ray spectroscopy (EDS) to detect higher yields of AuNPs in the irradiated regions of the gel nanosensor as expected.

Gel nanosensor enabled topographical detection and quantification of clinical radiation doses in anthropomorphic head and neck phantoms. (A) Anthropomorphic head and neck phantom treated with an irregularly shaped x-ray radiation field below the left eye. (B) Image of the gel nanosensor positioned on the anthropomorphic phantom in the radiation field mimicking a conventional radiotherapy session. (C) Axial view of the treatment planning image along the central axis of the radiation beam representing an irregularly shaped radiation field used to deliver a complex radiation pattern under the eye of the phantom. The core of the crescent-shaped treatment region receives a radiation dose of 2.3 Gy (highlighted in red), and regions receiving lower doses are highlighted with different colors going outward (from green to light pink). (D) Visual image of the dose pattern on the gel nanosensor formed after delivery of 2.3 Gy. Only the irradiated region develops a maroon color, while the nonirradiated region remains colorless. (E) Expected topographical dose “heat map” profile of the radiation dose delivered to the gel placed in the phantom. The expected profile is generated from the treatment plan in the dose delivery system. In these figures, red and blue colors indicate higher and lower radiation doses, respectivamente. (F) Topographical doses predicted by the irradiated gel nanosensor. Absorbance values of ≈2 mm × 2 mm grids were quantified using a calibration curve to generate the topographical dose profile. The anticipated dose received by the core of the crescent-shaped profile (2.3 Gy) is comparable to the dose profile predicted by the gel nanosensor (2.3 Gy), which demonstrates the capability of the gel nanosensor to qualitatively and quantitatively detect complex topographical dose profiles. Photo credit:Sahil Inamdar, Arizona State University. Crédito:Science Advances, doi:10.1126/sciadv.aaw8704.
To investigate translational potential of the gel nanosensor and predict topographical profiles of radiation, Pushpavanam et al. first used a head and neck phantom model. They delivered an irregular crescent-shaped radiation dose near the eye to mimic clinically challenging administration modes of radiotherapy close to critical structures such as the eye during skin cancer treatment. The dose profile delivered using the treatment planning system was in excellent agreement with the predictions of the gel nanosensor. Indicating its capability to detect and predict complex radiation patterns similar to those used in clinical human radiotherapy.
During preclinical studies, the research team used two canine models undergoing radiotherapy to investigate the efficiency of gel nanosensors as independent, nanoscale radiation dosimeters for the first time and compared the efficiency with conventional clinical radiochromic films. On completion of the treatment, Pushpavanam et al. observed maroon color formation in one-half of the gel, whereas the non-irradiated region remained colorless. They showed predictions of the gel nanosensor in the irradiated region to agree excellently with the treatment planning system and the radiochromic film. The gel nanosensor also predicted for the region external to the irradiation to receive minimal radiation and their topographical dose profiles as well. The performance was comparable to clinical radiochromic films but with faster than conventional wait times (typically> 24 hours) to obtain the results. The scientists demonstrated the simplicity of fabrication, operación, readout time and cost effectiveness ($ 0.50 per gel material only) of the frugal invention. They maintained the response of the gel nanosensor for at least seven days to indicate long-term retrieval of dosing data unlike with fluorescence-based dosimeters with readouts that lasts mere minutes.
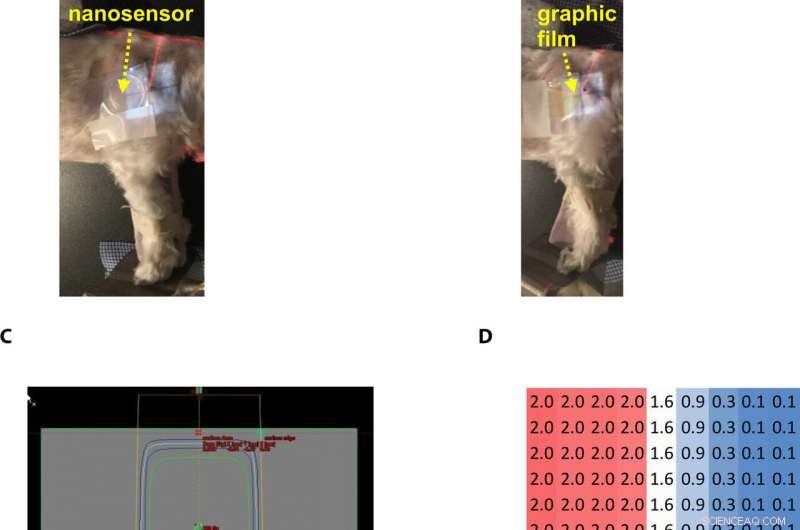
Gel nanosensor enabled topographical detection and quantification of radiation delivered to canine patient A undergoing clinical radiotherapy. Representative image of (A) half of the gel nanosensor and (B) half of the radiographic film positioned in the radiation field delivered to canine patient A. (C) Treatment planning software depicting the delivery of a 2-Gy dose delivered to the surface of patient A (neon green edge along the rectangular gray box indicates the region receiving the 2-Gy dose). (D) The irradiated region received a dose of 2 Gy (highlighted in red squares), with irradiation dose dropping to a minimal radiation 0.1 Gy (highlighted in blue squares) outside the field of irradiation. A color change is visible in both the (E) gel nanosensor whose color changes to maroon and (F) radiographic film whose color changes to dark green after irradiation. The predicted dose map in the gel nanosensor (Na2S addition wait time of 30 min and incubation time of 10 min) and radiographic film are shown below each corresponding sensor. Similarity in the dose profiles indicates the efficacy of the gel nanosensor for clinical dosimetry. The time for readout of the gel nanosensor was 1 hour after irradiation, while the radiochromic film required>24 hours of developing time before readout. All experiments were carried out three independent times. Photo credit:Sahil Inamdar, Arizona State University. Crédito:Science Advances, doi:10.1126/sciadv.aaw8704.
De este modo, Karthik Pushpavanam and colleagues developed the first colorimetric gel nanosensor as a nanoscale dosimeter to detect and distinguish regions exposed to irradiation. They optimized the platform with a chemical quenching agent (Na 2 S) to accurately reveal topographical dose distribution during clinical radiotherapy. The scientists can control the pore size distribution of the gel substrate to enhance efficacy of the nanosensor. They tested the efficiency of the gel nanosensor to predict complex topographical dose profiles in anthromorphic head and neck phantoms and in live canine patients undergoing radiotherapy. The highly disruptive and translational potential of the gel nanosensor technology will lead to improved patient safety and outcomes in clinical radiotherapy.
© 2019 Science X Network