
La investigadora de Sandia National Laboratories, Anastasia Ilgen, realiza experimentos en una caja de guantes anaeróbica. Crédito:Randy Montoya
Los investigadores de Sandia National Laboratories han descubierto el mecanismo para "encender" el hierro que reside en estructuras minerales de arcilla, conduciendo a la comprensión de cómo hacer que el hierro sea reactivo en condiciones libres de oxígeno.
Esta investigación ayudará a los científicos a comprender y predecir cómo los contaminantes, como el arsénico, selenio y cromo, moverse por el medio ambiente y entrar en las vías fluviales. Estos principios químicos se pueden aplicar para desarrollar barreras naturales en el suelo para eliminar estos contaminantes del agua y hacer membranas reactivas. que puede transformar contaminantes durante el proceso de filtración de agua.
El trabajo aparece en la portada de un número reciente de Ciencias ambientales:Nano en un papel titulado, "'Activar' hierro en minerales arcillosos, "por los investigadores de Sandia Anastasia Ilgen, Kevin Leung y Rachel Washington y Ravi Kukkadapu del Laboratorio Nacional del Noroeste del Pacífico. El trabajo fue financiado por el programa de Ciencias Energéticas Básicas del Departamento de Energía.
Comprender las reacciones del hierro
"En geociencias, Reconocimos durante décadas que comprender cómo reacciona el hierro es fundamental para comprender cómo se mueven y se transforman los contaminantes en el medio ambiente, ", dijo el autor principal Ilgen.
El hierro es un componente clave de la corteza terrestre y el cuarto elemento más común. Los minerales que contienen hierro constituyen una gran parte de los suelos y rocas sedimentarias. La adsorción y las transformaciones químicas en superficies minerales que contienen hierro definen el destino y el transporte de sustancias químicas en el medio ambiente. Adsorción, que es la fijación de contaminantes sobre superficies minerales, y las reacciones químicas en estas superficies minerales gobiernan cómo estos químicos se mueven a través del medio ambiente.
Ilgen explica que el hierro en los suelos puede existir en dos estados de oxidación:reducido y oxidado. Esto es importante, porque el hierro circula constantemente entre estas formas en respuesta a cambios leves en las condiciones del suelo.
"Los minerales arcillosos son muy comunes en los suelos y a menudo contienen hierro en sus estructuras, ", dijo." Las superficies de los minerales arcillosos, que solo contienen hierro oxidado, no son reactivos. Adsorben arsénico, pero no lo transforme químicamente. Sin embargo, estas mismas superficies se vuelven reactivas tan pronto como se introduce una pequeña cantidad de hierro reducido en la estructura del mineral de arcilla ".
Hasta ahora, se desconocía cómo y por qué los minerales arcillosos con trazas de hierro reducido reaccionan cuando no hay oxígeno presente.
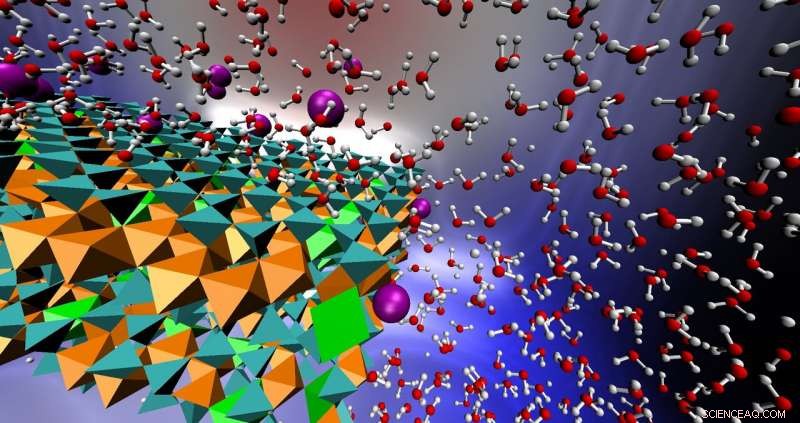
Este gráfico muestra el sistema reactivo descrito en el documento, mostrando la estructura del mineral arcilloso nontronita con hierro oxidado (naranja) y hierro reducido (verde brillante) rodeado de agua e iones de arsénico (violeta). Crédito:Tuan Ho
"Hemos descubierto el mecanismo por el cual el hierro oxidado en estructuras minerales arcillosas reacciona en condiciones libres de oxígeno, y por qué se necesitan trazas de hierro reducido para que se produzcan las reacciones, "Dijo Ilgen.
El equipo realiza el trabajo utilizando varias herramientas, métodos
Usando herramientas experimentales, el equipo identificó los sitios químicos exactos en los minerales de arcilla que reaccionaban con el arsénico. El equipo demostró que los átomos de hierro ubicados en los bordes de los minerales arcillosos eran reactivos, y para que se produzcan las reacciones, estos sitios deben contener hierro tanto reducido como oxidado.
El equipo utilizó métodos computacionales para calcular la energía necesaria para oxidar el arsénico, que se adsorbe en un sitio que contiene exclusivamente hierro oxidado frente a un sitio con hierro oxidado y reducido. Estos cálculos mostraron que la adición termodinámicamente de un hierro reducido junto a un hierro oxidado no hace que la oxidación del arsénico sea más favorable.
Luego, la pregunta es ¿por qué los sitios son reactivos en el medio ambiente? Usando análisis espectroscópico, el equipo demostró que para un contaminante, como el arsénico, oxidar en la superficie de un mineral de arcilla, debe desplazar las moléculas de agua de la superficie de ese mineral de arcilla. Separar una molécula de agua es un paso químico necesario para unir arsénico, para poder oxidarlo sobre la superficie del mineral arcilloso.
Los cálculos muestran que la remoción de agua de un sitio con hierro oxidado y reducido consume menos energía en comparación con un sitio que solo contiene hierro oxidado. Porque usa menos energía, es más fácil unir primero y luego oxidar el arsénico en este tipo de sitio químico en la superficie del mineral de arcilla y es por eso que tiene lugar la reacción.
Comprender este mecanismo ayuda a explicar el destino y el transporte de nutrientes y contaminantes sensibles a redox en el medio ambiente. y por qué algunos de estos persisten en formas oxidadas incluso en ausencia de oxígeno disuelto.
Continuar la investigación sobre el hierro en diferentes minerales naturales.
Ilgen dijo que el equipo continuará investigando los mecanismos químicos que gobiernan la reactividad del hierro en diferentes minerales naturales y explorará las condiciones requeridas para que el hierro sea reactivo en suelos y rocas sedimentarias.
El equipo utilizará este conocimiento para comprender mejor el destino ambiental y el transporte de contaminantes y nutrientes, y potencialmente diseñar barreras reactivas para evitar que los contaminantes entren en las vías fluviales.