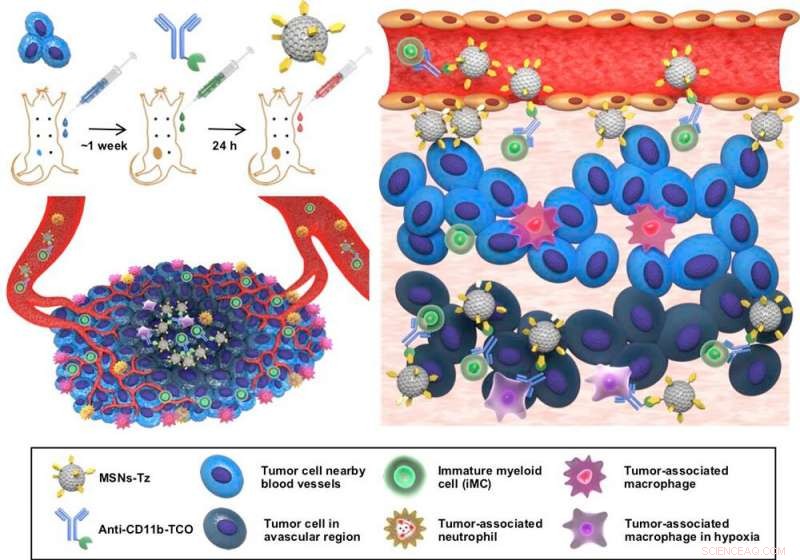
Figura 1:Una representación esquemática de la estrategia de focalización de células inmunitarias asistida por reacción de clic (CRAIT) utilizada para mejorar la penetración tumoral de NP cargadas con fármaco. (izquierda, arriba) Los anticuerpos se preinyectan para marcar las células inmunes circulantes, y las nanopartículas cargadas de fármaco se administran posteriormente para apuntar a las células inmunitarias mediante una reacción de clic. (izquierda, abajo) Ilustración esquemática del microambiente tumoral con reclutamiento de células inflamatorias y distribución de vasos sanguíneos no homogénea. (derecha) Ilustración esquemática de los principios de la estrategia CRAIT. Las células inmunes se marcan con anticuerpos y posteriormente se marcan con nanopartículas mediante una reacción de clic. Las células marcadas transportan nanopartículas desde la periferia del tumor hasta el interior del tumor. Crédito:IBS
Los científicos del IBS han informado sobre una nueva estrategia de focalización que permite la penetración tumoral profunda de nanopartículas cargadas con fármacos. Indujeron la vinculación de los anticuerpos dirigidos a las células inmunes a las nanopartículas cargadas de fármacos en las células, en lugar de absorberlos en las células o utilizar conjugados anticuerpo-nanopartícula.
Pequeños nanobots que fluyen por el cuerpo para reparar las células dañadas. Una vez que se supuso que se consideraba ciencia ficción, estos microrobots se están convirtiendo en una realidad con una gran cantidad de ensayos experimentales. En general, se piensa que las nanopartículas son tan pequeñas que pueden vagar libremente por todo el cuerpo después de su administración. Sin embargo, esto es solo parcialmente cierto. En un tumor las nanopartículas pueden penetrar en los tumores a una profundidad de hasta 100 µm de los vasos. La difusión de las nanopartículas también puede verse obstaculizada por varias barreras, como tejido tumoral denso, alta presión intersticial, y distribución vascular no homogénea. Por lo tanto, las células cancerosas ubicadas profundamente en el tejido pueden sobrevivir, resultando en recurrencia.
Curiosamente, se informa que las células inmunes tienden a acumularse en tumores profundos. A medida que los tumores superan el suministro de sangre, Las células inmunitarias se reclutan preferentemente en un microambiente tumoral para apoyar el suministro de sangre a los tumores y la remodelación de los tejidos. Ha habido varios intentos de usar células inmunes para administrar fármacos contra el cáncer a las regiones inaccesibles mediante enfoques de dirección convencionales. Dado que la mayoría de ellos requieren manipulaciones que requieren mucho tiempo para extraer, crecer, e inyectar células, este proceso ex vivo reduce la eficacia del tratamiento. Otros exploraron formas de hacer que las nanopartículas portadoras de anticuerpos se dirigieran a las células inmunitarias. De nuevo, este enfoque resulta ineficaz ya que las nanopartículas se acumulan con el fármaco de quimioterapia transportado y no pueden alcanzar las designaciones de manera eficiente.
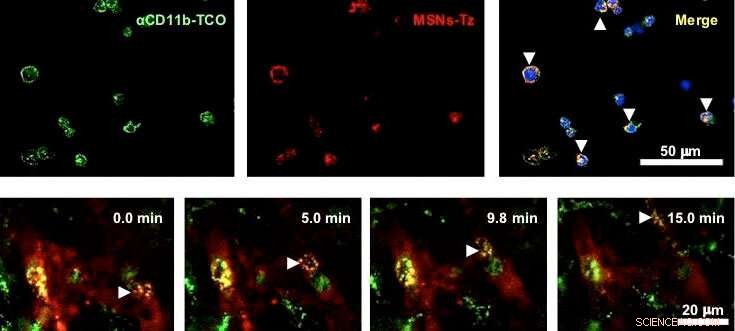
Figura 2:(arriba) Evaluación in vitro de la reacción de clic entre anticuerpos (verde) y nanopartículas (rojo) en células inmunes. (abajo) Las células inmunes que transportan nanopartículas migran en los vasos sanguíneos. Las flechas blancas indican células inmunes amarillas, ya que están etiquetadas con anticuerpos (verde) y nanopartículas (rojo). Crédito:IBS
En un artículo publicado en Revista de la Sociedad Química Estadounidense , el equipo de investigación conjunto dirigido por el Director Taeghwan Hyeon en el Centro de Nanopartículas dentro del Instituto de Ciencias Básicas (IBS) en Daejeon, Dr. Seung-Hae Kwon del Instituto de Ciencias Básicas de Corea en Seúl, y el Prof. Nohyun Lee de la Universidad Kookmin en Seúl, Corea del Sur informó sobre una nueva estrategia de focalización que permite la penetración tumoral profunda de nanopartículas cargadas con fármacos. Usaron una "reacción de clic, "una reacción química que se une fácilmente a los bloques de construcción moleculares del mismo modo que dos piezas de un cinturón de seguridad" hacen clic "para abrocharse." Nuestra idea era inducir la vinculación de los anticuerpos dirigidos a las células inmunitarias con las nanopartículas cargadas de fármacos en las células, en lugar de absorberlos en las células o utilizar conjugados anticuerpo-nanopartícula. La mayoría de los otros estudios lo hicieron y no produjeron resultados satisfactorios. "señala el profesor Nohyun Lee, el autor correspondiente del estudio.
En una reacción de clic, Los reactivos químicos permiten un enlace fácil de grupos químicos no naturales a cualquier sitio de una proteína diana con alta selectividad de sitio. En el estudio, Los investigadores utilizaron la reacción de clic entre el transcicloocteno y la tetrazina. Los anticuerpos funcionalizados con trans-cicloocteno se inyectan en ratones para marcar las células inmunes que se infiltran en el tumor. Después de cierto tiempo, Se administran nanopartículas de sílice mesoporosas funcionalizadas con tetrazina para que hagan "clic" para unirse a las células inmunes. "Esta estrategia de focalización de células inmunitarias asistida por reacción de clic (CRAIT)" invadió "con éxito las áreas previstas:las imágenes de fluorescencia en tiempo real del tejido tumoral muestran que las células inmunitarias móviles transportan las nanopartículas como se ve en la Figura 2. En comparación con la focalización pasiva, el método CRAIT trajo una doble reducción de la carga tumoral en modelos agresivos de cáncer de mama, "explica el Dr. Soo Hong Lee, el primer autor del estudio. Las nanopartículas cargadas con un medicamento contra el cáncer, doxorrubicina, no afectó la viabilidad y migración de las células.
Director Taeghwan Hyeon, el autor correspondiente del estudio dice, "La distribución intratumoral de nanopartículas administradas por el método CRAIT fue la clave para superar las limitaciones de los métodos de administración convencionales. Este estudio ampliará la aplicación de nanomedicinas".
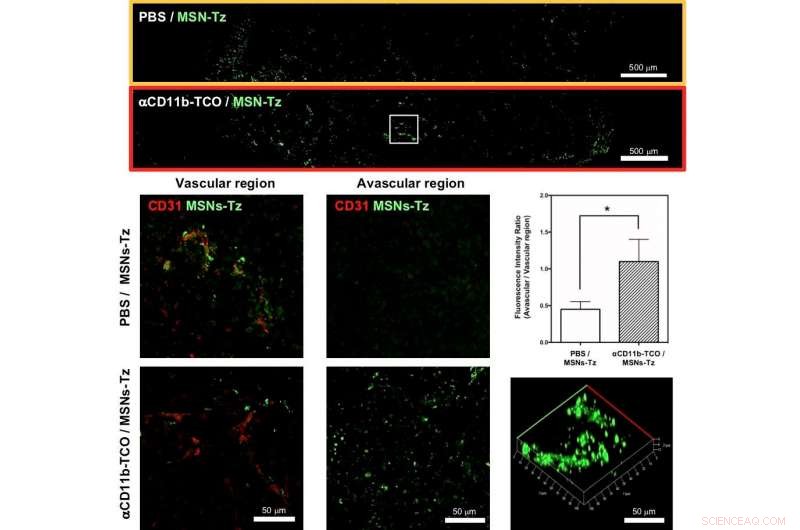
Figura 3:(arriba) Secciones de tumores representativas seleccionadas para mostrar la distribución de nanopartículas en el grupo no dirigido (recuadro naranja) y el grupo CRAIT (recuadro rojo). (medio y fondo, izquierda y centro) Distribución intratumoral del grupo no objetivo (centro) y el grupo CRAIT (abajo) en la región vascular (izquierda) y la región avascular (centro). (Derecha, medio) Relación entre vascular y la región del grupo no objetivo y el grupo CRAIT. (Derecha, abajo) Imagen de microscopía tridimensional de la sección del tumor. Crédito:IBS
Dado que el método CRAIT se basa en la reacción de clic, Se puede aplicar a varios vehículos de entrega, incluidas las micelas, liposomas, y otras nanopartículas. Adicionalmente, si se dispone de anticuerpos adecuados, se pueden usar varias celdas circulantes como vehículos de entrega. Debido a que las células circulantes están involucradas en diversas enfermedades inflamatorias, la cobertura del método CRAIT no se limita al cáncer. El método CRAIT versátil es simple, que requiere la modificación de anticuerpos y nanopartículas mediante una reacción de bioconjugación bien desarrollada.