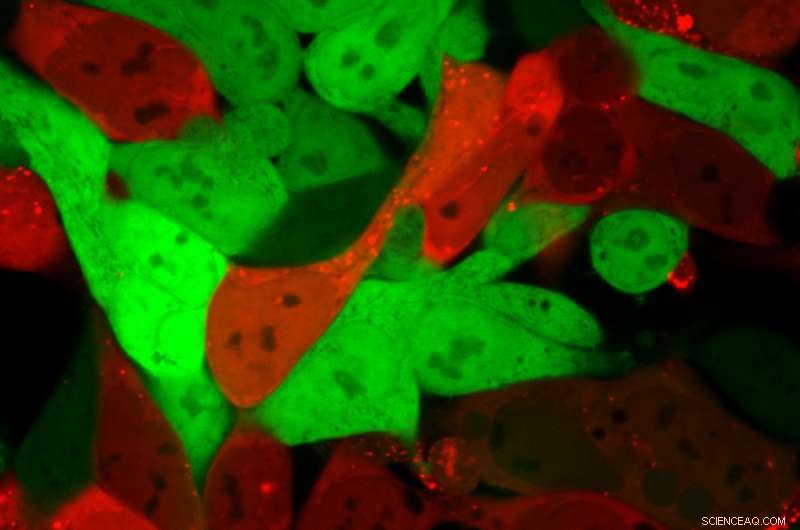
Las células que normalmente son de color verde brillante se vuelven de color rojo brillante después de que las nanopartículas de lípidos hayan entregado una carga de ARNm que codifica Cre. Las células rojas contienen el ARNm, mientras que las celdas verdes no lo hacen. Crédito:Daryll Vanover, Georgia Tech
Un nuevo proceso de detección podría acelerar drásticamente la identificación de nanopartículas adecuadas para administrar ARN terapéutico en células vivas. La técnica permitiría a los investigadores analizar cientos de nanopartículas a la vez, identificando los órganos en los que se acumulan y verificando que pueden entregar con éxito una carga de ARN a las células vivas.
Basado en un trabajo conocido como "código de barras de ADN, "la técnica inserta fragmentos únicos de ADN en hasta 150 nanopartículas diferentes para realizar pruebas simultáneas. Luego, las nanopartículas se inyectan en modelos animales y se les permite viajar a órganos como el hígado, bazo o pulmones. Luego, las técnicas de secuenciación genética identifican qué nanopartículas marcadas con ADN han llegado a órganos específicos.
En un artículo publicado el 1 de octubre en la revista procedimientos de la Academia Nacional de Ciencias , un equipo de investigación describe haber llevado el proceso un paso más allá para verificar que las nanopartículas hayan entrado en las células de órganos específicos. Además del código de barras de ADN, los investigadores insertaron en cada nanopartícula un fragmento de ARNm que se convirtió en una proteína conocida como "Cre". La proteína Cre genera un brillo rojo, Identificar las células en las que las nanopartículas ingresaron y entregaron con éxito el fármaco de ARNm, permitiendo a los investigadores identificar qué nanopartículas pueden administrar fármacos de ARN a las células de órganos específicos.
"Esta tecnica, conocido como Indicación Rápida de Descubrimiento de Nanopartículas (FIND), nos permitirá identificar el transportista correcto mucho más rápido y menos costoso de lo que pudimos hacer en el pasado, "dijo James E. Dahlman, profesor asistente en el Departamento de Ingeniería Biomédica Wallace H. Coulter en Georgia Tech y Emory University. "Como resultado, las probabilidades de que podamos encontrar portadores para tejidos específicos deberían aumentar drásticamente ".
La técnica FIND reemplazaría el cribado in vitro, que tiene un éxito limitado en la identificación de portadores de nanopartículas para las terapias genéticas. La investigación fue apoyada por fondos de los Institutos Nacionales de Salud, y de la Cystic Fibrosis Research Foundation, la Fundación para la Enfermedad de Parkinson y el Programa de Premios de Hemofilia de Bayer.

James Dahlman, profesor asistente en el Departamento de Ingeniería Biomédica Wallace H. Coulter en Georgia Tech y Emory University, contiene un chip de microfluidos que se usa para fabricar nanopartículas que podrían usarse para administrar genes terapéuticos. Crédito:Rob Felt, Georgia Tech
Las terapias basadas en ARN y ADN podrían abordar una amplia gama de enfermedades de base genética, incluyendo aterosclerosis, donde tales terapias pueden revertir la acumulación de placa en las arterias. Las nanopartículas que se utilizan para transportar el ARN y el ADN a las células están hechas de varios ingredientes cuyos niveles se pueden variar, creando el potencial para decenas de miles de nanopartículas diferentes. Encontrar la combinación correcta de estos ingredientes para apuntar a células específicas ha requerido extensos procesos de descubrimiento de prueba y error que han limitado el uso de terapias de ARN y ADN.
El uso del proceso de códigos de barras de ADN permite probar cientos de posibles combinaciones de nanopartículas simultáneamente en un solo animal, pero hasta ahora los investigadores solo pudieron decir que la combinación había llegado a órganos específicos. Al examinar qué células dentro de los órganos tienen el brillo rojo, ahora pueden verificar que las nanopartículas llevaban los códigos de barras y administraban medicamentos de ARNm funcional a las células.
En el papel, los investigadores informan haber descubierto dos nanopartículas que administraban ARNip de manera eficiente, sgRNA y mRNA a células endoteliales en el bazo. Los investigadores creen que su técnica puede administrar ARN y ADN terapéuticos a una amplia variedad de tipos de células endoteliales. y quizás también al sistema inmunológico y otros tipos de células.
"El campo ha podido administrar funcionalmente fármacos genéticos al hígado, y ahora estamos tratando de usar nuestra tecnología para administrar a diferentes órganos y tipos de células para permitir terapias para tratar todos los tipos de células que se encuentran en el hígado, "dijo Cory Sago, primer autor del artículo y un Ph.D. candidato en el laboratorio de Dahlman. "Ahora que tenemos un sistema que nos permite sondear estas preguntas a un nivel de resolución muy específico, ahora queremos ir tras otros tipos de células de una manera más eficiente ".
Dahlman espera utilizar la nueva tecnología rápidamente.

James Dahlman, profesor asistente en el Departamento de Ingeniería Biomédica Wallace H. Coulter en Georgia Tech y Emory University, se muestra en su laboratorio. Crédito:Christopher Moore, Georgia Tech
"Esperamos tomar proyectos que normalmente requerirían años y completar varios de ellos en los próximos 12 meses, ", dijo." FIND podría usarse para transportar todo tipo de fármacos de ácidos nucleicos a las células. Eso podría incluir ARN pequeños, grandes ARN, ADN pequeños y ADN grandes:muchos tipos diferentes de fármacos genéticos que ahora se están desarrollando en laboratorios de investigación ".
Los desafíos técnicos que se avecinan incluyen demostrar que identificar una afinidad por los órganos del ratón predice qué partículas funcionarán en el cuerpo humano, y que el enfoque funciona para diferentes clases de terapias genéticas.
Experimentalmente, El laboratorio de Dahlman produce las nanopartículas en tres estaciones de formulación que requieren aproximadamente 90 segundos para producir cada una de las aproximadamente 250 muestras utilizadas. Las nanopartículas resultantes luego se examinan para determinar el rango de tamaño adecuado (de 40 a 80 nanómetros de diámetro) antes de purificarlas y esterilizarlas para inyectarlas en los animales.
Después de tres días, los investigadores separan las células que brillan en rojo y secuencian los fragmentos de ADN en ellas para identificar qué composiciones químicas tuvieron más éxito en ingresar a las células de órganos específicos. Las composiciones químicas más prometedoras se utilizan para desarrollar un nuevo lote de nanopartículas candidatas para una nueva ronda de cribado. que tarda aproximadamente una semana en completarse.
"Queremos desarrollar las mejores partículas que podamos, "Dijo Sago." Cada uno de los componentes importa, y trabajamos para que cada componente sea adecuado para el tipo de celda que nos interesa. Se requiere mucha optimización ".