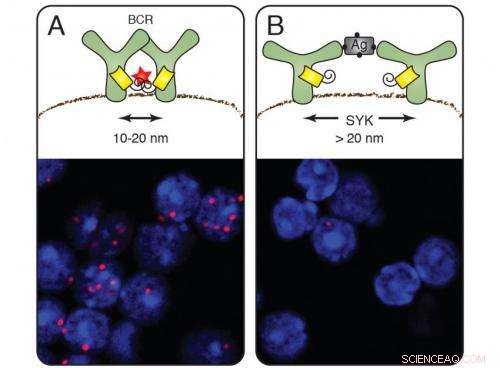
En las células en reposo (A), los receptores de antígenos de las células B forman grupos y la regla nano emite señales rojas (tinción celular debajo). Después de la activación de las células B por un antígeno, la señal roja desaparece (B). La quinasa Syk media la apertura del receptor. Crédito:Michael Reth
Después de un esfuerzo de diez años, El Prof. Dr. Michael Reth del Instituto de Biología III de la Universidad de Friburgo y el Instituto Max Planck de Inmunobiología y Epigenética ha desarrollado un método para investigar la organización de la superficie celular a escala nanométrica. Esto le permite monitorear cómo el receptor de antígeno, qué células B del sistema inmunológico utilizan para reconocer sustancias extrañas, cambios después de la activación. Este estudio muestra que los componentes del receptor se disocian entre sí, en lugar de ensamblarse, como se asumió anteriormente. La reorganización de los receptores en la membrana celular tiene lugar dentro de un rango de 10 a 40 nanómetros. Bajo un microscopio óptico, sin embargo, sólo es posible distinguir los objetos que se encuentran separados por al menos 250 nanómetros.
Mediante el uso de fragmentos de anticuerpos, los llamados Fabs, Reth, Ponente del cluster de excelencia BIOSS Center for Biological Signaling Studies de la Universidad de Friburgo, y su equipo mejoró la resolución del ensayo de ligadura de proximidad (PLA) desarrollado anteriormente unas 10 veces.
Esta tecnología permite la detección de moléculas solo cuando están ubicadas muy cerca unas de otras. Con la ayuda del método Fab-PLA más preciso, los científicos pudieron por primera vez investigar en una escala de diez nanómetros cómo se distribuyen los receptores en la membrana y cómo se reorganizan. El método Fab-PLA es un nuevo instrumento importante para el programa BIOSS Nanoscale Explorer Progamme (BiNEP), uno de los focos de investigación en el Cluster of Excellence BIOSS Center for Biological Signaling Studies de la Universidad de Friburgo.
Cuando se aplica a los receptores de antígenos, el método Fab-PLA reveló puntos rojos fluorescentes en la membrana celular de las células B inactivas:prueba de que los receptores de antígeno aparecen por primera vez en la membrana en grupos, los denominados grupos de receptores. Tan pronto como las células B detectaron un antígeno y se activaron, sin embargo, los puntos desaparecieron, los receptores se habían alejado unos de otros. Este hallazgo respalda el modelo de disociación de la activación de las células B propuesto por Michael Reth y Jianying Yang en 2010.
Los investigadores también demostraron cómo se produce la disociación:eliminaron en las células B el gen que codifica la molécula de señalización Syk, una quinasa que coopera estrechamente con el receptor de antígeno. En las células B sin Syk, los grupos de receptores todavía estaban presentes después de que se hubieran unido al antígeno. Syk es, por tanto, la llave molecular que abre el grupo de receptores e inicia la respuesta inmunitaria. Para dilucidar los detalles adicionales de la activación de las células B, los investigadores introdujeron Syk y los componentes del receptor de antígeno en las células de la mosca de la fruta. Modificaron Syk y determinaron que el grupo no se rompe hasta que la molécula se une a la parte interna del receptor de antígeno.
Los investigadores publicaron sus hallazgos en la nueva revista de acceso abierto. eLife . El estudio también incluyó una investigación de la organización a nanoescala de receptores adicionales en las células B, incluyendo la molécula CD19 o CD20. "Descubrimos que muchos receptores están organizados en la membrana en áreas específicas a nivel de nanoescala, "explica Kathrin Kläsener, Estudiante de doctorado y autor principal del estudio. La investigación fue financiada en parte por una subvención avanzada para el análisis a nanoescala de islas de proteínas en linfocitos del Consejo Europeo de Investigación (ERC), que Reth recibió en 2012.