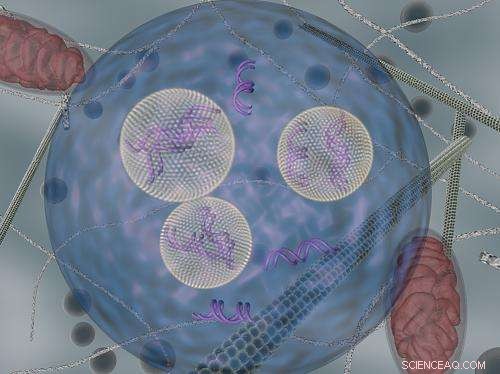
Las nanopartículas de lípidos (que llevan ARNip) se muestran a medida que se transportan dentro de las células mediante vesículas endocíticas. Crédito:DARIA ALAKHOVA Y GAURAV SAHAY
Las nanopartículas que liberan hebras cortas de ARN ofrecen una forma de tratar el cáncer y otras enfermedades al desactivar los genes que funcionan mal. Aunque este enfoque se ha mostrado prometedor, Los científicos aún no están seguros de qué sucede exactamente con las nanopartículas una vez que entran en sus células objetivo.
Un nuevo estudio del MIT arroja luz sobre el destino de las nanopartículas y sugiere nuevas formas de maximizar la entrega de las hebras de ARN que transportan. conocido como ARN de interferencia corto (ARNip).
"Hemos podido desarrollar nanopartículas que pueden enviar cargas útiles a las células, pero realmente no entendemos cómo lo hacen, "dice Daniel Anderson, el Profesor Asociado Samuel Goldblith de Ingeniería Química en el MIT. "Una vez que sepa cómo funciona, existe la posibilidad de que pueda modificar el sistema y hacerlo funcionar mejor ".
Anderson, miembro del Instituto Koch de Investigación Integrativa del Cáncer del MIT y del Instituto de Ingeniería Médica y Ciencia del MIT, es el líder de un equipo de investigación que se propuso examinar cómo se procesan las nanopartículas y la carga útil de sus fármacos a nivel celular y subcelular. Sus hallazgos aparecen en la edición del 23 de junio de Biotecnología de la naturaleza . Robert Langer, el profesor del Instituto David H. Koch del MIT, también es autor del artículo.
Un enfoque de suministro de ARN que se ha mostrado particularmente prometedor es empaquetar las hebras con un material similar a los lípidos; partículas similares se encuentran ahora en desarrollo clínico para el cáncer de hígado y otras enfermedades.
A través de un proceso llamado interferencia de ARN, ARNip se dirige al ARN mensajero (ARNm), que lleva instrucciones genéticas del ADN de una célula al resto de la célula. Cuando el ARNip se une al ARNm, el mensaje transportado por ese ARNm se destruye. La explotación de ese proceso podría permitir a los científicos desactivar genes que permiten que las células cancerosas crezcan sin control.
Los científicos ya sabían que las nanopartículas portadoras de ARNip ingresan a las células a través de un proceso, llamada endocitosis, por el cual las células engullen moléculas grandes. El equipo del MIT descubrió que una vez que las nanopartículas ingresan a las células, quedan atrapadas en burbujas conocidas como vesículas endocíticas. Esto evita que la mayor parte del ARNip alcance su ARNm objetivo, que se encuentra en el citosol de la célula (el cuerpo principal de la célula).
Esto sucede incluso con los materiales de administración de ARNip más efectivos, sugiriendo que hay mucho espacio para mejorar la tasa de publicación, Anderson dice.
"Creemos que estas partículas se pueden hacer más eficientes. Ya son muy eficientes, hasta el punto en que pueden funcionar microgramos de fármaco por kilogramo de animal, pero este tipo de estudios nos dan pistas sobre cómo mejorar el rendimiento, "Dice Anderson.
Atasco de tráfico molecular
Los investigadores encontraron que una vez que las células absorben las nanopartículas de ARN de lípidos, se descomponen en aproximadamente una hora y se excretan de las células.
También identificaron una proteína llamada Niemann Pick tipo C1 (NPC1) como uno de los principales factores en el proceso de reciclaje de nanopartículas. Sin esta proteína, las partículas no pudieron ser excretadas de las células, dando al ARNip más tiempo para alcanzar sus objetivos. "En ausencia del NPC1, hay un atasco de tráfico, y siRNA tiene más tiempo para escapar de ese atasco de tráfico porque hay un retraso, "dice Gaurav Sahay, un postdoctorado del MIT y autor principal del artículo Nature Biotechnology.
En estudios de células cultivadas en el laboratorio sin NPC1, Los investigadores encontraron que el nivel de silenciamiento de genes logrado con la interferencia de ARN era de 10 a 15 veces mayor que el de las células normales.
La falta de NPC1 también causa un trastorno de almacenamiento lisosómico poco común que suele ser fatal en la infancia. Los hallazgos sugieren que los pacientes con este trastorno podrían beneficiarse enormemente de la posible terapia de interferencia de ARN administrada por este tipo de nanopartículas. dicen los investigadores. Ahora planean estudiar los efectos de anular el gen NPC1 en la entrega de ARNip en animales. con miras a probar posibles tratamientos de ARNip para el trastorno.
Los investigadores también están buscando otros factores involucrados en el reciclaje de nanopartículas que podrían ser buenos objetivos para posiblemente ralentizar o bloquear el proceso de reciclaje. que creen que podría ayudar a que los fármacos de interferencia de ARN sean mucho más potentes. Las posibles formas de hacerlo podrían incluir administrar un medicamento que interfiera con el reciclaje de nanopartículas, o crear materiales de nanopartículas que puedan evadir con mayor eficacia el proceso de reciclaje.
"Este documento describe una forma nueva y muy importante de mejorar la potencia de los sistemas de administración de ARNip mediante la inhibición de proteínas que reciclan el material importado de la célula, "dice Pieter Cullis, profesor de bioquímica y biología molecular en la Universidad de Columbia Británica que no formaba parte del equipo de investigación. "Es posible que este enfoque dé lugar a mejoras de orden de magnitud en la potencia necesarias para que las terapias basadas en ARNip sean agentes más generalmente eficaces para tratar enfermedades".
Esta historia se vuelve a publicar por cortesía de MIT News (web.mit.edu/newsoffice/), un sitio popular que cubre noticias sobre la investigación del MIT, innovación y docencia.