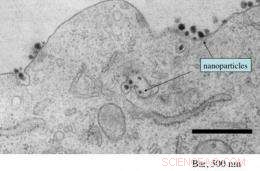
Esta micrografía electrónica muestra la presencia de numerosas nanopartículas dirigidas que contienen ARNip tanto que entran como dentro de una célula tumoral. Crédito:Caltech / Swaroop Mishra
Un equipo de investigadores y médicos dirigido por el Instituto de Tecnología de California (Caltech) ha publicado la primera prueba de que una nanopartícula dirigida, utilizada como terapéutica experimental e inyectada directamente en el torrente sanguíneo de un paciente, puede transitar hacia los tumores. entregar pequeños ARN interferentes de doble cadena (ARNip), y apagar un importante gen del cáncer mediante un mecanismo conocido como interferencia de ARN (ARNi). Es más, el equipo proporcionó la primera demostración de que este nuevo tipo de terapia, infundido en el torrente sanguíneo, puede llegar a los tumores humanos de una manera dependiente de la dosis, es decir, un mayor número de nanopartículas enviadas al cuerpo conduce a un mayor número de nanopartículas en las células tumorales.
Estos resultados, publicado en la edición en línea anticipada del 21 de marzo de la revista Naturaleza , Demostrar la viabilidad de utilizar tanto nanopartículas como terapias basadas en ARNi en pacientes. y abrir la puerta a futuras terapias que "cambien las reglas del juego" que ataquen el cáncer y otras enfermedades a nivel genético, dice Mark Davis, el Profesor Warren y Katharine Schlinger de Ingeniería Química en Caltech, y el líder del equipo de investigación.
El descubrimiento de la interferencia del ARN, el mecanismo por el cual las cadenas dobles de ARN silencian los genes, ganó a los investigadores Andrew Fire y Craig Mello el Premio Nobel de Fisiología o Medicina 2006. Los científicos informaron por primera vez sobre el hallazgo de este nuevo mecanismo en gusanos en 1998. Naturaleza papel. Desde entonces, El potencial de este tipo de inhibición genética para conducir a nuevas terapias para enfermedades como el cáncer ha sido muy promocionado.
"RNAi es una nueva forma de detener la producción de proteínas, "dice Davis. ¿Qué la convierte en una herramienta tan potencialmente poderosa, él añade, es el hecho de que su objetivo no es una proteína. Las áreas vulnerables de una proteína pueden estar ocultas dentro de sus pliegues tridimensionales, lo que dificulta que muchas terapias lleguen a ellos. A diferencia de, La interferencia de ARN se dirige al ARN mensajero (ARNm) que codifica la información necesaria para producir una proteína en primer lugar.
"En principio, "dice Davis, "Eso significa que ahora todas las proteínas se pueden drogar porque su inhibición se logra mediante la destrucción del ARNm. Y podemos ir tras los ARNm de una manera muy diseñada, dados todos los datos genómicos que están y estarán disponibles".
Todavía, Ha habido numerosos obstáculos potenciales para la aplicación de la tecnología de ARNi como terapia en humanos. Uno de los más problemáticos ha sido encontrar una forma de transportar la terapéutica, que están formados por ARNip frágiles, en las células tumorales después de la inyección directa en el torrente sanguíneo. Davis, sin embargo, tenía una solución. Incluso antes del descubrimiento de RNAi, él y su equipo habían comenzado a trabajar en formas de administrar ácidos nucleicos a las células mediante la administración sistémica. Eventualmente crearon un sistema de cuatro componentes, con un polímero único, que puede autoensamblarse en un Nanopartícula que contiene ARNip. El sistema de administración de ARNip está en desarrollo clínico por Calando Pharmaceuticals, C ª., una empresa de nanobiotecnología con sede en Pasadena.
"Estas nanopartículas pueden llevar los ARNip al sitio objetivo dentro del cuerpo, "dice Davis. Una vez que alcanzan su objetivo, en este caso, las células cancerosas dentro de los tumores:las nanopartículas ingresan a las células y liberan los ARNip.
Los resultados científicos descritos en el Naturaleza Los artículos son de un ensayo clínico de fase I de estas nanopartículas que comenzó a tratar pacientes en mayo de 2008. Los ensayos de fase I son, por definición, ensayos de seguridad; la idea es ver si y en qué nivel el fármaco u otra terapia se vuelve dañina o tóxica. Estos ensayos también pueden proporcionar una prueba de concepto científica en humanos, que es exactamente lo que se informa en el artículo de Nature.
Esta nanopartícula dirigida utilizada en el estudio y que se muestra en este esquema está hecha de un polímero único y puede llegar a las células tumorales humanas de una manera dependiente de la dosis. Crédito:Caltech / Derek Bartlett
Usando una nueva técnica desarrollada en Caltech, el equipo pudo detectar y obtener imágenes de nanopartículas dentro de las células obtenidas mediante biopsia de los tumores de varios de los participantes del ensayo. Además, Davis y sus colegas pudieron demostrar que cuanto mayor es la dosis de nanopartículas administrada al paciente, cuanto mayor sea el número de partículas que se encuentran dentro de las células tumorales, el primer ejemplo de este tipo de respuesta dependiente de la dosis utilizando nanopartículas dirigidas.
Aun mejor, Davis dice, la evidencia mostró que los ARNip habían hecho su trabajo. En las células tumorales analizadas por los investigadores, el ARNm que codifica la proteína de crecimiento celular ribonucleótido reductasa se había degradado. Esta degradación Sucesivamente, condujo a una pérdida de la proteína.
Más al punto, los fragmentos de ARNm encontrados tenían exactamente la longitud y la secuencia que deberían tener si hubieran sido escindidos en el lugar al que apunta el ARNip, señala Davis. "Es la primera vez que alguien encuentra un fragmento de ARN de las células de un paciente que muestra que el ARNm se cortó exactamente en la base correcta mediante el mecanismo de iARN, ", dice." Demuestra que el mecanismo del ARNi puede ocurrir usando ARNip en un ser humano ".
"Hay muchos objetivos del cáncer que pueden bloquearse de manera eficiente en el laboratorio utilizando ARNip, pero bloquearlos en la clínica ha sido esquivo, "dice Antoni Ribas, profesor asociado de medicina y cirugía en el Jonsson Comprehensive Cancer Center de UCLA. "Esto se debe a que muchos de estos objetivos no son susceptibles de ser bloqueados por medicamentos contra el cáncer diseñados tradicionalmente. Esta investigación proporciona la primera evidencia de que lo que funciona en el laboratorio podría ayudar a los pacientes en el futuro mediante la administración específica de ARNip utilizando nanopartículas dirigidas. Podemos empezar a pensar en apuntar a lo inalcanzable ".
"Aunque estos datos son muy tempranos y se necesita más investigación, este es un estudio prometedor de un nuevo agente contra el cáncer, y estamos orgullosos de nuestra contribución al desarrollo clínico inicial de ARNip para el tratamiento del cáncer, "dice Anthony Tolcher, director de investigación clínica en South Texas Accelerated Research Therapeutics (START).
"Los datos prometedores de los ensayos clínicos validan nuestros años de investigación en City of Hope sobre la ribonucleótido reductasa como objetivo de nuevas terapias contra el cáncer basadas en genes, "agrega el coautor Yun Yen, director asociado de investigación traslacional en City of Hope. "Estamos viendo por primera vez la utilidad del ARNip como terapia contra el cáncer y cómo la nanotecnología puede dirigirse específicamente a las células cancerosas".
El ensayo de fase I, patrocinado por Calando Pharmaceuticals, se está llevando a cabo en START y el Jonsson Comprehensive Cancer Center de UCLA. y los resultados clínicos del ensayo se presentarán más adelante. "Por lo menos, Hemos demostrado que el mecanismo de ARNi se puede utilizar en humanos para terapia y que la entrega dirigida de ARNip permite la administración sistémica. "Es un momento muy emocionante", dice Davis.