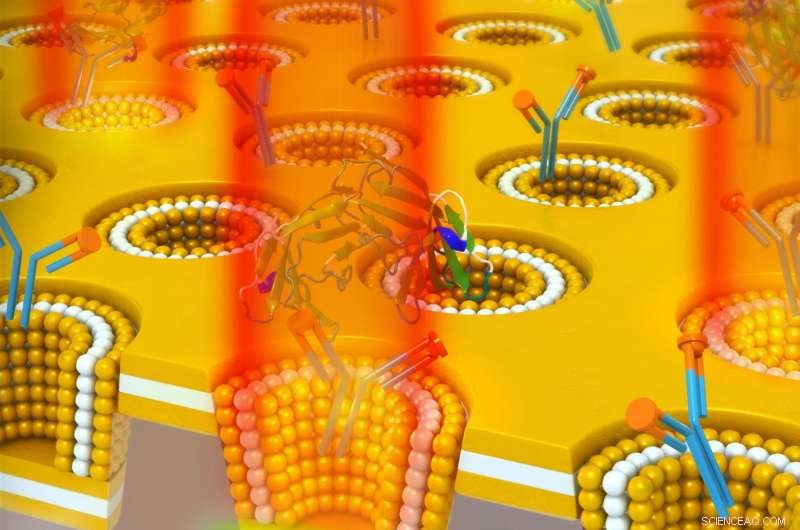
Un diseño de cavidad de metal-aislante-metal de nanocopa plasmónica utilizado para detectar el biomarcador de cáncer CEA. La nanocavidad conduce al almacenamiento de energía óptica que se acopla al campo lejano por un aumento del índice de refracción. Por lo tanto, La unión de CEA a su anticuerpo inmovilizado conduce a un aumento sensible en la intensidad de transmisión en la longitud de onda de resonancia sin cambio espectral. Crédito:Universidad de Illinois
Un nuevo sensor plasmónico desarrollado por investigadores de la Universidad de Illinois en Urbana-Champaign servirá como una detección temprana confiable de biomarcadores para muchas formas de cáncer y eventualmente otras enfermedades.
Se ha demostrado que el sensor es confiable para detectar la presencia del antígeno carcinoembrionario (CEA) del biomarcador del cáncer en una magnitud de 1 nanogramo por mililitro. La mayoría de los seres humanos portan al menos algunas cantidades de CEA con un rango promedio de 3-5 nanogramos por mililitro. Los investigadores optaron por centrarse en CEA porque su presencia en concentraciones más altas es un indicador temprano de muchas formas de cáncer. incluidos los cánceres de pulmón y próstata.
"El cáncer es una de las principales causas de muerte en los Estados Unidos, ya que más de la mitad de los nuevos pacientes son diagnosticados después de que ya se ha diseminado. Ameen explicó:"Esto muestra la gravedad con la que se debe abordar este problema y este nuevo diseño de un sensor plasmónico ayuda a detectar la menor concentración de CEA en un estado anterior".
El sensor plasmónico es una mejora del método actual de última generación por algunas razones. Primero, fue capaz de mejorar el límite de detección en al menos dos órdenes de magnitud. De hecho, la mayoría de los métodos no pueden detectar con precisión la presencia de CEA hasta que alcanza una concentración más alta.
En segundo lugar, porque funciona con mucha menos instrumentación, es menos costoso y más portátil y no requiere la experiencia necesaria para realizar una lectura. También significa que en lugar de necesitar un frasco de sangre para una prueba, Un simple pinchazo en el dedo servirá. Este aspecto será especialmente importante para aquellos que no viven cerca de una instalación médica avanzada, incluidos los de países en desarrollo.
El equipo de investigación fue dirigido por Logan Liu, y Lynford Goddard, profesores asociados de ingeniería eléctrica e informática con los alumnos Abid Ameen y Lisa Hackett que llevan a cabo el proyecto. El equipo publicó sus resultados en Materiales ópticos avanzados como artículo de portada.
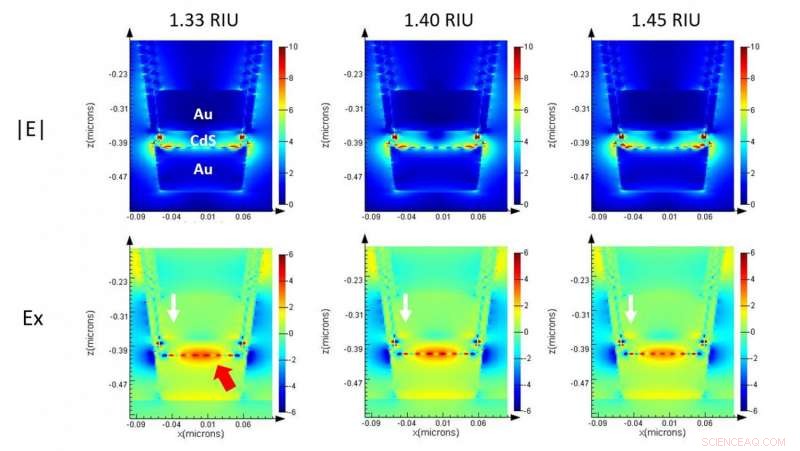
Simulación electromagnética de un solo nanocup en ML-nanoLCA que muestra la intensidad del campo en la sección transversal. Crédito:Universidad de Illinois
El dispositivo combina dos métodos de detección, que hasta ese momento no habían podido usarse juntos. Primero, utiliza una nanocavidad multicapa 3D en una matriz de nanocup, lo que permite que la luz se almacene en la cavidad compuesta por dos capas metálicas (en este caso oro) que rodean una capa aislante.
En segundo lugar, utiliza detección plasmónica, que detecta interacciones sensibles a nanoescala de luz y materia con biomoléculas en la superficie del dispositivo. Produce un confinamiento de campo mejorado y un campo localizado mejorado. Debido a la estructura plasmónica, la luz se desacopla de manera más eficiente a medida que cambia el índice de refracción circundante.
"Al combinar las propiedades plasmónicas y las propiedades de la cavidad óptica en un solo dispositivo, podemos detectar concentraciones más bajas de biomarcador por confinamiento y transmisión de luz en la capa de la cavidad y desde la parte superior del dispositivo, respectivamente, basado en el grosor de las multicapas y el índice de refracción de la capa de la cavidad, "Ameen explicó.
"La matriz nanocup proporciona una transmisión óptica extraordinaria, "Hackett agregó." Si tomas una película delgada de metal y tratas de hacer brillar la luz a través de ella, casi no se transmitirá luz. Sin embargo, si coloca una matriz periódica de nanoagujeros, o en nuestro caso una estructura nanocup, entonces lo que ves es una condición de resonancia donde a una cierta longitud de onda, tendrás un pico en la transmisión a través de este dispositivo ".
Debido a que la resonancia está cambiando en una sola longitud de onda y debido a que las características espectrales tienen ubicaciones de referencia, la excitación y la detección se pueden realizar de forma fiable sin ningún equipo especializado. Con este dispositivo, se puede usar una fuente de luz LED en lugar de un láser y se puede usar una fotocélula o una imagen de cámara en lugar de un espectrómetro de alta gama.
"Debido a nuestra estructura plasmónica multicapa de alto rendimiento, pudimos dispersar la luz de manera muy eficiente al campo lejano, "Hackett dijo." Cuando aumenta el índice de refracción de la región de detección, hace que la energía almacenada se acople. Por lo general, cuando tiene este tipo de sensores plasmónicos refractométricos, tiene un cambio en el ángulo o un cambio en su longitud de onda cuando se cumple la condición de resonancia. En nuestro caso, porque hemos incorporado una nanocavidad, tenemos una longitud de onda de resonancia fija ".
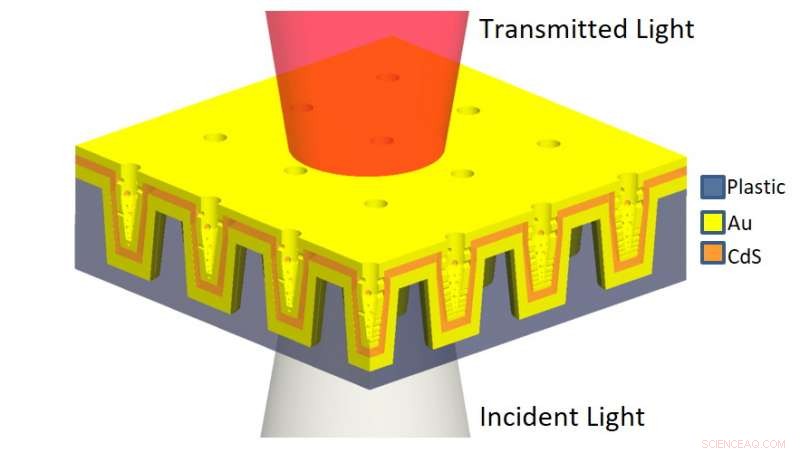
La ilustración esquemática del nanoLCA multicapa (ML-nanoLCA) muestra la estructura multicapa y la dirección de iluminación. Crédito:Universidad de Illinois en Urbana-Champaign
A medida que aumenta la concentración de biomoléculas (en este caso CEA), también lo hace el índice de refracción, lo que produce un aumento de la intensidad de transmisión a una longitud de onda fija que se puede detectar fácilmente.
"Lo que eso significa en el futuro es que podemos utilizar este sensor, que hemos optimizado e incorporado con un LED y tienen la instrumentación más compacta, de hecho, no hay instrumentación sofisticada en absoluto, ", Dijo Ameen." Esto permite la detección plasmónica de alto rendimiento la capacidad de ir hacia sistemas de detección portátiles y sensores portátiles a gran escala ".
Por ahora, se están implementando métodos de detección de biomarcadores de cáncer en pacientes de alto riesgo, especialmente pacientes con cáncer en remisión. Toman tiempo equipo especializado, y requieren mucha mano de obra.
En el futuro, sin embargo, debido a la portabilidad y la naturaleza económica de este método, se puede administrar más fácilmente a cualquier paciente en los controles de rutina. Esto permitiría tratar a las personas con una concentración elevada de CEA incluso antes de que las células cancerosas se diseminen por el cuerpo.
"En este momento, el cáncer se detecta más cerca de la etapa final, "Ameen anotó." Queremos detectarlo lo antes posible. Nuestro dispositivo nos brinda esa oportunidad ".
Si bien este estudio demostró la detección en una pequeña muestra de suero humano, el método podría utilizarse para la detección de otras enfermedades en el futuro.
"En el futuro, si son muy rentables y portátiles, "Hackett dijo, "Sería genial ver que las personas pudieran tener más control sobre su salud y monitorear algo como esto por su cuenta".