Si caminas por las montañas Apalaches, verás rodales de árboles muertos y debilitados. Si vives en una ciudad puede que notes edificios de piedra gastados, rayas en el techo de su automóvil o barandillas y estatuas de metal corroídas. Puedes ver los efectos de lluvia ácida casi donde quiera que vayas, pero con la atención de los medios y del público dirigida a la perspectiva más ominosa del calentamiento global, la lluvia ácida ha caído al borde del camino. El flagelo del cielo casi parece un problema del siglo XX, un tema tratado en las décadas de 1980 y 1990 por la legislación.
La lluvia ácida se produce principalmente en el hemisferio norte, los más industrializados, la mitad más sucia del mundo. Los vientos pueden barrer las emisiones de las chimeneas altas y llevar los contaminantes lejos de sus fuentes originales. cruzando las fronteras estatales y las fronteras nacionales en el proceso. La lluvia ácida puede no tener la gama global completa de gases de efecto invernadero, pero es un transfronterizo , y por tanto internacional, asunto.
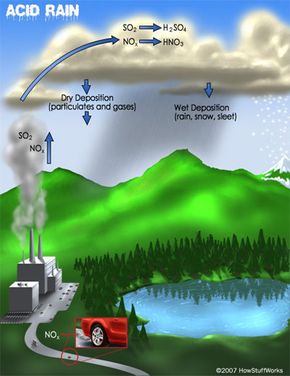
Lluvia ácida, también conocido como deposición ácida, es causada por emisiones de dióxido de azufre (SO2) y oxido de nitrógeno (NOx) de centrales eléctricas, automóviles y fábricas. Fuentes naturales como volcanes, Los incendios forestales y los rayos también se suman a la contaminación provocada por el hombre. El SO2 y el NOx se vuelven ácidos cuando entran a la atmósfera y reaccionan con el vapor de agua. Los ácidos sulfúrico y nítrico resultantes pueden caer como deposiciones húmedas o secas. La deposición húmeda es precipitación:lluvia ácida, nieve, aguanieve o niebla. La deposición seca cae como partículas ácidas o gases.
ContenidoLos científicos expresan la acidez de la lluvia ácida utilizando el escala PH . La escala define la acidez de una solución, neutralidad o alcalinidad basada en su concentración de iones de hidrógeno. Los ácidos tienen una alta concentración de iones de hidrógeno y un pH bajo. La escala va de cero a 14, con agua pura en un punto neutro 7.0. La mayor parte del agua sin embargo, no es exactamente puro. Incluso limpio la lluvia normal tiene un pH de aproximadamente 5,6. Esto se debe a que reacciona con el dióxido de carbono en la atmósfera y forma ácido carbónico ligeramente ácido antes de que se convierta en lluvia.
La lluvia ácida tiene un pH de 5.0 o menos. La mayor parte de la deposición ácida oscila entre un pH de 4,3 a 5,0, en algún lugar entre la acidez del jugo de naranja y el café negro. Pero comparando la lluvia ácida con la segura, Los ácidos naturales pueden inducir a error. Incluso en su punto más débil, La lluvia ácida destruye los ecosistemas al atrofiar las plantas sensibles y matar los delicados huevos acuáticos.
Los programas que monitorean la lluvia ácida analizan el contenido de hidrógeno para determinar el pH. También miden las concentraciones atmosféricas de ácido nítrico, nitrato, dióxido de azufre, sulfato y amonio. En los Estados Unidos, el Programa Nacional de Deposición Atmosférica (NADP) supervisa la deposición húmeda mientras que la Red de Tendencias y Estado del Aire Limpio (CASTNET) observa la deposición seca. El monitoreo de la deposición ácida ayuda a determinar cargas críticas , o la cantidad de contaminantes que un ecosistema puede soportar antes de sufrir daños. Las cargas críticas precisas ayudan a establecer objetivos efectivos para las reducciones de SO2 y NOx.
Ahora aprenderemos sobre los efectos nocivos de la lluvia ácida en los ambientes acuáticos, bosques acabados, materiales de construcción y salud humana.
Las aguas superficiales y sus frágiles ecosistemas son quizás las víctimas más famosas de la lluvia ácida. La mayor parte de la precipitación que entra en un lago, río, El arroyo o la marisma primero deben pasar y filtrarse a través del suelo. Todo suelo tiene un capacidad de almacenamiento , o capacidad para resistir cambios de acidez y alcalinidad. La capacidad amortiguadora del suelo determina la acidez de un cuerpo de agua. Si la capacidad es baja, o ha llegado a su límite, la lluvia ácida puede pasar sin neutralizar.
La mayor parte de la vida es cómoda a un pH casi neutro:aléjese demasiado del pH 7,0, y los organismos delicados comienzan a morir. El plancton y los invertebrados son sensibles a los cambios de acidez y mueren primero. A pH 5.0, Los huevos de los peces se degradan y las crías no pueden desarrollarse. Los peces y las ranas adultos a veces pueden tolerar acidez tan baja como pH 4.0, pero mueren de hambre a medida que se extinguen sus fuentes de alimentos más débiles. Cuando la lluvia ácida interrumpe la cadena alimentaria, la biodiversidad disminuye.
La deposición de nitrógeno de la lluvia ácida también daña las aguas costeras y los estuarios. El agua rica en nitrógeno favorece el crecimiento masivo de algas y la proliferación de algas. Las bacterias descomponen las algas muertas, florecer y absorber el oxígeno disponible en el agua. Pez, mariscos, los lechos de pastos marinos y los arrecifes de coral mueren en las algas, aguas empobrecidas en oxígeno. Los científicos estiman que entre el 10 y el 45 por ciento del nitrógeno producido por el hombre que termina en las aguas costeras proviene de la deposición atmosférica [Fuente:Agencia de Protección Ambiental].
La mayoría de las masas de agua ácidas no parecen estar contaminadas. A medida que la materia orgánica en descomposición se asienta, el agua acidificada puede aparecer clara y azul. Algunas especies como juncos y musgo, incluso prosperar en condiciones ácidas. Pero la vegetación y las aguas cristalinas desmienten un ambiente malsano. Gotas de diversidad y las especies que se quedan sin depredadores a menudo crecen inquietantemente.
La lluvia ácida también daña los bosques, como veremos en la siguiente sección.
Los bosques dependen de la capacidad amortiguadora de su suelo para protegerlos de la lluvia ácida. Las aguas ácidas extraen las toxinas del suelo como el aluminio. Los árboles absorben las sustancias venenosas, y la escorrentía lo arroja a los lagos, Rios y corrientes. La lluvia ácida también disuelve minerales y nutrientes útiles como el calcio, magnesio y potasio antes de que los árboles puedan absorberlos. La lluvia ácida rara vez mata un bosque por completo, sino que detiene su crecimiento a través de años de degradación del suelo. La privación de nutrientes y la exposición a toxinas hacen que los árboles sean más propensos a caer en tormentas o morir en clima frío.
Incluso los árboles en suelos bien tamponados pueden debilitarse en una fuerte niebla ácida. Los bosques de gran altitud se empapan en nubes ácidas, que despojan a las hojas de nutrientes y destruyen la capacidad de los árboles para resistir el frío. Los picos calvos de los Apalaches hablan del efecto venenoso de la lluvia ácida en los bosques de gran altitud.
La lluvia ácida tiene la inquietante capacidad de borrar y destruir la piedra y el metal, el más duradero de los materiales. Edificios viejos, los monumentos y las lápidas tienen los suaves signos de corrosión ácida y deterioro. La deposición ácida acelera la erosión natural causada por la lluvia, sol, nieve y viento.
La lluvia ácida también estropea la pintura de los automóviles. La industria automotriz considera que la deposición ácida es un tipo de corrosivo. consecuencias ambientales , junto con la savia de los árboles, polen y excrementos de aves. Las marcas de ácido dejan irregularidades, formas grabadas en superficies horizontales. Repintar es la única forma de reparar el acabado de un automóvil desfigurado por la lluvia ácida.
Dado que la lluvia ácida puede matar a los animales acuáticos, debilita los árboles y disuelve la piedra, parece que también podría escaldar o quemar a los humanos. Pero no afecta a las personas de la misma manera que a los peces o las plantas. La lluvia ácida se siente igual que la lluvia normal; incluso es seguro nadar en un lago ácido. Pero las partículas de sulfato y nitrato de deposición seca pueden causar asma, bronquitis y problemas cardíacos. El NOx en la deposición ácida también reacciona con compuestos orgánicos volátiles (COV) para formar ozono a nivel del suelo. Ozono, o niebla tóxica , agrava y debilita el sistema respiratorio.
La lluvia ácida ha existido desde que las primeras fábricas de la Revolución Industrial comenzaron a escupir emisiones tóxicas. Un científico inglés, Robert Angus Smith, acuñó el término "lluvia ácida" en 1872 cuando escribió sobre su toque corrosivo en los edificios y el efecto letal en las plantas. Pero la lluvia ácida no se convirtió en un problema ambiental controlado por el gobierno hasta más de un siglo después. Para entonces, los científicos habían determinado que la lluvia ácida era una preocupación transfronteriza más que local. En 1980, la Acid Deposition Act lanzó un estudio de 10 años sobre la lluvia ácida bajo la dirección de la Programa Nacional de Evaluación de Precipitaciones Ácidas (NAPAP) para monitorear sitios en todo el país.
En 1990, armado con el estudio de la NAPAP, El Congreso cambió la Ley de Aire Limpio existente para incluir la lluvia ácida. La nueva enmienda del Título IV de la Ley de Aire Limpio pedía reducciones de SO2 y NOx. los Programa de lluvia ácida (ARP) se formó en 1995 para poner en vigor el Título IV.
La ARP impone límites a la industria energética para reducir las emisiones anuales de SO2 y NOx. El ARP utiliza un programa de tope y comercio para reducir las emisiones de SO2. Establece un límite a la cantidad total de SO2 que pueden producir las centrales eléctricas de los Estados Unidos contiguos. Después de poner un límite, la ARP distribuye derechos de emisión a las unidades de centrales eléctricas. Las unidades solo pueden producir la cantidad de SO2 para la que tienen crédito. Si reducen las emisiones más rápido de lo que requiere el ARP, pueden depositar asignaciones para uso futuro o venderlas a otras plantas. El límite final de 2010 será de 8,95 millones de toneladas permitidas por año, un notable 50 por ciento menos que las emisiones de las centrales eléctricas de 1980 [Fuente:EPA].
El ARP regula las reducciones de NOx con un método más convencional. sistema regulatorio basado en tarifas . El programa establece un límite de libras permitidas de NOx por millón de unidades térmicas británicas (lb / mmBtu) para cada caldera de la planta de energía. Los propietarios cumplen con las reducciones objetivo para las calderas individuales o promedian las emisiones de todas las unidades que poseen y cumplen con un objetivo combinado. El ARP tiene como objetivo reducir los NOx a 2 millones de toneladas por debajo del nivel proyectado para 2000 si no hubiera existido el Título IV [Fuente:EPA].
Las centrales eléctricas cumplen sus objetivos de ARP mediante el uso de carbón con bajo contenido de azufre, "depuradores húmedos" o sistemas de desulfuración de gases de combustión, quemadores bajos en NOx y otras tecnologías limpias de carbón. También pueden intercambiar créditos de SO2 entre ellos.
Incluso con una mayor demanda de energía, el ARP ha logrado reducir las emisiones de SO2 y NOx. Pero NAPAP sugiere que para que los ecosistemas se recuperen por completo, las reducciones tendrán que caer entre un 40 y un 80 por ciento adicional por debajo de los límites de fuerza total de 2010 [Fuente:EPA].
Los coches también emiten NOx. Los diseños más nuevos de convertidores catalíticos ayudan a tratar los gases de escape y eliminar los NOx y otros contaminantes como el monóxido de carbono y los COV que contribuyen al smog.
Incluso con notables tecnologías de carbón limpio, convertidores catalíticos y tapas y regulaciones fuertes, Los combustibles fósiles siguen siendo una fuente de energía sucia. Formas alternativas de energía como la nuclear, la energía solar y la hidroeléctrica no emiten los millones de toneladas de SO2 y NOx que trastornan los ecosistemas, arruinan edificios y monumentos y debilitan la salud de las personas.
Para obtener más información sobre la lluvia ácida, formas alternativas de energía y otros temas relacionados, consulte los enlaces en la página siguiente.