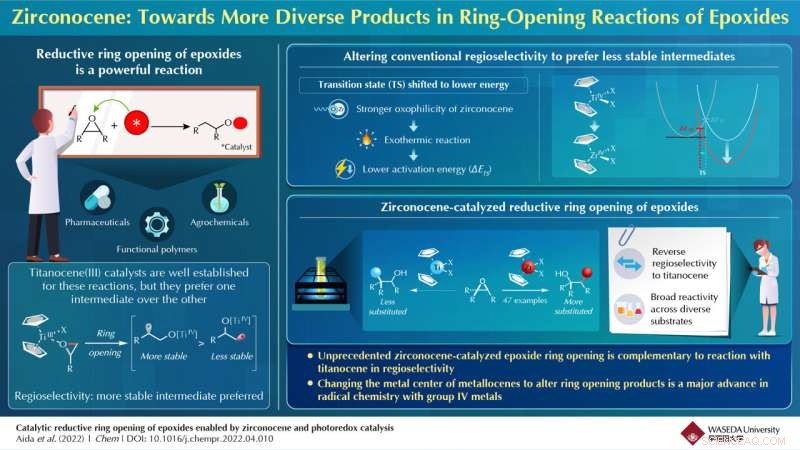
Los investigadores demuestran, por primera vez, una reacción de apertura de anillo de epóxido catalizada por zirconoceno bajo luz visible. Crédito:Universidad de Waseda
Los epóxidos pertenecen a una clase de compuestos orgánicos llamados "éteres cíclicos" que se caracterizan por un anillo de tres átomos. Son compuestos fácilmente disponibles que se encuentran en agentes medicinales y agroquímicos, así como en productos naturales. Los epóxidos son un valioso precursor industrial, ya que permiten la síntesis de una amplia gama de importantes alcoholes, polímeros funcionales, productos agroquímicos y productos farmacéuticos a través de una reacción reductora de apertura del anillo. Durante los últimos 30 años, el titanoceno (III) ha sido el único catalizador representativo para catalizar la reacción de apertura del anillo. Sin embargo, las reacciones catalizadas por titanoceno son regioselectivas, lo que significa que se prefieren algunos productos sobre otros. En su caso, los productos preferidos son los obtenidos a partir de radicales más estables (frente a los radicales menos estables). El mecanismo subyacente a esta regioselectividad aún no está claro.
En un nuevo estudio publicado en Chem , un equipo de químicos de Japón dirigido por el profesor Junichiro Yamaguchi, los estudiantes de posgrado Kazuhiro Aida y Marina Hirao, y el profesor asistente Eisuke Ota del Departamento de Química Aplicada de la Universidad de Waseda, investigaron el zirconoceno, la contraparte de zirconio del titanoceno, como un catalizador alternativo potencial. para la reacción de apertura del anillo. "El circonio es más oxofílico en comparación con el titanio, lo que significa que tiene una mayor tendencia a interactuar con los átomos de oxígeno. Esto cambia la vía de la reacción química. Descubrimos que cambiar el centro metálico de titanio a circonio hace que la reacción de apertura del anillo sea más exotérmica, lo que disminuye la energía de activación necesaria para la apertura del anillo", explica Ota. En su trabajo, el equipo informó, por primera vez, de una catálisis basada en zirconoceno de la apertura del anillo de epóxido en presencia de luz visible únicamente.
Alentados por sus hallazgos, los investigadores demostraron su enfoque novedoso para una amplia gama de sustratos y grupos funcionales, incluidos los productos naturales. Sin embargo, el aspecto más interesante de su enfoque fue que las reacciones catalizadas por zirconoceno dieron lugar a productos con regioselectividad complementaria opuesta en comparación con los obtenidos con reacciones catalizadas por titanoceno. Esto permitió una ruta de fácil acceso a muchos productos alcohólicos escurridizos que no se podían obtener antes debido a problemas de regioselectividad.
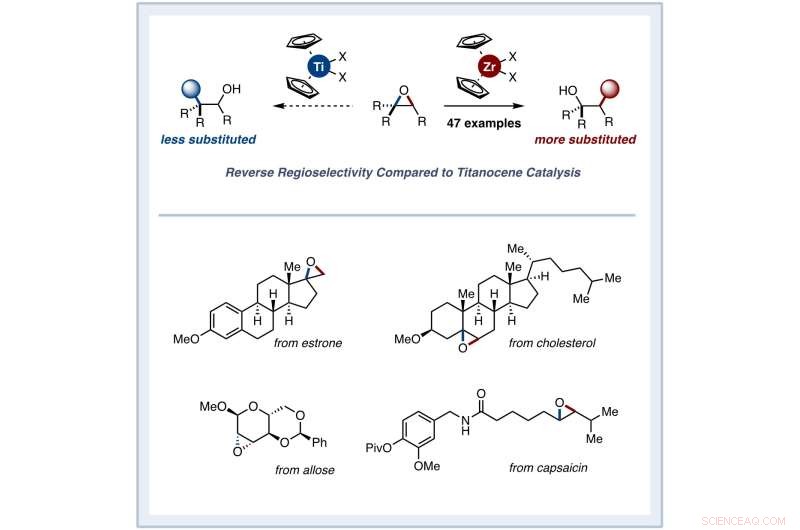
Un equipo de químicos de la Universidad de Waseda, Japón, demostró recientemente una reacción de catálisis fotorredox basada en zirconoceno que permite una apertura de anillo reductor de epóxidos con una regioselectividad inversa en comparación con las reacciones mediadas por titanoceno. Crédito:Junichiro Yamaguchi de la Universidad de Waseda
Además, el circonio ofrece otra ventaja sobre el titanio. Como explica Yamaguchi, "el circonio es uno de los elementos más abundantes en la corteza terrestre, lo que hace que esté fácilmente disponible y sea de bajo costo. Dado que nuestra reacción puede catalizarse con luz visible, también es respetuosa con el medio ambiente. Con mejoras adicionales, nuestro método podría ser un contribuyente clave a la química verde".
En general, los resultados de este estudio brindan una nueva perspectiva que podría contribuir en gran medida a ampliar significativamente el alcance de las reacciones de apertura del anillo de epóxido reductor y agregar una nueva dimensión a la química radical. El sistema 'cargado por resorte' hace estallar el fósforo en anillos moleculares