
El dióxido de carbono (representado en rojo y blanco a la izquierda) es el principal gas de efecto invernadero que calienta la Tierra y se emite en grandes cantidades en los gases de combustión de las plantas industriales y de energía. Un nuevo método para eliminar el CO2 de estos gases de combustión consiste en canalizar las emisiones a través de un material poroso basado en el químico melamina (centro). DETA, un compuesto químico dentro de la melamina porosa, atrapa el CO2 y lo elimina del gas, con nitrógeno expulsado a la atmósfera. Crédito:Haiyan Mao y Jeffrey Reimer, UC Berkeley
Usando un polímero económico llamado melamina, el componente principal de Formica, los químicos han creado una forma económica, fácil y eficiente de energía para capturar el dióxido de carbono de las chimeneas, un objetivo clave para los Estados Unidos y otras naciones en su intento de reducir las emisiones de gases de efecto invernadero. .
El proceso para sintetizar el material de melamina, publicado esta semana en la revista Science Advances , podría reducirse potencialmente para capturar las emisiones de los gases de escape de los vehículos u otras fuentes móviles de dióxido de carbono. El dióxido de carbono de la quema de combustibles fósiles representa aproximadamente el 75 % de todos los gases de efecto invernadero producidos en los EE. UU.
El nuevo material es fácil de fabricar y requiere principalmente polvo de melamina listo para usar, que hoy cuesta alrededor de $ 40 por tonelada, junto con formaldehído y ácido cianúrico, un químico que, entre otros usos, se agrega con cloro a las piscinas.
"Queríamos pensar en un material de captura de carbono que se derivara de fuentes que fueran realmente baratas y fáciles de conseguir. Entonces, decidimos comenzar con la melamina", dijo Jeffrey Reimer, profesor de la Escuela de Graduados en el Departamento de Química y Ingeniería Biomolecular en la Universidad de California, Berkeley, y uno de los autores correspondientes del artículo.
La llamada red porosa de melamina captura el dióxido de carbono con una eficiencia comparable a los primeros resultados de otro material relativamente reciente para la captura de carbono, estructuras orgánicas metálicas o MOF. Los químicos de UC Berkeley crearon el primer MOF de captura de carbono de este tipo en 2015, y las versiones posteriores han demostrado ser aún más eficientes para eliminar el dióxido de carbono de los gases de combustión, como los de una planta de energía alimentada con carbón.
Pero Haiyan Mao, becario postdoctoral de UC Berkeley y primer autor del artículo, dijo que los materiales a base de melamina usan ingredientes mucho más baratos, son más fáciles de fabricar y son más eficientes energéticamente que la mayoría de los MOF. El bajo costo de la melamina porosa significa que el material podría implementarse ampliamente.
"En este estudio, nos enfocamos en el diseño de materiales más económicos para la captura y el almacenamiento y en dilucidar el mecanismo de interacción entre CO2 y el material", dijo Mao. "Este trabajo crea un método de industrialización general hacia el CO2 sostenible captura mediante redes porosas. Esperamos poder diseñar un accesorio futuro para capturar los gases de escape de los automóviles, o tal vez un accesorio para un edificio o incluso un revestimiento en la superficie de los muebles".
El trabajo es una colaboración entre un grupo de UC Berkeley dirigido por Reimer; un grupo de la Universidad de Stanford dirigido por Yi Cui, quien es director del Instituto Precourt para la Energía, profesor visitante Somorjai Miller en UC Berkeley y ex becario postdoctoral de UC Berkeley; Profesor de la Escuela de Graduados de UC Berkeley Alexander Pines; y un grupo de la Universidad Texas A&M dirigido por Hong-Cai Zhou. Jing Tang, becario postdoctoral en Stanford y el Centro Acelerador Lineal de Stanford y académico visitante en UC Berkeley, es coautor junto con Mao.
Neutralidad en carbono para 2050
Si bien eliminar la quema de combustibles fósiles es esencial para detener el cambio climático, una importante estrategia provisional es capturar las emisiones de dióxido de carbono, el principal gas de efecto invernadero, y almacenar el gas bajo tierra o convertir el CO2 en productos utilizables. El Departamento de Energía de EE. UU. ya ha anunciado proyectos por un total de 3180 millones de dólares para impulsar tecnologías avanzadas y comercialmente escalables para la captura, utilización y secuestro de carbono (CCUS) a fin de alcanzar un ambicioso CO2 de gases de combustión. objetivo de eficiencia de captura del 90%. El objetivo final de EE. UU. es cero emisiones netas de carbono para 2050.
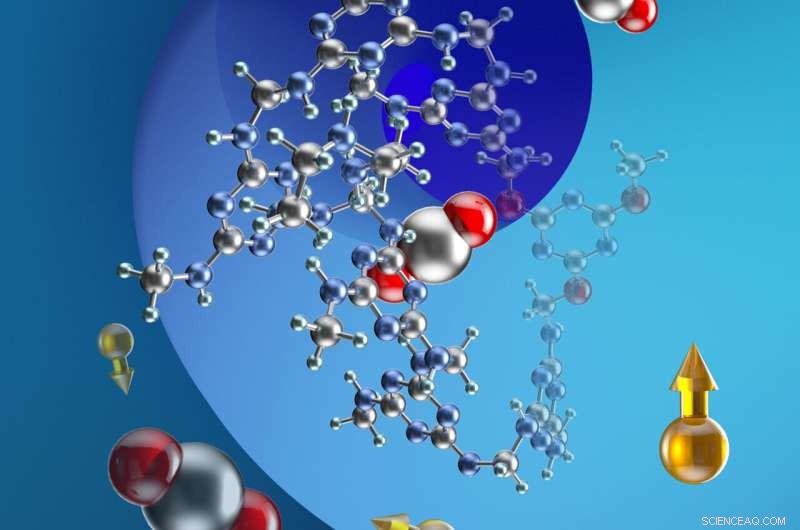
Investigadores de UC Berkeley desarrollaron una nueva familia de materiales de estado sólido escalables y sostenibles (redes nanoporosas de melamina estabilizadas con ácido cianúrico, añadidas con poliamina) que adsorben CO2 espontáneamente para capturar y almacenar carbono. En el gráfico, las moléculas de dióxido de carbono (carbono en plata, oxígeno en rojo) interactúan con las aminas del material (nitrógeno en azul, hidrógeno en verde), lo que permite que el material absorba el gas de las emisiones de las chimeneas. Las bolas amarillas con flechas representan isótopos de carbono-13 y sus espines nucleares, que se emplearon en estudios de RMN del material. Crédito:Haiyan Mao y Jeffrey Reimer, UC Berkeley
Pero la captura de carbono está lejos de ser comercialmente viable. La mejor técnica actual consiste en canalizar los gases de combustión a través de aminas líquidas, que se unen al CO2 . Pero esto requiere grandes cantidades de energía para liberar el dióxido de carbono una vez que se une a las aminas, de modo que pueda concentrarse y almacenarse bajo tierra. La mezcla de aminas debe calentarse entre 120 y 150 grados Celsius (250-300 grados Fahrenheit) para regenerar el CO2 .
En cambio, la red porosa de melamina con DETA y modificación con ácido cianúrico captura CO2 a unos 40 grados centígrados, ligeramente por encima de la temperatura ambiente, y lo libera a 80 grados centígrados, por debajo del punto de ebullición del agua. El ahorro de energía proviene de no tener que calentar la sustancia a altas temperaturas.
En su investigación, el equipo de Berkeley/Stanford/Texas se centró en el polímero de melamina común, que se utiliza no solo en la fórmica, sino también en vajillas y utensilios económicos, revestimientos industriales y otros plásticos. El tratamiento del polvo de melamina con formaldehído, que los investigadores hicieron en cantidades de kilogramos, crea poros a nanoescala en la melamina que los investigadores pensaron que absorbería CO2 .
Mao dijo que las pruebas confirmaron que la melamina tratada con formaldehído absorbió CO2 algo, pero la adsorción podría mejorarse mucho agregando otro químico que contiene amina, DETA (dietilentriamina), para unir CO2 . Posteriormente, ella y sus colegas descubrieron que agregar ácido cianúrico durante la reacción de polimerización aumentaba drásticamente el tamaño de los poros y mejoraba radicalmente el CO2 eficiencia de captura:casi todo el dióxido de carbono en una mezcla de gas de combustión simulada se absorbió en aproximadamente 3 minutos.
La adición de ácido cianúrico también permitió que el material se usara una y otra vez.
Mao y sus colegas realizaron estudios de resonancia magnética nuclear (RMN) de estado sólido para comprender cómo interactuaban el ácido cianúrico y el DETA para hacer que la captura de carbono fuera tan eficiente. Los estudios demostraron que el ácido cianúrico forma fuertes enlaces de hidrógeno con la red de melamina que ayuda a estabilizar el DETA, evitando que se filtre fuera de los poros de la melamina durante ciclos repetidos de captura y regeneración de carbono.
"Lo que Haiyan y sus colegas pudieron mostrar con estas técnicas elegantes es exactamente cómo se entremezclan estos grupos, cómo se mezclan exactamente los CO2. reacciona con ellos y que, en presencia de este ácido cianúrico que abre los poros, puede reciclar el CO2 encendido y apagado muchas veces con una capacidad que es bastante buena", dijo Reimer. "Y la tasa a la que el CO2 adsorbe es en realidad bastante rápido, en relación con algunos otros materiales. Así pues, todos los aspectos prácticos a escala de laboratorio de este material para CO2 captura se han cumplido, y es increíblemente barato y fácil de hacer".
"Utilizando técnicas de resonancia magnética nuclear de estado sólido, dilucidamos sistemáticamente con detalles atómicos sin precedentes el mecanismo de reacción de las redes amorfas con CO2 ", dijo Mao. "Para la comunidad energética y ambiental, este trabajo crea una familia de redes de estado sólido de alto rendimiento junto con una comprensión profunda de los mecanismos, pero también fomenta la evolución de la investigación de materiales porosos a partir de prueba y error. métodos para la modulación racional, paso a paso, a nivel atómico".
Los grupos de Reimer y Cui continúan modificando el tamaño de los poros y los grupos de aminas para mejorar la eficiencia de captura de carbono de las redes porosas de melamina, manteniendo la eficiencia energética. Esto implica el uso de una técnica llamada química combinatoria dinámica para variar las proporciones de los ingredientes para lograr CO2 efectivo, escalable, reciclable y de alta capacidad. capturar.
Reimer y Mao también han colaborado estrechamente con el grupo Cui de Stanford para sintetizar otros tipos de materiales, incluidas membranas nanoporosas jerárquicas (una clase de nanocompuestos combinados con una esfera de carbono y óxido de grafeno) y carbonos nanoporosos jerárquicos hechos de madera de pino, para adsorber carbono. dióxido. Reimer desarrolló la RMN de estado sólido específicamente para caracterizar el mecanismo por el cual los materiales sólidos interactúan con el dióxido de carbono, con el fin de diseñar mejores materiales para la captura de carbono del medio ambiente y el almacenamiento de energía. Cui desarrolló una plataforma sólida y sostenible de estado sólido y técnicas de fabricación para crear nuevos materiales para abordar el cambio climático y el almacenamiento de energía. La captura de carbono adquiere forma de esponja con un nuevo método rentable