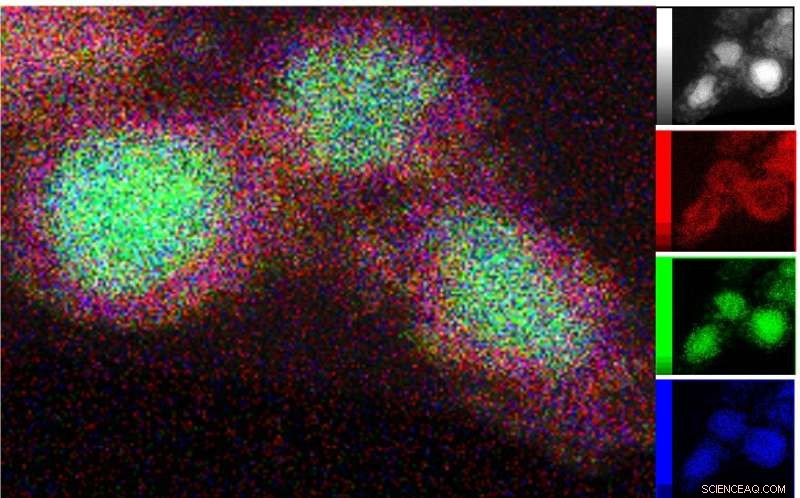
La microscopía electrónica de transmisión (TEM) de la fase catalíticamente activa se combinó con la espectroscopia de rayos X de energía dispersiva para mapear la distribución de Ni (verde), Si (azul) y oxígeno (rojo) alrededor de las estructuras de núcleo y capa. Crédito:P. Menezes /HZB/TU Berlín
La electrólisis puede ser un concepto familiar de las lecciones de química en la escuela:dos electrodos se sumergen en agua y se ponen bajo tensión. Este voltaje hace que las moléculas de agua se descompongan en sus componentes y las burbujas de gas se elevan en los electrodos:se forma gas oxígeno en el ánodo, mientras que se forman burbujas de hidrógeno en el cátodo. La electrólisis podría producir hidrógeno en un CO2 -manera neutral—siempre y cuando la electricidad requerida sea generada por formas de energía libres de fósiles como el sol o el viento.
El único problema es que estas reacciones no son muy eficientes y son extremadamente lentas. Para acelerar las reacciones se utilizan catalizadores a base de metales preciosos y raros como el platino, el rutenio o el iridio. Sin embargo, para un uso a gran escala, tales catalizadores deben consistir en elementos muy baratos y ampliamente disponibles.
Nanoestructuras químicamente inducidas
Para acelerar la reacción de evolución del oxígeno en el ánodo, los materiales a base de níquel se consideran buenos candidatos. El níquel es resistente a la corrosión, apenas tóxico y también económico. Sin embargo, hasta ahora, los procesos de alta temperatura que consumen mucha energía se han utilizado principalmente para producir materiales catalizadores a base de níquel.
Un equipo dirigido por el Dr. Prashanth Menezes (HZB/TU Berlín) ha encontrado ahora una forma "química suave" de producir un catalizador eficiente basado en nanocristales intermetálicos de níquel-silicio.
“Combinamos el elemento níquel con silicio, el segundo elemento más abundante en la corteza terrestre, y logramos la nanoestructuración mediante una reacción química. El material resultante tiene excelentes propiedades catalíticas”, dice Menezes. El Ni2 cristalino Si sirvió como precatalizador para la reacción de evolución de oxígeno alcalino en el ánodo y sufre una transformación superficial para formar hidróxido de níquel (oxi) como catalizador activo en condiciones de funcionamiento. Sorprendentemente, la electrólisis del agua se combinó con una reacción de oxidación orgánica de valor agregado en la que se produjo la electrosíntesis de compuestos de nitrilo industrialmente valiosos a partir de aminas primarias con conversión selectiva y completa en condiciones suaves. Dichos métodos electrosintéticos pueden impulsar la generación de hidrógeno en el cátodo y, al mismo tiempo, proporcionar acceso a productos industriales valiosos en el ánodo.
Más eficiente y estable
En comparación con los catalizadores modernos basados en níquel, cobalto, hierro, rutenio e iridio, el Ni2 nanoporoso Si es significativamente más activo y permanece estable durante un tiempo de reacción más prolongado en condiciones de nivel industrial. Entender el comportamiento de Ni2 Más detalladamente, el equipo combinó diferentes métodos de medición, incluidos análisis elementales, microscopía electrónica y mediciones espectroscópicas modernas en BESSY II. "En el futuro, incluso los electrolizadores industriales de agua alcalina podrían equiparse con una capa de este siliciuro de níquel nanoporoso", dice Menezes.
La investigación fue publicada en Advanced Energy Materials . El níquel recubierto de carbono permite una celda de combustible de hidrógeno libre de metales preciosos