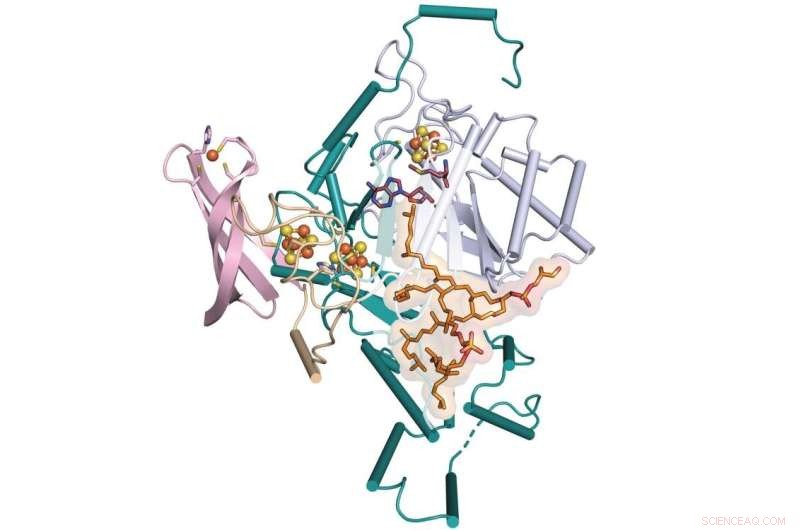
Un equipo de Penn State y la Universidad de Illinois Urbana-Champaign ha determinado el paso que falta en la formación de una molécula llamada GDGT, que es un candidato prometedor para su uso como indicador del clima pasado. El equipo determinó la estructura cristalina de rayos X de una enzima que facilita este proceso llamada GDGT/MAS, que se muestra aquí unida a cofactores adicionales. Crédito:Booker Lab/Penn State
Ahora se ha descifrado el paso que faltaba en la formación de una molécula lipídica que permite a ciertos organismos unicelulares sobrevivir en los entornos más extremos de la Tierra. Esta nueva comprensión, descubierta por un equipo de bioquímicos de Penn State y la Universidad de Illinois Urbana-Champaign, podría mejorar la capacidad de los lípidos para usarse como indicador de temperatura a lo largo del tiempo geológico.
El lípido, llamado glicerol dibifitanil glicerol tetraéter (GDGT), se encuentra en la membrana celular de algunas especies de arqueas, organismos unicelulares que originalmente se pensaba que eran bacterias pero ahora se consideran un grupo separado. Este lípido proporciona la estabilidad para que algunas especies prosperen en ambientes con temperaturas, salinidad o acidez extremadamente altas, como fuentes termales en el océano, aguas termales y aguas hipersalinas. La estabilidad única de GDGT también permite que se detecte cientos o incluso miles de años después de la muerte del organismo. Debido a que estos organismos tienden a producir más GDGT a temperaturas más altas, se considera un candidato prometedor para estimar la temperatura a lo largo del tiempo geológico.
"Para que GDGT se use con precisión como un proxy para reconstruir los cambios en las temperaturas geológicas, los científicos deben comprender mejor cómo se hace, qué genes lo codifican y qué especies pueden crearlo", dijo Squire Booker, bioquímico de Penn State. , investigador del Instituto Médico Howard Hughes y líder del equipo de investigación. "Pero, hasta ahora, faltaba un paso en la formación de este lípido. Utilizamos técnicas de imagen junto con métodos químicos y bioquímicos para deconstruir la ruta química de este paso faltante".
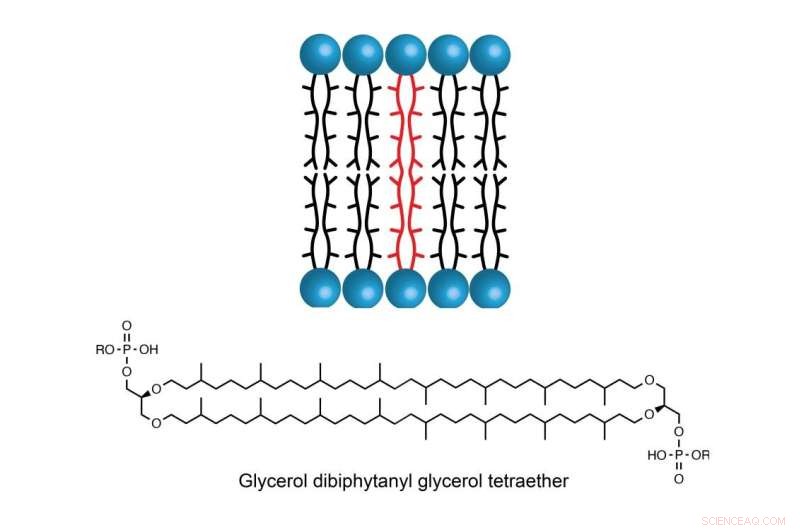
La molécula GDGT se encuentra en la membrana celular de algunas especies de arqueas, lo que permite que los organismos unicelulares prosperen en entornos con temperaturas, salinidad o acidez extremadamente altas. Crédito:Booker Lab/Penn State
La estabilidad de GDGT se debe en parte a sus dos largas cadenas de hidrocarburos que se extienden por toda la membrana. Pero la forma en que estas dos cadenas se unen ha intrigado a los científicos durante décadas.
"El acoplamiento de los carbonos al final de las dos cadenas de hidrocarburos es un desafío químico porque son inertes, son químicamente inactivos", dijo Cody Lloyd, estudiante de posgrado en Penn State y miembro del equipo de investigación. "Identificamos la enzima que activa estos carbonos terminales y hace posible este acoplamiento. Además, ahora conocemos el gen que codifica esta enzima, lo que debería mejorar el uso de GDGT como indicador de climas pasados".
La enzima que facilita el acoplamiento de las dos cadenas hidrocarbonadas pertenece a una clase de proteínas llamadas proteínas radicales SAM, que se sabe que desempeñan un papel importante en una variedad de reacciones químicas, incluida la producción de antibióticos, la modificación de proteínas, ADN y ARN, y la creación de varias biomoléculas.
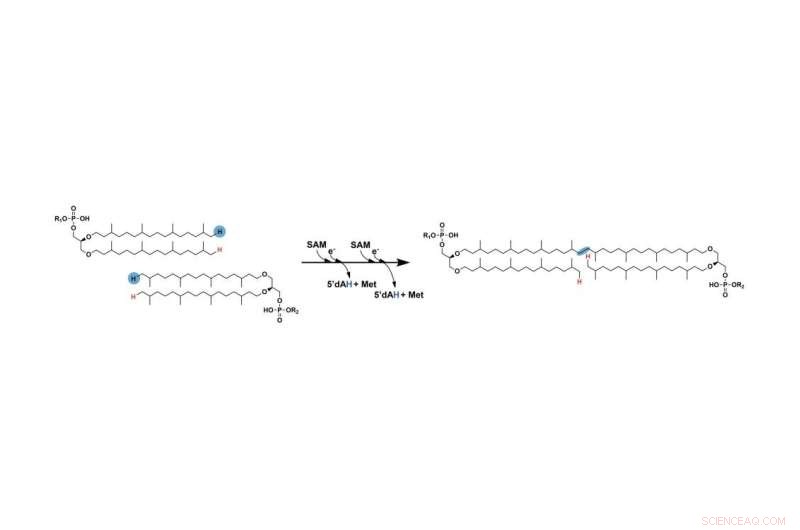
El paso que antes faltaba en la formación de GDGT consiste en conectar dos largas cadenas de hidrocarburos. Los dos hidrógenos marcados en azul finalmente se eliminan y las cadenas finalmente se conectan en los lugares donde se eliminaron esos átomos. Una enzima SAM radical facilita este proceso. Crédito:Booker Lab/Penn State
El primer paso es similar al de otras reacciones que involucran enzimas SAM radicales:la enzima SAM radical usa uno de sus grupos de hierro y azufre para escindir una molécula llamada S-adenosil-L-metionina (SAM), produciendo un "radical libre". o un electrón desapareado que es altamente reactivo y ayuda a que la reacción avance. Luego, el radical arranca un átomo de hidrógeno del carbono al final de la cadena. En un paso posterior, este proceso se repite con la segunda cadena utilizando una segunda molécula de SAM.
"En última instancia, los carbonos al final de cada una de las cadenas terminan uniéndose entre sí en la posición donde se eliminaron los átomos de hidrógeno", dijo Lloyd. "Pero una vez que se elimina el hidrógeno de la primera cadena, se vuelve tan inestable que podría reaccionar con casi cualquier cosa. Para evitar temporalmente que la primera cadena reaccione con cualquier objetivo, el carbono se une a un átomo de azufre de otro de los tres grupos de hierro y azufre de la enzima".
Una vez que se ha eliminado el hidrógeno de la segunda cadena, el radical resultante anima a la primera cadena a eliminarse del grupo de hierro y azufre de la enzima y, en cambio, se une a la segunda cadena. Esto da como resultado que las dos cadenas se unan, completando el paso faltante en la formación de GDGT. Los investigadores presentan sus resultados en un artículo que aparece en línea e impreso en la edición del 1 de septiembre de la revista Nature .
"Este es un uso completamente nuevo de un grupo de hierro y azufre, y este es el primer ejemplo en la naturaleza del acoplamiento de dos átomos de carbono completamente inertes con esta configuración electrónica, que los químicos llaman hibridación sp3", dijo Booker. "Ha habido mucho interés en crear este tipo de enlaces carbono-carbono a partir de carbonos con hibridación sp3 como parte de productos farmacéuticos y otros productos industriales. La naturaleza ha tenido millones de años para resolver esto, por lo que continuamos observando la naturaleza. en busca de inspiración para reacciones sintéticas, como este novedoso uso de un grupo de hierro y azufre". La clave para la formación de un poderoso antibiótico ahora está clara