
Una nueva técnica permite a los científicos mapear cómo fluyen los electrones en el complejo de evolución de oxígeno del Fotosistema II. El objetivo final es montar una película atómica de todo el proceso, incluido el elusivo estado transitorio que une los átomos de oxígeno de dos moléculas de agua para formar moléculas de oxígeno. Crédito:Greg Stewart / SLAC National Accelerator Laboratory
El fotosistema II es un complejo proteico en plantas, algas y cianobacterias que se encargan de dividir el agua y producir el oxígeno que respiramos. En los ultimos años, una colaboración internacional entre científicos del Laboratorio Nacional Lawrence Berkeley del Departamento de Energía, El Laboratorio Nacional Acelerador de SLAC y varias otras instituciones han podido observar varios pasos de este ciclo de división del agua a la temperatura a la que ocurre en la naturaleza.
Ahora, el equipo ha utilizado el mismo método para concentrarse en un paso clave en el que una molécula de agua se mueve para unir los átomos de manganeso y calcio en el complejo catalítico que divide el agua para producir oxígeno respirable. Lo que aprendieron los acerca un paso más a obtener una imagen completa de este proceso natural, lo que podría informar a la próxima generación de sistemas fotosintéticos artificiales que producen energía limpia y renovable a partir de la luz solar y el agua. Sus resultados fueron publicados en el procedimientos de la Academia Nacional de Ciencias hoy dia.
"Demostramos que es posible realizar estas mediciones en iteraciones anteriores de este trabajo, pero nunca tuvimos la resolución espacial o los puntos de tiempo suficientes para profundizar realmente en estos detalles más finos, "dice el coautor Uwe Bergmann, un científico distinguido del personal de SLAC. "Después de optimizar cuidadosamente este experimento durante muchos años, perfeccionamos nuestra capacidad para realizar mediciones con una calidad lo suficientemente alta como para ver estos pequeños cambios por primera vez ".
La brigada del cubo
Durante la fotosíntesis, el complejo generador de oxígeno, un grupo de cuatro átomos de manganeso y un átomo de calcio conectados por átomos de oxígeno, ciclos a través de cuatro estados de oxidación estables, conocido como S0 a S3, cuando se expone a la luz solar.
En un campo de béisbol S0 sería el comienzo del juego cuando un jugador en la base de casa está listo para ir al bate. S1-S3 serían jugadores en primer lugar, segundo, y tercero. Cada vez que un bateador conecta con una pelota, o el complejo absorbe un fotón de luz solar, el jugador en el campo avanza una base. Cuando se golpea la cuarta bola, el jugador se desliza a casa, anotar una carrera o, en el caso del fotosistema II, liberando oxígeno respirable. Esta investigación se centró en la transición de S2 a S3, el último estado intermedio estable antes de que se produzca una molécula de oxígeno.
El complejo generador de oxígeno está rodeado de agua y proteínas. En el paso que miraron los científicos, el agua fluye a través de un camino hacia el complejo, donde una molécula de agua finalmente forma un puente entre un átomo de manganeso y un átomo de calcio. Esta molécula de agua probablemente proporciona uno de los átomos de oxígeno en la molécula de oxígeno producida al final del ciclo.
Usando el láser de rayos X de fuente de luz coherente Linac (LCLS) de SLAC, Los investigadores descubrieron que las moléculas de agua se transportan al complejo como a través de una brigada de cubos:se mueven en muchos pasos pequeños de un extremo del camino al otro. También demostraron que el átomo de calcio dentro del complejo podría estar involucrado en el transporte del agua.
"Es como la cuna de Newton, "dice Vittal Yachandra, uno de los autores del estudio y científico senior en Berkeley Lab que ha estado trabajando en Photosystem II durante más de 35 años. "Por lo general, en el agua líquida, las cosas se mueven constantemente, pero ahora nos encontramos en esta fascinante situación en la que algunas de las moléculas de agua alrededor del grupo de manganeso cambian de posición, mientras que otros están siempre en el mismo lugar. Puedes repetir el experimento 10, 000 veces y seguirán sentados en el mismo lugar ".
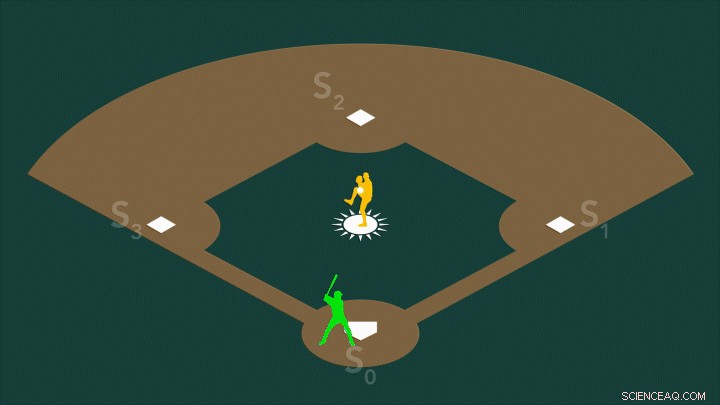
En el fotosistema II, el centro divisor de agua recorre cuatro estados estables, S0-S3. En un campo de béisbol S0 sería el comienzo del juego cuando un bateador en la base de home está listo para batear. S1-S3 serían los jugadores esperando primero, segundo, y tercero. El centro se eleva al siguiente estado cada vez que absorbe un fotón de luz solar, al igual que un jugador en el campo avanza una base cada vez que un bateador conecta con una pelota. Cuando se golpea la cuarta bola, el jugador se desliza a casa, anotar una carrera o, en el caso del Fotosistema II, liberando el oxígeno que respiramos. Crédito:Greg Stewart / SLAC National Accelerator Laboratory
Trabajando en tándem
En LCLS, El equipo extrajo muestras de cianobacterias con pulsos ultrarrápidos de rayos X para recopilar datos de espectroscopia y cristalografía de rayos X para mapear cómo fluyen los electrones en el complejo de evolución de oxígeno del Fotosistema II. A través de esta técnica, pueden mapear simultáneamente su estructura y descubrir información sobre el proceso químico en el grupo de manganeso.
Previamente, los investigadores habían utilizado esta técnica para asegurarse de que la muestra estuviera intacta y, lo que es más importante, también en el estado químico intermedio correcto. Este artículo marca la primera vez que los investigadores pudieron fusionar los dos conjuntos de información para ver las conexiones entre los cambios estructurales y químicos. Esto permitió a los investigadores observar cómo se desarrollan los pasos en tiempo real, y aprender cosas nuevas sobre la reacción.
"Es emocionante ver la 'causa y efecto' de los cambios inducidos por la absorción de luz a medida que ocurren, "Dice Yachandra.
"Es fácil olvidar lo crítico que es el entorno y cómo permite estos procesos realmente complicados, "dice Junko Yano, uno de los autores del estudio y científico senior en Berkeley Lab. "La vida no ocurre en el vacío; todos los componentes tienen que trabajar juntos para hacer posible la reacción. Estos resultados nos muestran cómo las moléculas de proteína y agua alrededor del grupo catalítico trabajan en conjunto para producir oxígeno. Nuestros resultados iniciarán una nueva forma de pensar e inspirar nuevos tipos de preguntas ".
Listo, colocar, ¡acción!
Más allá de la fotosíntesis, Yano dice, esta técnica se puede aplicar a otros sistemas enzimáticos para hacer instantáneas más detalladas de reacciones catalíticas.
"Nos permite conectar la biología estructural y la química de los sistemas para comprender y controlar reacciones químicas complicadas, " ella dice.
El objetivo final del proyecto es reconstruir una película atómica utilizando muchas instantáneas realizadas a lo largo del proceso, incluido el escurridizo estado transitorio al final que une dos átomos de oxígeno de dos moléculas de agua para formar la molécula de oxígeno.
"Nuestro sueño es recorrer todo el ciclo de reacción y obtener suficientes puntos de tiempo y detalles para que pueda ver cómo se desarrolla todo el proceso, desde el primer fotón de luz que entra hasta la primera molécula de oxígeno respirable que sale, "dice el coautor Jan Kern, un científico de planta en Berkeley Lab. "Hemos estado construyendo el escenario para esta película, estableciendo nuestra técnica y mostrando lo que es posible. Ahora las cámaras finalmente están rodando y podemos empezar a trabajar en el largometraje ".