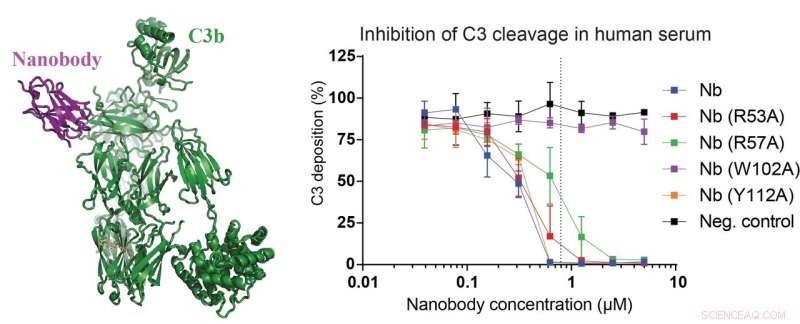
El panel izquierdo de la figura muestra la estructura del nanocuerpo recientemente desarrollado (magenta) unido a un fragmento C3 llamado C3b (verde). En los paneles de la derecha, datos que demuestran que el nanocuerpo y sus mutantes son capaces de inhibir la escisión de C3 en un 15 por ciento de suero humano. Los investigadores también construyeron un nanocuerpo mutante que pierde por completo su efecto inhibidor sobre la escisión de C3 (curva púrpura), lo que lo convierte en un control negativo perfecto. Crédito:Rasmus Kjeldsen Jensen y Janus Asbjørn Schatz-Jakobsen, Universidad de Aarhus
Investigadores del Departamento de Biología Molecular y Genética y del Departamento de Biomedicina de la Universidad de Aarhus han desarrollado y descrito en colaboración un anticuerpo de llama que podría tener un impacto significativo para futuros diagnósticos y tratamientos de, p.ej., enfermedades renales.
El equipo de investigación estudió una proteína llamada C3 de la parte del sistema inmunológico innato conocida como sistema del complemento. Tras el reconocimiento de organismos patógenos o células corporales moribundas, C3 es escindido por enzimas sanguíneas como parte de un mecanismo de defensa. Estas enzimas se conocen como convertasas C3, y la escisión de C3 da como resultado dos fragmentos. El fragmento llamado 3b se une directamente a los patógenos, mientras que el otro fragmento recluta y estimula a las células inmunitarias para eliminar al objetivo.
En una persona sana las células están protegidas contra los efectos de la escisión de C3. Sin embargo, como resultado de mutaciones en el ADN, esta protección podría perderse, aumentando el riesgo de desarrollar trastornos inflamatorios crónicos o enfermedades autoinmunes. Por mucho tiempo, los investigadores se han centrado en el desarrollo de agentes que eviten dicha activación indeseable del complemento. Por esta razón, desarrollaron el anticuerpo de llama para prevenir la escisión de C3. Los anticuerpos de llama también se conocen como nanocuerpos debido a su pequeño tamaño, y en comparación con los anticuerpos normales, son fáciles de desarrollar y significativamente más baratos de producir.
"La tecnología utilizada para desarrollar y producir estos nanocuerpos se conoce desde hace más de dos décadas, ", dice Gregers Rom Andersen." Y, por lo tanto, es algo sorprendente que seamos los primeros en el mundo en desarrollar un nanocuerpo que inhibe el sistema del complemento ".
Al exponer cristales a rayos X y correlacionar los resultados con los datos de microscopía electrónica, los investigadores han descrito cómo su nanocuerpo se une a C3 con gran detalle.
"La estructura cristalina de nuestro nanocuerpo unido a C3 respalda nuestros modelos propuestos anteriormente que describen cómo las convertasas del complemento reconocen sus sustratos y, por lo tanto, explica claramente por qué nuestro nanocuerpo ejerce su efecto inhibidor sobre la escisión de C3. Nuestros resultados también mejoran la comprensión básica de cómo esto mecanismo esencial dentro del sistema del complemento funciona. Al comparar con estructuras proteicas previamente publicadas, Además, podemos explicar por qué nuestro nanocuerpo inhibe la formación de las convertasas C3, nuestro nanocuerpo tiene un efecto 'doble inhibidor' por así decirlo, "explica Rasmus Kjeldsen Jensen.
Además del trabajo que describe el complejo de nanocuerpos C3, el equipo de investigación también ha realizado varios experimentos de laboratorio utilizando suero tanto de ratones como de humanos. Estos resultados confirman las observaciones de la estructura atómica y revelan claramente que su nanocuerpo recientemente desarrollado inhibe la escisión de C3 tanto en suero humano como murino. Esto último es importante, ya que los ratones se utilizan a menudo como modelos de enfermedades.
"Nuestros experimentos en suero son importantes, ya que muestran que nuestro nanocuerpo funciona en condiciones fisiológicas, donde el sistema del complemento ejerce naturalmente su función. Estos resultados indican que nuestro nanocuerpo podría usarse en el tratamiento de enfermedades causadas por la sobreactivación del sistema del complemento. Como ejemplo, parte del riñón no está protegida contra el complemento en el mismo grado que otros tejidos, y en este caso nuestro nanocuerpo podría ser un candidato para detener la progresión de la enfermedad impulsada por el complemento, "dice Gregers Rom Andersen". Sin embargo, También descubrimos que nuestro nanocuerpo es capaz de inhibir los efectos protectores que nuestro propio cuerpo normalmente ejerce contra el complemento. y, por lo tanto, se debe tener mucho cuidado y evaluar meticulosamente los posibles efectos secundarios del tratamiento terapéutico de enfermedades utilizando nuestro nanocuerpo, ", concluye Gregers Rom Andersen.
La base de este trabajo fue establecida por los dos profesores asistentes Kasper Røjkjær Andersen y Nick Stub Laursen del Departamento de Biología Molecular y Genética, quienes fueron los primeros en Dinamarca en desarrollar y producir sistemáticamente nanocuerpos a gran escala. Sin embargo, la fuerza impulsora del proyecto fue el estudiante de doctorado Rasmus Kjeldsen Jensen bajo la supervisión del profesor Gregers Rom Andersen, quien en la caracterización del nanocuerpo contó con la asistencia de los dos estudiantes de doctorado Trine Amalie Fogh Gadeberg y Rasmus Pihl.