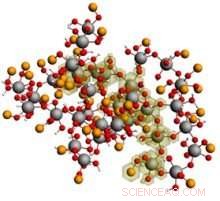
Las soluciones alcalinas de iones de aluminio y sodio forman geles complejos (ver ejemplo) compuestos por redes de centros de metal de aluminio. Durante la cristalización, estas redes liberan iones cuya estructura está influenciada por la presencia de grandes concentraciones de iones sodio y la organización soluto / solvente. Crédito:Laboratorio de Ciencias Moleculares Ambientales
Investigadores del Centro de Investigación de la Frontera Energética de Dinámica Interfacial en Ambientes y Materiales Radiactivos (IDREAM) cuantificaron especies de Al3 + pentacoordinadas transitorias durante la cristalización de gibbsita a partir de geles de aluminio hidratados en soluciones de hidróxido de sodio concentrado. La investigación muestra que los electrolitos concentrados en solución afectan los enlaces de hidrógeno, interacciones de iones, y geometrías de coordinación en formas actualmente impredecibles.
Estos estudios mecanicistas apoyan el desarrollo de nuevos diagramas de flujo de procesos para acelerar el procesamiento de desechos radiactivos en dos sitios del Departamento de Energía. Más lejos, los estudios pueden proporcionar rutas que consuman menos energía para la producción industrial de aluminio.
La gibbsita (α-Al (OH) 3) es un recurso mineral importante para la producción industrial de aluminio. También está presente en grandes cantidades en los tanques de desechos radiactivos de alto nivel en los sitios del Departamento de Energía de EE. UU. En el estado de Washington y Carolina del Sur. El procesamiento tradicional para la producción de aluminio o el tratamiento de desechos radiactivos es una actividad que consume mucha energía. El procesamiento implica calentar para facilitar la disolución de la gibbsita en soluciones altamente alcalinas de electrolitos concentrados. Al calentamiento le sigue el enfriamiento para estimular la precipitación de estos sistemas químicamente extremos.
Para el tratamiento de residuos radiactivos, las etapas de disolución y precipitación suelen ser bastante lentas. ¿Por qué? En parte, ambos procesos implican cambios en la geometría de coordinación del aluminio trivalente. En la fase sólida, tiene seis coordenadas para dar una geometría octaédrica. Para pasar a la fase de solución, el ion aluminio debe cambiar su geometría a una forma tetraédrica de cuatro coordenadas.
Dirigido por Jian Zhi Hu y Kevin Rosso, El equipo llevó a cabo estudios de espectroscopía de resonancia magnética nuclear giratoria de ángulo mágico de campo alto que sondearon las interacciones de los iones. organización de solutos, y propiedades de los disolventes durante la precipitación de gibbsitas. El equipo capturó la dinámica del sistema en tiempo real en función de las condiciones experimentales, revelando detalles mecanicistas previamente desconocidos.
El trabajo del equipo muestra que el cambio en la coordinación no es una simple transición entre las especies tetraédricas a octaédricas. El cambio implica un centro de metal de aluminio pentacoordinado intermedio. Más lejos, estas especies están influenciadas por cambios sutiles en la organización de los solutos y disolventes. Estos cambios conducen a redes de gel que a veces pueden facilitar la formación o disolución de la fase sólida. Comprender cómo cambia la coordinación del aluminio en entornos extremos puede conducir a eficiencias en la producción de aluminio y acelerar el procesamiento de desechos radiactivos.