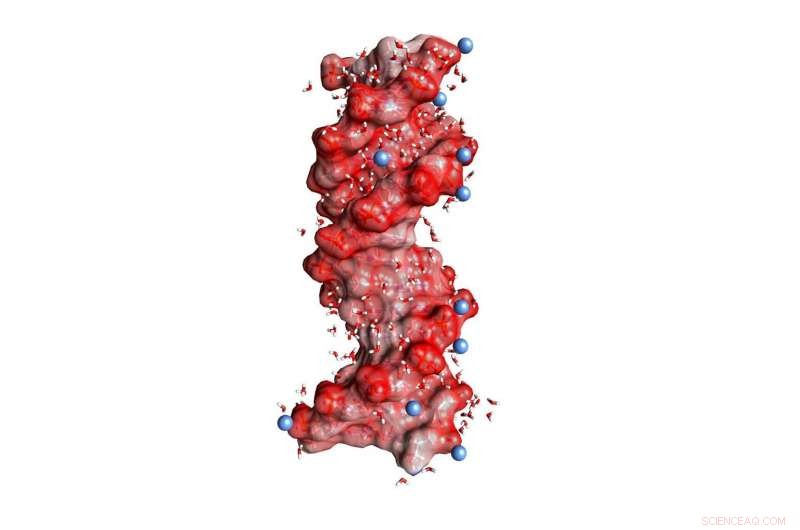
Fig.1:Doble hélice de ADN incrustada en agua (moléculas pequeñas en ángulo, no a escala). Las esferas de color rojo oscuro en la superficie de la hélice representan átomos de oxígeno de las unidades de PO2 cargadas negativamente, las esferas azules iones cargados positivamente en el medio ambiente. Crédito:MBI Berlín
Los pares de grupos fosfato cargados negativamente e iones de magnesio positivos representan una característica estructural clave del ADN y el ARN incrustados en agua. Las vibraciones de los grupos fosfato se han establecido ahora como sondas selectivas de tales pares de contactos y permiten un mapeo de interacciones y estructura en las escalas de tiempo ultrarrápidas de la dinámica molecular.
El ADN y el ARN son polímeros cargados que codifican información genética en una estructura de doble hélice y actúan como un actor clave en la biosíntesis de proteínas. Sus cargas negativas se encuentran en la columna vertebral molecular, que consiste en fosfato iónico (PO 2- ) y de grupos de azúcar (Figura 1). La estabilización de las estructuras macromoleculares de ADN y ARN requiere una compensación de fuertes fuerzas eléctricas repulsivas entre los grupos fosfato igualmente cargados por iones de opuestos, es decir., Carga positiva. En este contexto, magnesio (Mg 2+ ) Los iones son particularmente relevantes ya que no solo estabilizan la estructura, sino que también median en el reconocimiento de socios vinculantes externos y actúan como centros catalíticos. Es más, los cambios de estructura macromolecular a través de procesos de plegamiento dinámicos están conectados con una reordenación de iones positivos incrustados en la capa de agua circundante.
Los iones positivos se organizan en diferentes geometrías alrededor del ADN y el ARN:en las denominadas geometrías de enlace de sitio o de pares de contacto, un ion positivo se encuentra en contacto directo con un átomo de oxígeno de un grupo fosfato. A diferencia de, la llamada atmósfera de iones externos consta de iones positivos separados por al menos una capa de moléculas de agua de los grupos fosfato. El papel funcional de las diferentes geometrías y las interacciones subyacentes están lejos de entenderse. Una comprensión más profunda a nivel molecular requiere sondas altamente sensibles que permitan discernir las diferentes geometrías de iones sin perturbarlos. y para mapear su dinámica en la escala de tiempo ultrarrápida de los movimientos moleculares.

Fig. 2:Arriba:Estructura molecular de un par de iones de contacto que consta de dimetilfosfato (DMP) y un ión de magnesio Mg2 incrustado en agua. Las flechas marcan los alargamientos de los enlaces fósforo-oxígeno en la vibración asimétrica de estiramiento de PO2. Abajo:Espectros infrarrojos bidimensionales (2D-IR) de la vibración asimétrica de estiramiento de PO2 medidos en un tiempo de espera T =500 fs después de la excitación vibratoria. La respuesta vibracional se muestra en función de la excitación infrarroja y las frecuencias de detección y consiste en un componente P1 de moléculas DMP sin un ion magnesio en la vecindad y la contribución P2 de los pares de iones de contacto. Este último se desplaza a frecuencias más altas debido a la interacción entre PO2- y Mg2. Crédito:MBI Berlín
En una publicación reciente, Los investigadores del Instituto Max Born (MBI) demuestran que las vibraciones de los grupos fosfato representan sondas sensibles y no invasivas de geometrías iónicas en un entorno acuático. Dimetilfosfato (DMP, (CH 3 O) 2PO 2- ), un sistema modelo establecido para la columna vertebral de ADN y ARN, se preparó en agua líquida con un exceso de Mg 2+ iones (Figura 2, arriba) y estudiado por espectroscopía vibracional no lineal en el dominio del tiempo de femtosegundos (1 fs =10 -15 s). Los experimentos utilizan espectroscopía infrarroja bidimensional (2-D-IR), un método más sofisticado para analizar las interacciones y estructuras iónicas en la escala de tiempo intrínseca de los movimientos moleculares fluctuantes.
El mapa de experimentos Mg 2+ iones en contacto directo con un PO 2- grupo a través de una característica distinta en el espectro 2-D-IR (Figura 2, fondo). La interacción con el Mg 2+ iones desplaza el PO asimétrico 2- Estirar la vibración a una frecuencia más alta que en ausencia de Mg. 2+ iones. La forma lineal y la evolución temporal de esta nueva característica revelan fluctuaciones de la geometría del par de iones de contacto y la capa de agua de incrustación en una escala de tiempo de cientos de femtosegundos, mientras que el par de contacto en sí existe durante tiempos mucho más largos (~ 10 -6 s). Un análisis teórico en profundidad muestra que el sutil equilibrio de las fuerzas atractivas electrostáticas (Coulomb) y las fuerzas repulsivas debido a la interacción de intercambio cuántico-mecánico gobierna la posición de frecuencia de la vibración de fosfato.
La capacidad de la espectroscopia 2-D-IR para caracterizar la interacción de iones fosfato de corto alcance en solución proporciona una nueva herramienta analítica que complementa las técnicas estructurales actualmente disponibles. Una extensión de este nuevo enfoque para el ADN y el ARN y su entorno iónico es muy prometedora y se espera que proporcione una nueva visión de las fuerzas que estabilizan las estructuras de equilibrio y que impulsan los procesos de plegamiento.