Muchas enfermedades pueden tratarse con éxito en el entorno sencillo de una placa de cultivo celular, pero para tratar con éxito a personas reales, el fármaco tiene que emprender un viaje a través del entorno infinitamente más complejo de nuestro cuerpo y llegar, intacto, al interior de las células afectadas. Este proceso, llamado administración de fármacos, es una de las barreras más importantes en medicina.
Una colaboración entre el Laboratorio Nacional Lawrence Berkeley (Berkeley Lab) y Genentech, miembro del Grupo Roche, está trabajando para superar algunos de los obstáculos en la entrega de medicamentos mediante el diseño de las nanopartículas lipídicas (LNP, por sus siglas en inglés) más efectivas:pequeñas bolsas esféricas hechas de moléculas grasas. que encapsulan agentes terapéuticos hasta que se acoplan a las membranas celulares y liberan su contenido. El primer medicamento que utilizó LNP se aprobó en 2018, pero el método de administración saltó a la fama mundial con las vacunas COVID de ARNm de Pfizer y Moderna.
"Es un sistema bastante inteligente, porque si simplemente entregas el ARN al cuerpo humano, las nucleasas lo degradan y no puede cruzar fácilmente la membrana celular debido a su tamaño y carga, pero las LNP lo entregan de manera segura dentro de la célula. " explicó el coautor principal Chun-Wan Yen, científico principal senior del grupo de Ciencias Farmacéuticas de Moléculas Pequeñas de Genentech.
Actualmente se están explorando ampliamente las LNP como sistema de administración de vacunas para otras enfermedades infecciosas o vacunas terapéuticas contra el cáncer. La viabilidad de estas nuevas aplicaciones dependerá de qué tan bien se fusionen las envolturas lipídicas con las células diana, qué tan estables sean las formulaciones de fármaco-LNP en almacenamiento (para que tengan una vida útil prolongada) y qué tan estables sean en el cuerpo. (por lo que pueden conferir una actividad farmacológica prolongada).
Todas estas propiedades están controladas por la mezcla de moléculas utilizadas para crear el LNP y la estructura 3D resultante de la partícula. El equipo dirigido por Yen y sus codirectores Greg Hura y Michal Hammel, ambos biofísicos del Laboratorio de Berkeley, ha estado estudiando cómo ajustar la estructura de las LNP para las propiedades deseadas durante varios años.
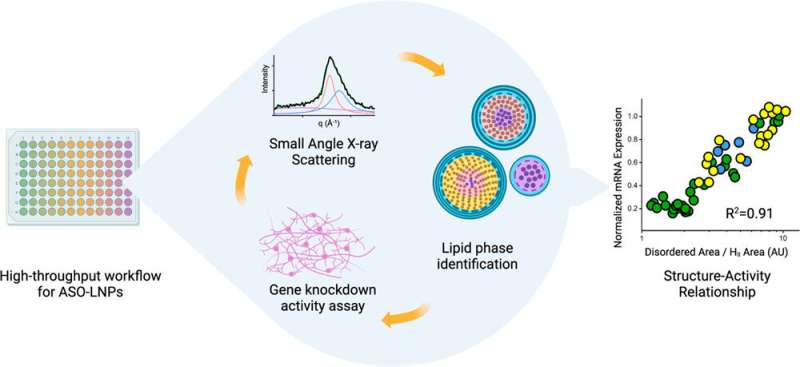
Su último artículo, publicado recientemente en ACS Nano , documenta cómo un flujo de trabajo de alto rendimiento les permite producir y caracterizar LNP a una velocidad récord. El estudio también incluye la primera demostración de cómo la estructura de LNP se correlaciona con la actividad de su contenido, que para esta investigación era un oligonucleótido antisentido (ASO). Los ASO son pequeños fragmentos de pares de bases de ARN o ADN que bloquean la expresión genética uniéndose a hebras de ARNm e impidiendo que se traduzcan en proteínas. Los ASO son una excelente manera de tratar enfermedades causadas por proteínas defectuosas o por un exceso de proteína. Pero, al igual que el ARNm, son susceptibles a las nucleasas itinerantes (enzimas que degradan el ARN y el ADN) y las células no las absorben fácilmente.
Los científicos descubrieron que las LNP que transportaban ASO con estructuras internas cuidadosamente ordenadas y estrechamente empaquetadas conducían a un mejor silenciamiento de un gen defectuoso en las neuronas humanas que está asociado con una enfermedad degenerativa, en comparación con las LNP que tenían una estructura más desordenada. Los hallazgos provienen de actividades celulares, no de estudios en animales, por lo que aún queda trabajo por delante, pero el equipo está entusiasmado de aprovechar estos conocimientos utilizando las herramientas complementarias de cada institución.

"Generamos los LNP en alto rendimiento y el equipo de Greg y Michal puede ofrecer el análisis de alto rendimiento", dijo Yen. "Si miras la publicación hoy en día, normalmente solo hacen una o dos formulaciones, pero para nosotros es diferente. Podemos generar grandes conjuntos de datos, y creo que esa es la razón por la que podemos tener este hallazgo tan único y genial".
"Este artículo realmente establece el método que vamos a aplicar a las miles de otras formulaciones que pretendemos caracterizar", añadió Hura, que forma parte del Área de Biociencias del Laboratorio de Berkeley. "Esperamos que este sea un método general para que las personas optimicen sus nanopartículas lipídicas. Ya sean vacunas, una y otra vez, las vacunas han recibido la mayor atención hasta ahora o más allá. Este tipo de terapia tiene una aplicación muy amplia más allá de eso. ."
Las estructuras de los LNP se ven afectadas por cómo se mezclan, qué se mezclan y en qué orden. Los LNP tienen cuatro ingredientes:lípidos ionizables, fosfolípidos auxiliares, colesterol y lípidos de polietilenglicol (lípidos PEG), y cada ingrediente tiene diferentes formas. Además, se pueden combinar en diferentes proporciones, lo que da lugar a un número exponencial de fórmulas posibles. Para complicar aún más las cosas, los LNP cambian con el tiempo. Una formulación que comienza como una esfera ordenada y compacta eventualmente se transformará en una estructura más desordenada.
Los científicos de Genentech desarrollaron un flujo de trabajo impulsado por robots que puede generar cientos de formulaciones de LNP en tan solo unas horas. Luego se llevan muestras de cada formulación al Laboratorio de Berkeley para realizar dispersión de rayos X de ángulo pequeño (SAXS) en Advanced Light Source, un acelerador de partículas circular que crea haces de rayos X de diferentes energías.
La línea de luz biológica SAXS puede procesar rápidamente muchas muestras y, a diferencia de otras formas de difracción de rayos X en materiales biológicos, las muestras no necesitan congelarse ni cristalizarse, lo que podría cambiar la estructura de las LNP e impedir que los científicos descubran cuál es el problema. Los LNP se verían a temperaturas fisiológicas en el cuerpo humano. SAXS también les permite tomar instantáneas de los LNP en momentos específicos para determinar su longevidad estructural.
Además, el equipo de Genentech utiliza un proceso acelerado para estudiar cómo las LNP afectan la expresión genética en sus células diana. Al combinar todas estas técnicas aceleradas, toda la colaboración puede detectar LNP potenciales a un ritmo sin precedentes.
Yen planea continuar usando la línea de luz SAXS para estudiar pequeños detalles, como cómo un cambio del 1% en la concentración de ingredientes o el uso de una nueva máquina durante la producción puede afectar la actividad celular de LNP, así como grandes preguntas, como si los LNP se comportan de manera diferente si son transportar otros tipos de carga y cómo interactúan con diferentes células objetivo.
"Sabemos que los LNP de ARNm funcionan, pero todavía existe una enorme brecha de conocimiento", dijo Yen. "Por eso creo que nuestro artículo es pionero en este campo y espero que también podamos generar más datos y conocimientos para futuras aplicaciones".
Más información: Michal Hammel et al, Correlación de la estructura y la actividad de silenciamiento genético de nanopartículas lipídicas cargadas con oligonucleótidos mediante dispersión de rayos X de ángulo pequeño, ACS Nano (2023). DOI:10.1021/acsnano.3c01186
Información de la revista: ACS Nano
Proporcionado por el Laboratorio Nacional Lawrence Berkeley