Un equipo de investigadores del Centro Oncológico MD Anderson de la Universidad de Texas ha desarrollado un nuevo método para utilizar vesículas extracelulares para mejorar las respuestas a la inmunoterapia en el glioblastoma, lo que podría abrir la puerta a un uso más amplio del ARN mensajero (ARNm) diseñado para la terapia del cáncer. El estudio fue publicado hoy en Nature Communications.
A principios de este año, un equipo de investigadores dirigido por Betty Kim, M.D., Ph.D., y Wen Jiang, M.D., Ph.D., desarrolló un método novedoso para cargar ARNm en vesículas extracelulares, pequeñas estructuras creadas por las células para transportar biomoléculas. y ácidos nucleicos dentro del cuerpo. El estudio actual se basa en esa investigación al demostrar el potencial antitumoral de las vesículas extracelulares cargadas de ARNm.
Las terapias con ARNm, que fueron reconocidas con el Premio Nobel de Fisiología o Medicina de 2023, han tenido durante mucho tiempo un potencial revolucionario en infecciones patógenas y enfermedades como el cáncer. Sin embargo, persisten desafíos para administrar con precisión el ARNm en todo el cuerpo. Durante años, los científicos han estudiado posibles mecanismos de administración, incluidas las nanopartículas lipídicas o poliméricas, pero cada uno de ellos tiene sus propias limitaciones.
"Existen dos desafíos principales en el uso de terapias de ARNm para el tratamiento del cáncer. Primero, ¿cómo apuntar con precisión a las células tumorales en el cuerpo? Segundo, ¿cómo se produce suficiente terapia para uso humano?" Dijo Jiang. "Nuestro enfoque resuelve esos dos problemas."
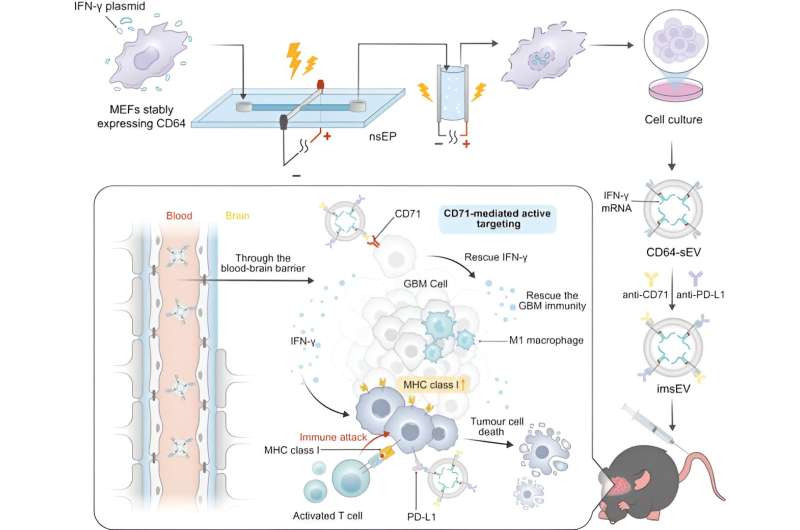
El problema de la cantidad se resuelve mediante el uso de un sistema de alto rendimiento para producir vesículas extracelulares cargadas de ARNm a partir de células diseñadas. Las células huésped y un plásmido de diseño que codifica el ARNm se someten a dos pulsos eléctricos extremadamente cortos, lo que hace que las membranas del interior de la célula, así como la propia membrana celular, se vuelvan temporalmente permeables. Esto lleva a las células a secretar muchas vesículas extracelulares cargadas con material de ARNm que luego puede recolectarse.
Para este estudio, los investigadores diseñaron las vesículas extracelulares para expresar la proteína CD64 en su superficie, que sirve como mecanismo de acoplamiento para cargar anticuerpos anti-CD71 y anti-PD-L1. Una vez en el cuerpo, buscan CD71 y PD-L1, los cuales comúnmente se sobreexpresan en los glioblastomas.
Estas vesículas extracelulares estaban cargadas con ARNm que codifica interferón gamma, una proteína de señalización inmunitaria. Cuando las vesículas se unen a los receptores de las células tumorales, se internalizan y liberan el ARNm.
Una de las razones por las que el glioblastoma es difícil de tratar es que la regulación negativa del MHC-1, así como otras características del microambiente tumoral, crean un entorno inmunosupresor que evade la detección y limita la eficacia de las inmunoterapias. El ARNm revierte esto, cambiando el microambiente del tumor para hacer que el tumor sea detectable por el sistema inmunológico y responda mejor a las inmunoterapias. En los modelos preclínicos, se observó un aumento significativo en el tiempo de supervivencia y la actividad antitumoral inicial dentro de los 7 días posteriores a la inyección.
"Elegimos el glioblastoma porque actualmente tiene opciones de tratamiento limitadas", dijo Jiang. "Sabemos que el interferón gamma puede inducir respuestas a la inmunoterapia en el glioblastoma, pero hasta ahora su administración a las células tumorales ha demostrado ser un desafío importante debido a su vida media y a la incapacidad de la mayoría de los sistemas de administración para cruzar el torrente sanguíneo-cerebro. Se espera que estos resultados allanen el camino para que las vesículas extracelulares cargadas con ARNm se utilicen en aplicaciones contra el cáncer".
Según Jiang, una de las otras ventajas de este enfoque es que es plug-and-play, lo que significa que se puede adaptar a otros tumores simplemente cambiando los anticuerpos para que se dirijan a los que se sobreexpresan en otros tipos de tumores.
Se están realizando más trabajos preclínicos para seguir mejorando los métodos de producción y perfilar la seguridad de las vesículas extracelulares antes de que se apliquen en entornos clínicos.
Más información: Shiyan Dong et al, Diseño adaptativo de vesículas extracelulares cargadas con ARNm para inmunoterapia dirigida del cáncer, Nature Communications (2023). DOI:10.1038/s41467-023-42365-5
Información de la revista: Comunicaciones sobre la naturaleza
Proporcionado por el Centro Oncológico M. D. Anderson de la Universidad de Texas