Los científicos de Northwestern Medicine han desarrollado una forma más eficaz de crear vacunas y medicamentos nanoterapéuticos, según un nuevo estudio publicado en ACS Nano .
"Durante la última década, la tecnología del ácido nucleico esférico, o SNA, ha surgido como una amplia plataforma terapéutica para una amplia variedad de enfermedades, incluido el cáncer y otras enfermedades", dijo Chad Mirkin, Ph.D., profesor de Medicina en la División de Hematología y Oncología, profesor de Química George B. Rathmann en la Facultad de Artes y Ciencias Weinberg de Northwestern y director del Instituto Internacional de Nanotecnología, autor principal del estudio.
En el laboratorio de Mirkin, los investigadores han aprovechado esta tecnología SNA en su trabajo para diseñar nanomedicamentos de precisión para su uso en la regulación genética y en la inmunoterapia contra el cáncer con efectos secundarios limitados no deseados a través de un proceso de desarrollo sistemático conocido como vacunología racional.
"En el desarrollo de vacunas, históricamente se ha prestado muy poca atención a la estructura de la vacuna", dijo Mirkin, quien también es miembro del Centro Integral de Cáncer Robert H. Lurie de la Universidad Northwestern. "Todo el énfasis se ha puesto en los componentes. La premisa de la vacunología racional es que, si bien los componentes son críticos, la estructura es igualmente importante. La forma en que se presentan los componentes de la vacuna dentro de una arquitectura modular a nanoescala puede tener un impacto dramático en la eficacia de la vacuna, ya sea tratar enfermedades infecciosas o cáncer."
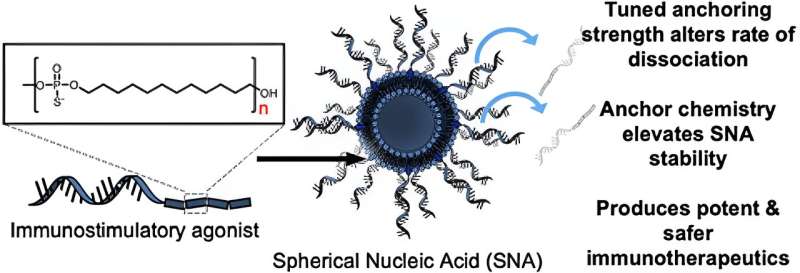
En el estudio, los investigadores primero probaron los efectos del uso de diferentes grupos de anclaje químico para unir los oligonucleótidos (hebras cortas de ADN o ARN) a la superficie de los liposomas para preparar SNA. Descubrieron que cuando se utilizaban grupos de anclaje cada vez más hidrófobos a base de dodecano, la estabilidad de la nanoestructura mejoraba significativamente. Cuando se introdujeron en células dendríticas derivadas de la médula ósea de ratones, estas construcciones de SNA más estables mostraron una absorción celular mejorada en comparación con las otras versiones de SNA que se prepararon utilizando otros tipos de grupos de anclaje, con diferentes químicas.
"Descubrimos una forma de anclar los oligonucleótidos a la superficie de la partícula que cambia la estabilidad general de la construcción SNA, lo cual es fundamental", dijo Jasper Dittmar, Ph.D. estudiante en el laboratorio Mirkin y coautor del estudio. "La belleza de la arquitectura SNA es que es reconocida por casi todos los tipos de células, incluidas las células inmunes, y se internaliza rápidamente. La vacuna ingresa a las células importantes con la estequiometría deseada, con la cantidad deseada de antígenos y moléculas adyuvantes."
Luego, los científicos del laboratorio de Mirkin cargaron la vacuna SNA con OVA1 (un péptido modelo derivado de la proteína del huevo que se utiliza a menudo en el desarrollo de vacunas) y la administraron a ratones con linfoma. Los ratones tratados con OVA1 SNA no sólo tenían una mayor cantidad de células T polifuncionales (que se consideran potentes contra infecciones crónicas y tumores), sino que también mostraron una reducción de 21 veces en los volúmenes tumorales en comparación con los ratones tratados con solución salina, según el estudio.
Para evaluar los efectos secundarios inflamatorios de la vacuna, los investigadores estudiaron el SNA para ver si activaba respuestas inmunes excesivas en ratones. Los ratones que recibieron el tratamiento no produjeron una tormenta de citocinas, un efecto secundario a veces mortal de las inmunoterapias.
Debido a que las tormentas de citocinas están asociadas con casos graves de COVID-19, Mirkin y su equipo de investigación también crearon una vacuna SNA en la que el péptido OVA1 se intercambió por un péptido del virus que causa el COVID-19 (péptido CoV) y se lo administró a humanos. células y finalmente ratones. Los investigadores descubrieron que la vacuna mejoraba las respuestas inmunitarias anti-COVID específicas de antígeno con efectos secundarios adversos mínimos.
"En conjunto, los resultados de este estudio sientan las bases para una nueva forma de desarrollar y administrar vacunas y otros tratamientos de precisión, independientemente de la enfermedad objetivo", afirmó Michael Evangelopoulos, Ph.D. estudiante en el laboratorio Mirkin y coautor del estudio.
Los hallazgos también resaltan la importancia de la construcción de vacunas, afirmó Mirkin.
"La estructura importa", dijo Mirkin. "En un campo en el que hemos dedicado muy poco tiempo a centrarnos en la estructura de las vacunas, es posible que nos hayamos perdido el bosque por los árboles. Es una comprensión combinada de los componentes y la presentación estructural lo que conduce a un medicamento eficaz o no. ."
En el futuro, el grupo Mirkin seguirá ideando diferentes configuraciones de vacunas SNA para evaluar cuáles son las más efectivas, afirmó.
"Estamos dedicando mucho tiempo a utilizar la plataforma SNA para descubrir las estructuras que son más eficaces, y luego tratando de descubrir por qué, qué funciona y también por qué funciona", dijo Mirkin. "Creemos que, al hacerlo, podremos crear toda una nueva generación de medicamentos basados en este concepto de vacunología racional".
Más información: Jasper W. Dittmar et al, Ajuste de la disociación del ADN a partir de ácidos nucleicos esféricos para una inmunoestimulación mejorada, ACS Nano (2023). DOI:10.1021/acsnano.3c04333
Información de la revista: ACS Nano
Proporcionado por la Universidad Northwestern