Los polímeros autoplegables que contienen gadolinio y que forman complejos nanométricos podrían ser la clave para mejorar las imágenes por resonancia magnética y la administración de fármacos de próxima generación, como lo demostraron los científicos del Tokyo Tech. Gracias a su pequeño tamaño, baja toxicidad y buena acumulación y penetración tumoral, estos complejos suponen un gran avance respecto a los agentes de contraste para el diagnóstico del cáncer, así como a la radioterapia de captura de neutrones.
La resonancia magnética (MRI) es una herramienta de diagnóstico crucial para el cáncer, ya que permite capturar imágenes detalladas de los tejidos blandos. Para visualizar los tumores más claramente en las resonancias magnéticas, los médicos suelen inyectar a los pacientes agentes de contraste. Estos compuestos afectan la forma en que los iones de hidrógeno cercanos responden a los pulsos de radiofrecuencia utilizados en la resonancia magnética. Idealmente, los agentes de contraste deberían acumularse selectivamente en los tumores y aumentar su contraste en la resonancia magnética.
Sin embargo, a pesar de muchos esfuerzos de investigación, los agentes de contraste convencionales quelatos de gadolinio (Gd) están alcanzando sus límites de rendimiento. En pocas palabras, lograr una dosis óptima en la distribución de quelatos de Gd dentro de los tumores, el tejido sano y la sangre ha demostrado ser un desafío sin recurrir a dosis excesivas de Gd.
En este contexto, un estudio colaborativo realizado por un equipo de investigación del Instituto de Tecnología de Tokio (Tokyo Tech), los Institutos Nacionales de Ciencia y Tecnología Cuánticas (QST) y el Centro de Innovación de Nanomedicina (iCONM), dirigido por el profesor asociado Yutaka Miura de Tokyo Tech, desarrolló con éxito un nuevo agente de nanocontraste (NCA) con un rendimiento excepcional gracias a un diseño molecular innovador. Sus hallazgos fueron publicados en la Advanced Science. el 29 de noviembre.
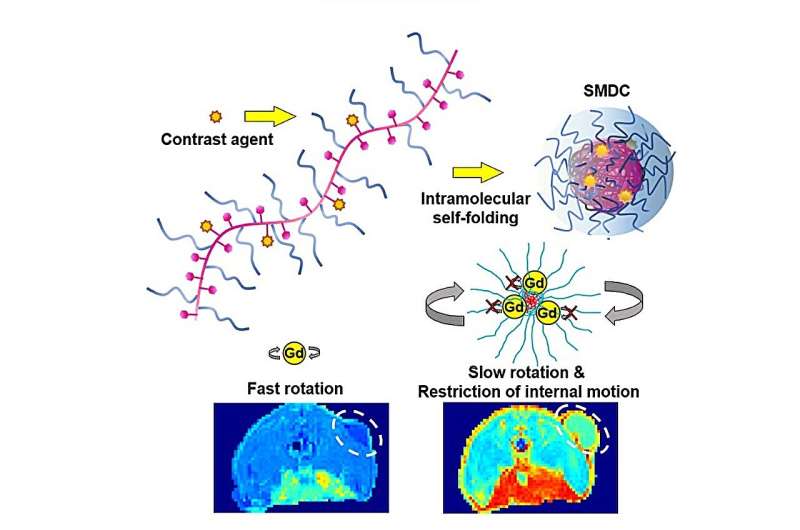
La NCA propuesta se basa en el uso de Gd como agente de contraste en lo que los investigadores llamaron un "portador de fármacos macromolecular autoplegable (SMDC)". Incorporaron quelatos que contienen Gd clínicamente aprobados en una cadena polimérica compuesta de acrilato de éter metílico de polietilenglicol (PEGA) y acrilato de bencilo (BZA). Dado que el polímero contenía segmentos hidrofílicos e hidrofóbicos, rápidamente se plegó en forma de pequeña cápsula cuando se sumergía en agua, con los segmentos hidrofóbicos en el núcleo y los segmentos hidrofílicos en la capa exterior.
Utilizando este enfoque, los investigadores pudieron producir moléculas SMDC-Gds de menos de 10 nanómetros de diámetro. Mediante experimentos en ratones con cáncer de colon, comprobaron que estos NCA no sólo se acumulaban mejor en los tumores, sino que también se eliminaban rápidamente del torrente sanguíneo, lo que permitía mejorar el rendimiento de la resonancia magnética sin efectos tóxicos.
"La alta acumulación en el tumor y el rápido perfil de eliminación sanguínea de SMDC-Gds permiten aumentar la proporción de acumulación de tumor en órganos principales, además de minimizar la deposición innecesaria de Gds", explica el profesor Miura.
El equipo también demostró un efecto novedoso que sitúa a los SMDC-Gds por delante de los quelatos de Gd existentes. Idealmente, el movimiento de los iones de Gd debería ser mínimo para que su influencia sobre los iones de hidrógeno cercanos sea constante y prolongada. En el diseño molecular propuesto, la estructura núcleo/capa crea un entorno molecular "saturado" que suprime no sólo la rotación, sino también los movimientos segmentarios e internos de los iones de Gd.
El efecto resultante es un contraste más fuerte en las imágenes de resonancia magnética, lo que permitirá el uso de elementos alternativos con perfiles más seguros no sólo en los pacientes sino también en el medio ambiente en el futuro.
Vale la pena destacar que las aplicaciones de SMDC-Gds se extienden más allá de la resonancia magnética. Estos compuestos se pueden utilizar en la terapia de captura de neutrones (NCT), una prometedora técnica de radioterapia dirigida en la que los Gds capturan neutrones y liberan radiación de alta energía, matando las células cancerosas cercanas.
Los experimentos en ratones revelaron que la NCT después de repetidas inyecciones de SMDC-Gd conducía a una gran supresión del crecimiento tumoral. El equipo cree que la razón de esto fue la acumulación selectiva y la profunda penetración de SMDC-Gds en los tejidos tumorales.
En conjunto, los esfuerzos colaborativos de los investigadores para lograr estos hallazgos subrayan el potencial de los SMDC no solo para mejorar el diagnóstico por resonancia magnética, sino también como herramientas efectivas para tratar el cáncer y otras enfermedades.
"Este estudio presenta nuevas posibilidades para explotar la administración de fármacos utilizando diversas cargas terapéuticas, y actualmente estamos investigando el desarrollo de tales sistemas SMDC", concluye el profesor Miura.
Más información: Shan Gao et al, Portador de fármacos macromoleculares autoplegable para imágenes y terapia del cáncer, Ciencia avanzada (2023). DOI:10.1002/adv.202304171
Información de la revista: Ciencia avanzada
Proporcionado por el Instituto de Tecnología de Tokio