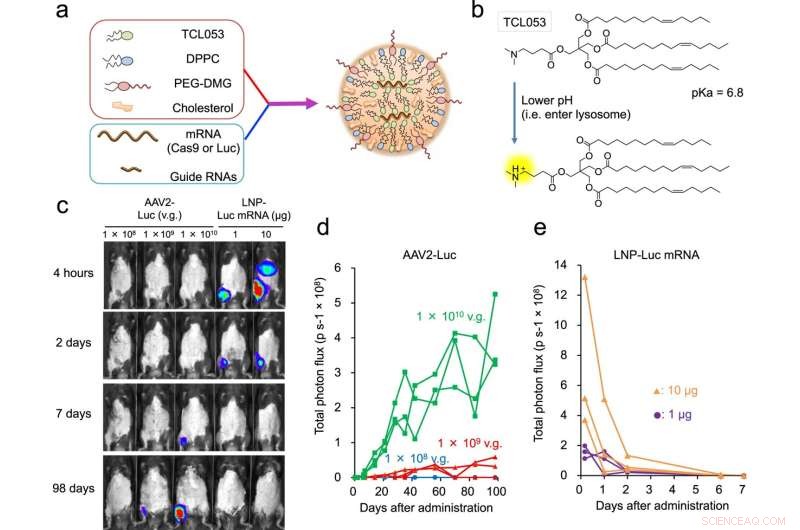
Fig. 1:Entrega de Luc-mRNA o CRISPR-Cas9 mRNA/sgRNA mediada por LNP en el tejido muscular. una ilustración esquemática de LNP-CRISPR. El ARNm de Luc o el ARNm/sgRNA de Cas9 se encapsula en LNP que consta de TCL053, DPPC (dipalmitoilfosfatidilcolina), PEG-DMG (polietilenglicol-dimiristoilglicerol) y colesterol. b Estructura química del lípido ionizable recién sintetizado, TCL053. c Imágenes de bioluminiscencia representativas de ratones C57BL/6J después de la inyección intramuscular de AAV2-Luc (1 × 108, 1 × 109 o 1 × 1010 v.g., genomas vectoriales) o ARNm de LNP-Luc (1 o 10 μg de ARNm). d, e Cuantificación de la señal de bioluminiscencia en músculo esquelético de ratones C57BL/6J tratados con ARNm de AAV2-Luc (d) o LNP-Luc (e). Los mismos ratones (n = 3 ratones por grupo) se examinaron repetidamente a lo largo del tiempo. Los datos de flujo total (p s−1, fotones por segundo) se trazan como una sola línea por ratón. Crédito:DOI:10.1038/s41467-021-26714-w
Muchas enfermedades intratables son el resultado de una mutación genética. La tecnología de edición del genoma promete corregir la mutación y, por lo tanto, nuevos tratamientos para los pacientes. Sin embargo, llevar la tecnología a las células que necesitan la corrección sigue siendo un gran desafío. Un nuevo estudio dirigido por el Profesor Asociado Junior de CiRA, Akitsu Hotta, y en colaboración con Takeda Pharmaceutical Company Limited como parte del Programa de Investigación Conjunta T-CiRA, informa cómo las nanopartículas de lípidos proporcionan un medio eficaz para el tratamiento de la distrofia muscular de Duchenne (DMD) en ratones. .
El Premio Nobel de Química del año pasado a los descubridores de CRISPR-Cas9 consolidó el impacto de la tecnología de edición del genoma. Si bien CRISPR-Cas9 se puede aplicar a la agricultura y la ganadería para obtener alimentos más nutritivos y cultivos robustos, la mayor parte de la atención de los medios se centra en su potencial médico. La DMD es solo una de las muchas enfermedades para las que los investigadores prevén un tratamiento con CRISPR-Cas9.
"Los medicamentos con oligonucleótidos ahora están disponibles para la DMD, pero sus efectos son transitorios, por lo que el paciente debe someterse a tratamientos semanales. Por otro lado, los efectos de CRISPR-Cas9 son duraderos", dijo Hotta.
La DMD produce atrofia muscular progresiva en todo el cuerpo. Los pacientes normalmente comienzan a mostrar síntomas, como caídas fáciles e incapacidad para correr antes de la edad escolar, y a menudo usan respiradores antes de la edad adulta.
Para una enfermedad como la DMD, es necesario apuntar a una amplia gama de músculos esqueléticos, lo que significa que las inyecciones múltiples son importantes. Los sistemas de administración actualmente investigados utilizan virus no patógenos para administrar CRISPR-Cas9, pero estos virus inducen reacciones inmunitarias y la producción de anticuerpos, lo que prohíbe las inyecciones múltiples.
Las nanopartículas de lípidos pueden prevenir estas reacciones. Como su nombre indica, las nanopartículas lipídicas son partículas diminutas de menos de 0,1 µm de diámetro y compuestas de lípidos que cambian sus propiedades en respuesta a la acidez. Esta característica les permite permanecer intactos fuera de la célula, pero una vez dentro se rompen para liberar su contenido, como CRISPR-Cas9, que luego queda libre para corregir la mutación del gen. Las nanopartículas de lípidos se están utilizando para las vacunas COVID-19, pero su utilidad para la terapia de edición del genoma aún está bajo investigación. Como parte del Programa de Investigación Conjunta T-CiRA, Hotta ha estado desarrollando nanopartículas lipídicas que pueden brindar tecnología de edición del genoma a la célula.
Después de experimentar con varias formulaciones, el estudio informa sobre una nueva nanopartícula lipídica que encapsula CRISPR-Cas9 en el interior y se dirige a las células musculares en ratones.
A diferencia de los fármacos oligonucleótidos, cuyos efectos en ratones disminuyeron constantemente después del tratamiento y desaparecieron después de unos meses, el estudio muestra que la administración de CRISPR-Cas9 con la nueva nanopartícula lipídica mantuvo un efecto constante en el músculo que duró más de un año.
Además, los efectos fueron evidentes incluso al administrar las partículas con múltiples inyecciones intramusculares, mientras que la administración basada en virus no tuvo efecto después de la segunda inyección. Además, las nanopartículas de lípidos perfundidas por vía intravenosa en las extremidades tuvieron un beneficio terapéutico en múltiples tejidos musculares.
Además de la seguridad, anotó Hotta, "CRISPR-Cas9 desapareció del cuerpo en unos pocos días. Eso significa que el riesgo de una edición del genoma fuera del objetivo es mínimo, pero los efectos terapéuticos duran mucho tiempo". La edición de genes CRISPR/Cas9 aumenta la eficacia de la terapia contra el cáncer con ultrasonidos