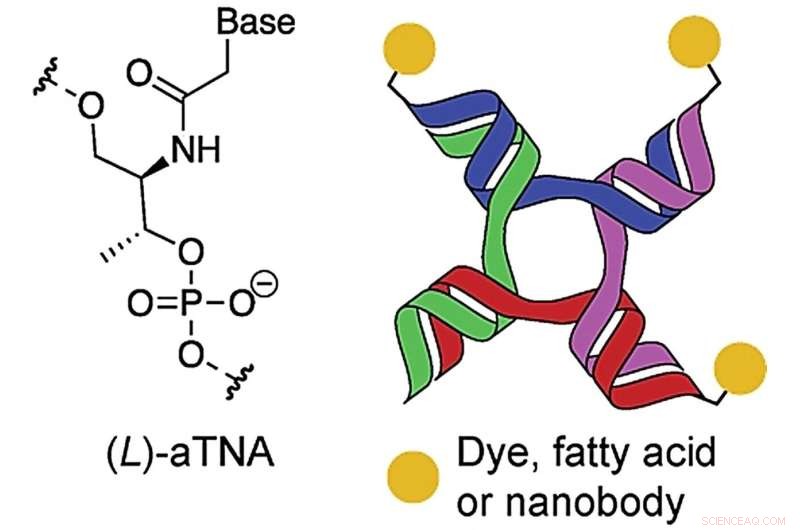
Investigadores de la Universidad de Aarhus han encontrado una manera de crear nanoestructuras más estables que pueden unirse y ensamblar biomoléculas con diferentes funciones, que en combinación, por ejemplo, pueden proporcionar una medicina contra el cáncer más efectiva. La ilustración es del artículo científico en Angewandte Chemie Int. Ed., que muestra esquemáticamente la nanoestructura utilizada con cadenas del bloque de construcción artificial, ácido nucleico de L-treoninol acíclico (aTNA). Crédito:Angew. Chem.Int. Edición
Durante milenios, el ADN ha jugado un papel central en el almacenamiento de la información genética de cada célula y consta de hebras con una secuencia específica de cuatro bloques de construcción diferentes. Estas hebras de ADN son copiadas por la célula en cada división celular de una manera extremadamente bien orquestada, pero sorprendentemente, esta maquinaria sofisticada se rige por reglas muy simples.
En los últimos años, se ha descubierto que estas reglas simples se utilizan no solo en el contexto de la ingeniería genética, sino también para construir nanoestructuras de ADN útiles mediante el diseño de hebras de ADN. Se ha demostrado que estas nanoestructuras de ADN tienen una serie de funciones biomédicas útiles, como la capacidad de transportar medicamentos contra el cáncer a los lugares exactos del cuerpo donde se necesitan. Esto puede aumentar el efecto del medicamento y proporcionar menos efectos secundarios en comparación con el tratamiento convencional contra el cáncer.
Las nanoestructuras de ADN también se utilizan cada vez más como herramienta para unir y ensamblar biomoléculas en estructuras multifuncionales. Una de estas nanoestructuras de ADN utilizadas forma una estructura ramificada con cuatro extremos, denominada uniones de 4 vías (4WJ), que también se encuentran de forma natural.
Con versiones especialmente diseñadas de estas estructuras 4WJ, por ejemplo, la Facultad de Medicina de Harvard en Boston logró unir y recolectar varios anticuerpos, que en combinación aseguraron que las células T atacaran a las células cancerosas agresivas con mayor intensidad y, por lo tanto, mataran los tumores.
Nanoestructuras de ADN mejoradas con bloques de construcción artificiales
Los investigadores que forman parte del Centro para el Diseño de Fármacos Biomoleculares Multifuncionales (CEMBID) de la Universidad de Aarhus también están trabajando para encontrar nuevas formas de vincular diferentes fármacos para lograr mecanismos de acción cada vez más efectivos. El grupo de investigación, dirigido por el profesor Kurt Gothelf, acaba de publicar un artículo en la revista Angewandte Chemie Int. Edición con resultados que involucran las estructuras 4WJ mencionadas anteriormente, pero en una versión mejorada. El trabajo fue realizado en colaboración con los grupos de Jørgen Kjems y Ken Howard quienes también forman parte del CEMBID.
Es cierto que estas nanoestructuras de ADN (4WJ) son inteligentes, pero existe la desventaja de las estructuras de ADN de que el ADN es de facto un polímero biodegradable. Esto significa que las estructuras se descomponen en la sangre más rápido de lo deseado. Además, las estructuras pueden ser tan grandes que ellas mismas activan el sistema inmunológico. Para que las estructuras se utilicen para diagnóstico o en medicina, es crucial que las estructuras sean muy estables, no tóxicas y que no desencadenen por sí mismas una reacción inmunitaria en el paciente.
Anders Märcher, un postdoctorado en el grupo de investigación de Kurt Gothelf y parte de CEMBID, junto con sus colegas de investigación, ahora ha encontrado una manera de aumentar la estabilidad de estas nanoestructuras. Lo han logrado mediante el uso de pequeñas cadenas, llamadas oligonucleótidos, de bloques de construcción artificiales y modificados para formar la nanoestructura. Los oligonucleótidos artificiales, Märcher et al. El uso se llama ácido nucleico de L-treoninol acíclico (aTNA) y funciona de la misma manera y tan bien como los componentes básicos naturales del ADN. Aquí, la molécula de azúcar (desoxirribosa) en los componentes básicos naturales se reemplaza con una molécula de azúcar artificial (L-treoninol acíclico), que fortalece la estructura general.
Los resultados positivos mostraron que las estructuras 4WJ con el bloque de construcción artificial, aTNA, son muy estables, no se degradan en la sangre, se ha demostrado que no son tóxicas para las células y no provocan una respuesta inmunitaria no específica. Cuando los investigadores acoplaron un tipo particular de biomolécula, que se sabe que se une a un biomarcador en células de cáncer de mama de alta especificidad, a la nueva estructura 4WJ, resultó que la estructura 4WJ puede resultar eficaz para dirigir los medicamentos contra el cáncer a las células deseadas. . Además, al realizar más modificaciones a la nueva estructura 4WJ, podrían extender su vida útil en el torrente sanguíneo y, por lo tanto, también el efecto del fármaco que puede acoplarse a la nanoestructura de ADN.
Los investigadores imaginan que su estructura 4WJ construida con bloques de construcción artificiales puede usarse como una herramienta para transportar medicamentos a la posición correcta en el cuerpo de un paciente. Además, ven que puede servir como una herramienta valiosa en la investigación. Por ejemplo, los investigadores imaginan que los efectos de diferentes combinaciones de biomoléculas que degradan el cáncer se pueden detectar de forma más rápida y eficiente, de modo que se pueda encontrar más rápidamente el tratamiento contra el cáncer más eficaz. La hélice de la vida:un nuevo estudio muestra cómo el ARN se une de forma estable a los ácidos nucleicos artificiales