Gráficamente abstracto. Crédito:DOI:10.1016 / j.colsurfb.2021.111931
Los científicos rusos han descubierto que el recubrimiento de nanopartículas magnéticas con una capa de sílice no magnética disminuyó significativamente la viabilidad de las células cancerosas en un campo magnético alterno de baja frecuencia. El recubrimiento aumenta la estabilidad de las nanopartículas, prevenir la agregación en los endosomas y mantenerlos como actuadores magneto-mecánicos efectivos en un campo magnético alterno de baja frecuencia. El estudio fue publicado en Coloides y superficies B:Biointerfaces.
Los nanomateriales magnéticos biocompatibles se han estudiado intensamente para diversas aplicaciones en biomedicina. Pueden controlarse de forma remota mediante un campo magnético externo, lo que permite afectar específicamente a las moléculas diana a nivel molecular.
La citotoxicidad de las nanopartículas magnéticas depende de los parámetros del campo magnético que actúan, los más importantes son la amplitud del campo magnético, frecuencia, y la duración de la acción. En un campo magnético alterno de baja frecuencia, ellos giran, causando daño mecánico a las células.
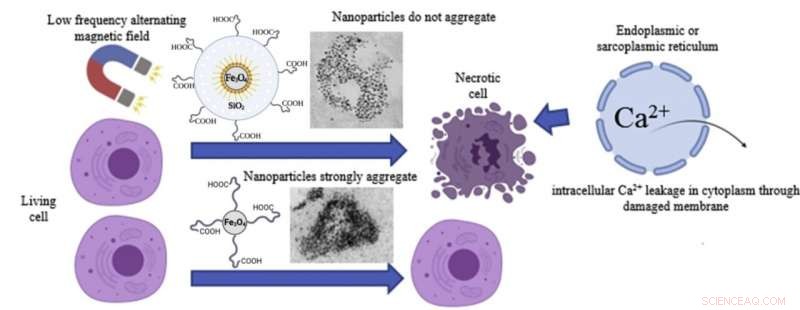
Científicos de NUST MISIS, M.V. Universidad Estatal Lomonosov de Moscú, V. Centro Nacional de Investigaciones Médicas de Psiquiatría y Narcología Serbsky, Universidad Estatal de Medicina de Siberia, Investigación Nacional de la Universidad Politécnica de Tomsk, Skoltech, D.I. La Universidad de Tecnología Química de Mendeleev de Rusia y la Universidad Médica de Investigación Nacional de Rusia N.I Pirogov han descubierto que una capa de cáscara no magnética aumenta significativamente la citotoxicidad de las nanopartículas magnéticas. Se sintetizaron dos tipos de nanopartículas de óxido de hierro con el mismo núcleo magnético con y sin caparazones de sílice. Las nanopartículas con caparazones de sílice disminuyeron significativamente la viabilidad de las células de cáncer de próstata humano en un campo magnético alterno de baja frecuencia según la prueba de citotoxicidad. a diferencia de las nanopartículas sin recubrimiento.
El estudio ha demostrado que la muerte celular es el resultado de una falla en la integridad de la membrana intracelular, y la concentración de iones calcio aumenta con la necrosis subsiguiente. La microscopía electrónica de transmisión y las imágenes de dispersión dinámica de la luz mostraron que las nanopartículas sin recubrimiento son grabadas por medios ácidos en el endosoma y forman agregados. Como resultado, encuentran una alta viscosidad macromolecular endosomal y se vuelven incapaces de rotar de manera eficiente.
Los científicos asumen que la rotación efectiva de nanopartículas causa la muerte celular en un campo magnético alterno de baja frecuencia. Sucesivamente, el revestimiento de la cáscara de sílice aumenta la estabilidad de las nanopartículas, Previniendo la agregación en endosomas.
"Nuestros fondos tienen valor tanto teórico como práctico. Descubrimos que la fase no magnética aumenta la estabilidad coloidal de las nanopartículas, siendo así la clave para su eficaz actuación magneto-mecánica. Esto es importante para la comprensión fundamental del mecanismo de actuación magneto-mecánica y cuáles deberían ser las características estructurales de las nanopartículas para maximizar su citotoxicidad. Por otra parte, hemos demostrado que nuestras nanopartículas funcionan, causan muerte celular. El siguiente paso sería probar su eficacia in vivo, "señaló Artyom Ilyasov, Laboratorio de Nanomateriales Biomédicos NUST MISIS.