La imagen es un montaje de la representación de un artista de un portador de un fármaco liposomal salpicado de porinas de nanotubos de carbono que se acopla a la superficie de una célula cancerosa y administra una carga de quimioterapia con una imagen de microscopía de fluorescencia de células teñidas expuestas a estos portadores. La mancha roja indica que las células están muertas y que el tratamiento fue exitoso. Crédito:P. Lastrico de MPI y N.T. Ho y A. Noy de LLNLL
La medicina moderna se basa en un extenso arsenal de medicamentos para combatir enfermedades mortales como la neumonía, tuberculosis, VIH-SIDA y malaria. Los agentes de quimioterapia han prolongado la vida de millones de pacientes con cáncer, y en algunos casos, curó la enfermedad o la convirtió en una condición crónica.
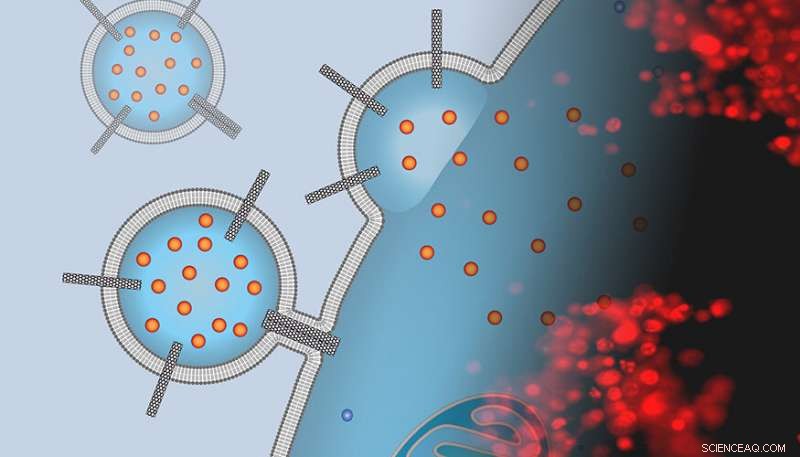
Pero hacer que esos medicamentos entren en células plagadas de enfermedades sigue siendo un desafío importante para la farmacología y la medicina modernas. Para hacer frente a esta dificultad, El Laboratorio Nacional Lawrence Livermore (LLNL) y la Universidad de California Merced, científicos y colaboradores del Instituto Max Planck de Biofísica en Alemania han utilizado nanotubos de carbono para permitir la administración directa de fármacos desde los liposomas a través de la membrana plasmática al interior de la célula facilitando la fusión de la membrana portadora. con el celular. La investigación aparece en el procedimientos de la Academia Nacional de Ciencias .
Los fármacos suelen ser poco solubles, muy tóxicos para otros tejidos o se enfrentan a una rápida degradación en los diferentes entornos químicos de un organismo. Pueden acumularse en tejidos no diana, se unen a otros componentes celulares o pueden no internalizarse eficientemente en las células diana.
Los sistemas de administración de liposomas tienen como objetivo mitigar estos problemas encapsulando fármacos en vehículos externos que circulan por el torrente sanguíneo. Sin embargo, estos sistemas implican un compromiso entre mejorar la estabilidad liposomal en el camino hacia el objetivo y facilitar la liberación de la carga útil en el citosol de la célula objetivo.
La mayoría de las estrategias actuales de administración de liposomas se basan en la vía endosómica para la entrada celular, que es inherentemente ineficaz y a menudo da como resultado la degradación del fármaco. Lípidos catiónicos de uso común, que mejoran la fusión liposomal con la membrana diana y mejoran el escape endosomal, resultó ser tóxico.
"Pensamos que las porinas de nanotubos de carbono (trozos cortos de nanotubos de carbono insertados en las membranas lipídicas) pueden imitar la funcionalidad del péptido de fusión viral y ayudar a fusionar los portadores liposomales a las membranas de las células cancerosas. "dijo el científico Alex Noy, quien dirigió la investigación en LLNL.
En una serie de experimentos, el equipo demostró que una plataforma de nanomateriales simple, un dímero de porinas de nanotubos de carbono de diámetro pequeño (CNTP), funciona como un potente promotor de la fusión de membranas. Es más, cuando Noy y su equipo cargaron sus liposomas con un potente agente quimioterapéutico (doxorrubicina), estos portadores entregaron el fármaco a las células cancerosas, matando a la mayoría de ellos.
"Nuestros resultados abren una vía para portadores de administración de medicamentos simples y eficientes compatibles con una amplia gama de terapias, "dijo Nga Ho, investigador postdoctoral del LLNL y coautor del artículo.
Simulaciones dinámicas moleculares de grano grueso, realizado por el equipo de Max Planck, reveló un mecanismo de fusión distinto e inusual donde los dímeros de CNTP unen las vesículas, acerque las membranas y luego fusione sus valvas externas e internas.
"Nos alegró mucho ver que la fusión de membranas facilitada por porinas de nanotubos de carbono de pequeño diámetro puede llevar a una mezcla completa del material de la membrana y el contenido interior de la vesícula". "dijo Marc Siggel, estudiante de posgrado en Max Planck, y co-primer autor del estudio.
"Nuestros experimentos demuestran que los liposomas con incrustaciones de CNTP pueden proporcionar la base para construir el tan deseado, pero hasta ahora escurridizo, portador versátil para la administración directa y altamente eficiente de medicamentos y vacunas de ADN y ARN a través de la membrana plasmática, "Dijo Noy.
"Esta estrategia podría evitar la vía endocitótica por completo y así evitar algunos de los problemas encontrados por las estrategias de administración anteriores". "añadió Gerhard Hummer, un biofísico teórico en el Instituto Max Planck, quien lideró el esfuerzo de modelado.