
Imagen de los implantes quirúrgicos, recubierto de nanopartículas de oro (pila de mallas a la izquierda) en comparación con las mallas quirúrgicas originales anteriores al tratamiento (pila de mallas a la derecha). Crédito:ICFO
Inventado hace aproximadamente 50 años, las mallas médicas quirúrgicas se han convertido en elementos clave en los procedimientos de recuperación de las cirugías de tejido dañado, la más frecuente es la reparación de hernias. Cuando se implanta dentro del tejido del paciente, El diseño flexible y adaptable de estas mallas ayuda a mantener los músculos tensos y permite que los pacientes se recuperen mucho más rápido que con la cirugía convencional de siembra y costura.
Sin embargo, la inserción de un implante médico en el cuerpo de un paciente conlleva el riesgo de contaminación bacteriana durante la cirugía y la posterior formación de una biopelícula infecciosa sobre la superficie de la malla quirúrgica. Tales biopelículas tienden a actuar como una capa impermeable, impidiendo que cualquier tipo de antibiótico alcance y ataque las bacterias formadas en la película para detener la infección. Por lo tanto, terapias con antibióticos, que son de tiempo limitado, podría fallar contra estas bacterias súper resistentes y el paciente podría terminar en cirugías recurrentes que incluso podrían conducir a la muerte. Como una cuestión de hecho, según la Red europea de vigilancia de la resistencia a los antimicrobianos (EARS-Net), en 2015 más de 30, 000 muertes en Europa se relacionaron con infecciones por bacterias resistentes a los antibióticos.
En el pasado, Se han buscado varios enfoques para prevenir la contaminación del implante durante la cirugía. Se han establecido e implementado protocolos asépticos posoperatorios para combatir estas bacterias resistentes a los antibióticos, pero ninguno ha cumplido por completo la función de resolver este problema.
En un estudio reciente publicado en Nano letras y resaltado en Fotónica de la naturaleza , Investigadores del ICFO Dr. Ignacio de Miguel, Arantxa Albornoz, dirigido por el Prof. ICREA en ICFO Romain Quidant, en colaboración con los investigadores Irene Prieto, Dra. Vanesa Sanz, La Dra. Christine Weis y el Dr. Pau Turon de la principal empresa de dispositivos médicos y dispositivos farmacéuticos B. Braun, han ideado una técnica novedosa que utiliza nanotecnología y fotónica para mejorar drásticamente el rendimiento de las mallas médicas para implantes quirúrgicos.
A través de una colaboración continua desde 2012, el equipo de investigadores del ICFO y B. Braun Surgical, S.A., desarrolló una malla médica con una característica particular:la superficie de la malla fue modificada químicamente para anclar millones de nanopartículas de oro. ¿Por qué? Porque se ha demostrado que las nanopartículas de oro convierten la luz en calor de manera muy eficiente en regiones muy localizadas.

Micrografías SEM del S. aureus biopelícula formada en la superficie de la malla quirúrgica. Crédito:ICFO
La técnica de utilizar nanopartículas de oro en procesos de conversión de luz-calor ya había sido probada en tratamientos contra el cáncer en estudios anteriores. Aún más, en el ICFO esta técnica había sido implementada en varios estudios previos apoyados por la Fundación Cellex, por lo tanto, es otro ejemplo destacado de cómo el apoyo filantrópico visionario temprano dirigido a abordar problemas fundamentales eventualmente conduce a aplicaciones prácticas importantes. Para este caso particular, sabiendo que cada año se realizan más de 20 millones de operaciones de reparación de hernias en todo el mundo, creían que este método podría reducir los costos médicos en las operaciones recurrentes y eliminar los tratamientos antibióticos costosos e ineficaces que se están empleando actualmente para abordar este problema.
Por lo tanto, en su experimento in vitro y a través de un proceso minucioso, el equipo cubrió la malla quirúrgica con millones de nanopartículas de oro, distribuyéndolos uniformemente por toda la estructura. Probaron las mallas para garantizar la estabilidad a largo plazo de las partículas, la no degradación del material, y el no desprendimiento o liberación de nanopartículas en el entorno circundante (matraz). Pudieron observar una distribución homogénea de las nanopartículas sobre la estructura utilizando un microscopio electrónico de barrido.
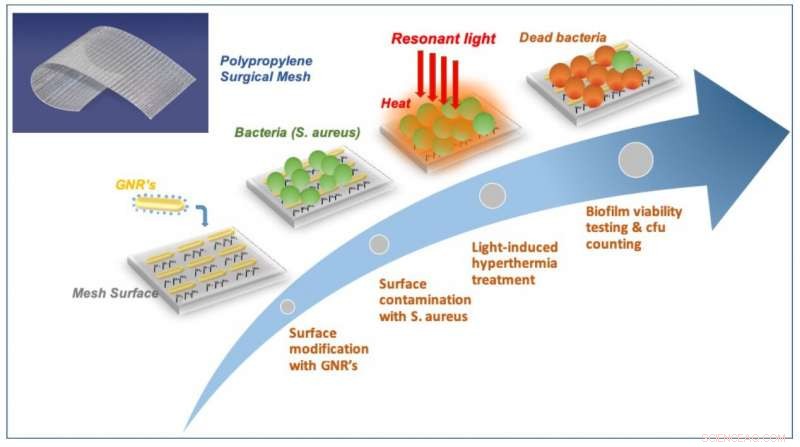
Vista esquemática de la prevención de biopelículas habilitadas por plasmón en mallas quirúrgicas. Crédito:ICFO
Una vez que la malla modificada estuvo lista, el equipo lo expuso a la bacteria S. aureus durante 24 horas hasta que observaron la formación de una biopelícula en la superficie. Después, comenzaron a exponer la malla a pulsos cortos e intensos de luz infrarroja cercana (800 nm) durante 30 segundos para garantizar que se alcanzara el equilibrio térmico, antes de repetir este tratamiento 20 veces con 4 segundos de intervalos de descanso entre cada pulso. Descubrieron lo siguiente:en primer lugar, vieron que iluminar la malla a la frecuencia específica induciría resonancias de plasmones superficiales localizados en las nanopartículas, un modo que da como resultado la conversión eficiente de luz en calor, quemando las bacterias en la superficie. En segundo lugar, utilizando un microscopio confocal de fluorescencia, vieron cuántas bacterias habían muerto o seguían vivas. Por las bacterias que quedaron vivas, observaron que las bacterias del biofilm se convirtieron en células planctónicas, recuperando su sensibilidad o debilidad hacia la terapia con antibióticos y la respuesta del sistema inmunológico. Por las bacterias muertas observaron que al aumentar la cantidad de luz entregada a la superficie de la malla, las bacterias perderían su adherencia y se despegarían de la superficie. En tercer lugar, confirmaron que operar en rangos de luz infrarroja cercana era completamente compatible con entornos in vivo, lo que significa que tal técnica probablemente no dañaría el tejido sano circundante. Finalmente, repitieron el tratamiento y confirmaron que el calentamiento recurrente de la malla no había afectado su capacidad de eficiencia de conversión.
Como comenta el profesor ICREA en ICFO Romain Quidant, "Los resultados de este estudio han allanado el camino hacia el uso de nanotecnologías de plasmón para prevenir la formación de biopelículas bacterianas en la superficie de los implantes quirúrgicos. Todavía hay varios problemas que deben abordarse, pero es importante enfatizar que tal técnica de hecho significan un cambio radical en los procedimientos de operación y una mayor recuperación del paciente ".
Dr. Pau Turon, Director de Investigación y Desarrollo en B. Braun Surgical, S.A. explica, "Nuestro compromiso de ayudar a los profesionales de la salud a evitar las infecciones hospitalarias nos impulsa a desarrollar nuevas estrategias para combatir las bacterias y las biopelículas. Además, el equipo de investigación está explorando la posibilidad de extender dicha tecnología a otros sectores en los que se deben evitar las biopelículas ".