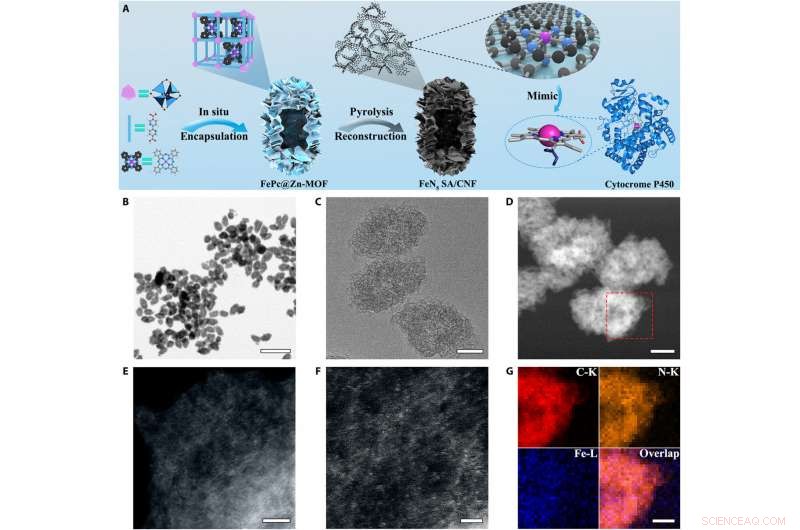
Esquema sintético y caracterización morfológica de FeN5SA / CNF. (A) Esquema del proceso de formación de sitios de Fe dispersos atómicamente confinados en nanoframe de carbono con coordinación axial de cinco N para imitar el centro activo del citocroma P450. (B y C) imágenes TEM y (D) imagen STEM anular de campo oscuro de alto ángulo (HAADF-STEM) de FeN5 SA / CNF. (E y F) Imágenes HAADF-STEM ampliadas de FeN5 SA / CNF que muestran el único átomo metálico dominante. (G) Imágenes de mapeo de EELS de FeN5 SA / CNF de la región seleccionada en (D). Barras de escala, 1 μm y 100, 100, 5, 2, y 50 nm (B a G, respectivamente). Crédito:Science Advances, doi:10.1126 / sciadv.aav5490.
Las nanozimas son nanomateriales catalíticos con características similares a las de las enzimas que han atraído un enorme interés de investigación reciente. Los nanomateriales catalíticos ofrecen ventajas únicas de bajo costo, alta estabilidad, actividad catalítica sintonizable y facilidad de producción y almacenamiento en masa. Estas propiedades son muy deseables para una amplia gama de aplicaciones en biodetección, Terapéutica de ingeniería de tejidos y protección del medio ambiente. Sin embargo, Las tecnologías de nanozimas convencionales enfrentan desafíos críticos en relación con su tamaño, composición y catálisis dependiente de facetas, además de una densidad de sitios activos inherentemente baja.
Ahora escribiendo en Avances de la ciencia , Liang Huang y sus colaboradores en los departamentos de Física y Química Electroanalítica en China detallan el descubrimiento de una nueva clase de enzimas de un solo átomo con sitios activos similares a enzimas dispersos atómicamente en nanomateriales. Los sitios mejoraron significativamente el rendimiento catalítico de las nanozimas de un solo átomo y los científicos descubrieron su mecanismo subyacente utilizando la catálisis de oxidasa como un modelo de reacción experimental junto con cálculos teóricos. Revelaron las actividades catalíticas y el comportamiento de nanozimas de un solo átomo que contienen un nanoframe de carbono (un solo átomo / nanoframe de carbono:SA / CNF) y FeN confinado. 5 centros activos (FeN 5 SA / CNF) para imitar el hemo coordinado por ligando axial natural del citocromo P450 para aplicaciones antibacterianas versátiles. Los resultados sugieren que las nanozimas de un solo átomo tienen un gran potencial para convertirse en nanozimas de próxima generación para aplicaciones en nanobiotecnología.
Desde que descubrió la actividad similar a la peroxidasa de las nanopartículas ferromagnéticas en 2007, Los científicos han diseñado varias nanozimas utilizando materiales como óxidos metálicos, metales nobles, materiales de carbono y estructuras organometálicas (MOF). Sin embargo, Dos desafíos contemporáneos permanecen en las tecnologías de nanozimas, donde (1) los sitios activos de baja densidad mostraron una menor actividad catalítica en comparación con las enzimas naturales, y (2) la composición elemental no homogénea podría complicar los mecanismos catalíticos. Debido a estos cuellos de botella, Los científicos han encontrado un desafío para descubrir los sitios precisos y el origen de la actividad enzimática, restringir las aplicaciones extensivas de nanozimas convencionales.
En el presente trabajo, Huang y sus colaboradores se propusieron resolver estos problemas mediante el descubrimiento de una nueva clase de nanoenzimas de un solo átomo que incorporan la tecnología de punta de un solo átomo para diseñar sitios activos inherentes similares a las enzimas. Los científicos demostraron que los centros metálicos dispersos atómicamente maximizaban la eficiencia y la densidad de los sitios activos en la nueva arquitectura de nanozimas. Utilizaron la estructura de coordinación bien definida para proporcionar un modelo experimental claro durante las investigaciones de su mecanismo de trabajo. Huang y col. informaron sobre un método general y eficaz para sintetizar las nanozimas de un solo átomo altamente activas imitando las estructuras espaciales de los centros activos en las enzimas naturales.
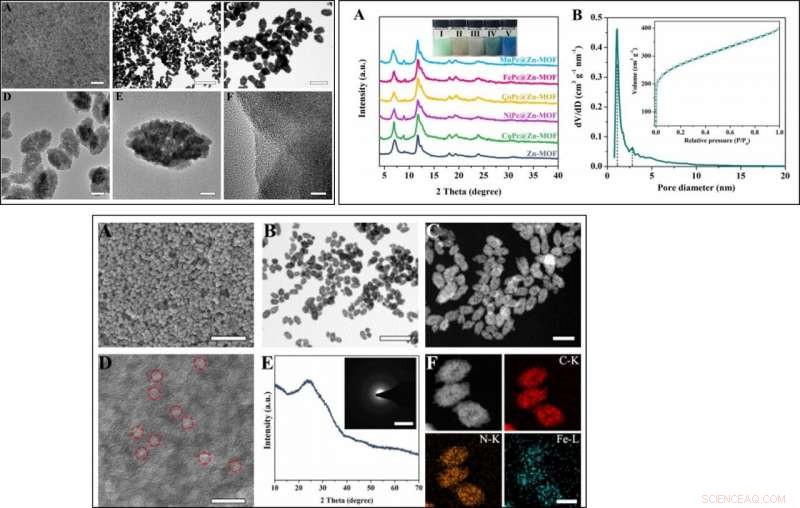
ARRIBA IZQUIERDA:Morfología del precursor Zn-MOF. (A) imagen SEM y (B) imagen TEM de ZnMOF. (C, D) Imágenes TEM y (E, F) Imágenes HRTEM de FePc @ Zn-MOF. SUPERIOR DERECHA:Estructura del precursor de Zn-MOF. (A) Patrón XRD de MnPc @ Zn-MOF (I), FePc @ Zn-MOF (II), CoPc @ Zn-MOF (III), NiPc @ Zn-MOF (IV), CuPc @ Zn-MOF (V) y ZnMOF. El recuadro es la imagen óptica del correspondiente MPc @ Zn-MOF en solución de etanol (10 mg mL-1). (Crédito de la foto:Liang Huang, Instituto de Química Aplicada de Changchun) (B) Distribución del tamaño de poro de FePc @ Zn-MOF, y el recuadro de (B) son las correspondientes isotermas de adsorción / desorción de N2. INFERIOR:Morfología y estructura de FeN5 SA / CNF. (A) imagen SEM, (B) imagen TEM, (C) imagen STEM, (D) Imagen HRTEM, (E) Patrón XRD y (F) Imágenes de mapeo elemental TEM-EDS de FeN5 SA / CNF. La estructura porosa en (D) está indicada por círculos. El recuadro de (E) es el patrón SAED correspondiente. Crédito:Science Advances, doi:10.1126 / sciadv.aav5490.
Utilizaron la catálisis de oxidasa como modelo de reacción y completaron cálculos teóricos y estudios experimentales. Los científicos identificaron la mayor actividad similar a la oxidasa del FeN 5 SA / CNF para resultar a través del efecto sinérgico y el mecanismo donante de electrones. De nota, Pantano 5 SA / CNF mostró una actividad similar a la oxidasa entre 17 y 70 veces mayor en comparación con el FeN plano cuadrado 4 catalizador y el Pt / C comercial (catalizador de platino sobre carbono) con contenido metálico normalizado. Los resultados explicaron el inesperado efecto de empuje similar a la oxidasa de la coordinación axial en FeN. 5 SA / CNF y su actividad catalítica significativamente mejorada, en comparación con las nanozimas convencionales.
Para sintetizar el FeN 5 SA / CNF, Huang y col. diseñó por primera vez una estructura huésped-huésped de ftalocianina de hierro encapsulada en un marco orgánico metálico (MOF) (FePc:FePc @ Zn-MOF). Esta estructura podría albergar diversos metales para reemplazar la ftalocianina de hierro (FePc) en experimentos posteriores como MPc donde M variaba entre manganeso (MnPc), níquel (NiPc), cobre (CuPc) a cobalto (CoPc) y pirolizó el precursor a 900 0 C bajo nitrógeno gaseoso para obtener las nanozimas de un solo átomo.
Los científicos habían demostrado previamente que el FeN cuadrado plano 4 los sitios se conservarían durante las reacciones de calcinación de porfirina de hierro y FePc (ftalocianina de hierro), pero en ausencia de soporte, los sitios monodispersos se aglomeraron en nanopartículas. En el presente proceso sintético, por lo tanto, los científicos aislaron el FeN 4 sitios confinados en los nanoframas de carbono y los coordinó con el sustrato de nitrógeno piridínico (N) para generar el FeN más termodinámico y estable 5 / C sitios.
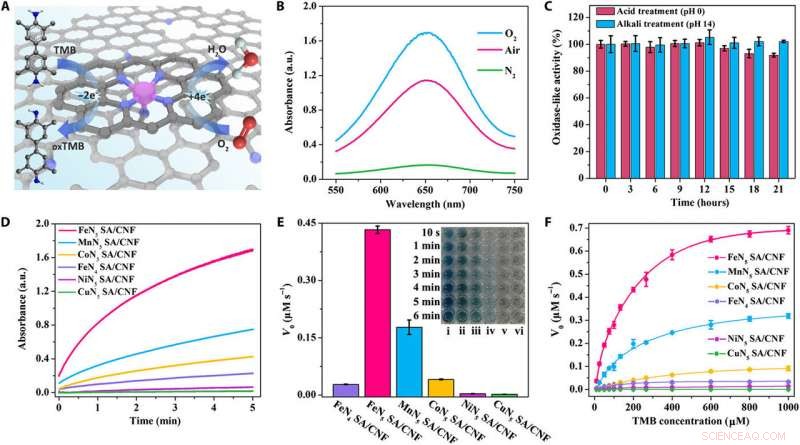
Actividad de tipo oxidasa de FeN5SA / CNF. (A) Ilustración esquemática de las características de tipo oxidasa de la oxidación de TMB catalizada por FeN5 SA / CNF. (B) Espectros de absorción ultravioleta-visible (UV-vis) de FeN5 SA / CNF en O2 saturado, saturado de aire, y tampón de acetato de sodio-ácido acético saturado en N2. (C) La durabilidad del FeN5 SA / CNF tratado con ácido (álcali) durante 21 horas. (D) Cambios de absorbancia dependientes del tiempo a 652 nm, (E) histograma de V0, y (F) curvas típicas de Michaelis-Menten en presencia de FeN5 SA / CNF (i), MnN5 SA / CNF (ii), CoN5 SA / CNF (iii), FeN4 SA / CNF (iv), NiN5 SA / CNF (v), y CuN5 SA / CNF (vi) en tampón de acetato de sodio-ácido acético saturado con aire. El recuadro de (E) es una imagen óptica de la solución de TMB catalizada por los catalizadores correspondientes. Crédito de la foto:Liang Huang, Instituto de Química Aplicada de Changchun. Crédito:Science Advances, doi:10.1126 / sciadv.aav5490
Luego, los científicos caracterizaron la morfología y estructura del FeN 5 SA / CNF usando microscopía electrónica de barrido (SEM) y microscopía electrónica de transmisión (TEM) para revelar el FePc @ Zn-MOF fusiforme como un producto dominante con morfología uniforme. Observaron que las cavidades huecas y las conchas porosas dotan al sustrato de elevadas superficies específicas y abundantes nanoporos jerárquicos.
Los patrones de difracción de rayos X (XRD) indicaron que la estructura cristalina de Zn-MOF no sufrió cambios significativos después de encapsular FePc in situ, mientras que el espectro de infrarrojos por transformada de Fourier (FTIR) de FePc @ Zn-MOF verificó la encapsulación exitosa de FePc. Luego, utilizando el mapeo de espectroscopía de pérdida de energía de electrones, los científicos demostraron que los átomos de Fe y N estaban distribuidos homogéneamente en todo el dominio, indicando la generación de sitios Fe-N en matrices 3-D.
Huang y col. analizó la estructura atómica del FeN 5 SA / CNF para mostrar que el número de coordinación del átomo de Fe era casi cinco, para confirmar la formación de cinco Fe-N 5 mitades. Para comprender la estructura subyacente a los mecanismos catalíticos, los científicos también utilizaron la espectroscopia de Mössbauer (utilizada para determinar el estado de oxidación del hierro) e investigaron la estructura electrónica y la coordinación del hierro (Fe). Luego determinaron las actividades de tipo oxidasa de FeN 5 SA / CNF utilizando ensayos colorimétricos y utilizó la oxidación de TMB (3, 3, 5, 5-tetrametilbencidina) como modelo de reacción catalítica para comprender la interacción de las moléculas de oxígeno con el FeN. 5 SA / CNF en varios entornos.
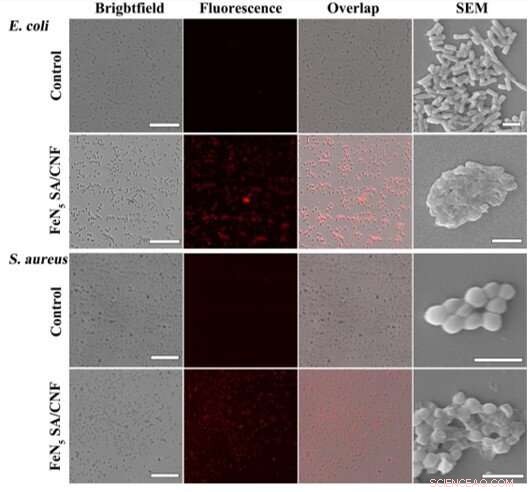
Cambios morfológicos en bacterias. Imágenes de campo claro, Imágenes de fluorescencia, imágenes superpuestas e imágenes SEM de bacterias E. coli y S. aureus tratadas o no tratadas con FeN5 SA / CNF. Las barras de escala son de 40 μm para imágenes de fluorescencia y de 2 μm para imágenes SEM. Crédito:Science Advances, doi:10.1126 / sciadv.aav5490
Los resultados mostraron la intensa actividad catalítica del FeN 5 SA / CNF durante la reducción de oxígeno y los científicos atribuyeron la tasa de oxidación de TMB a la concentración de oxígeno. Huang y col. luego estudió comparativamente las actividades de tipo oxidasa del FeN 5 SA / CNF frente a MN 5 SA / CNF donde reemplazaron M con diferentes metales de Mn, Fe, Co, Ni y Cu. Mostraron la tasa catalítica de FeN 5 SA / CNF para ser el más alto (17 órdenes más alto que FeN 4 SA / CNF) a través de distintos cambios de color a lo largo del tiempo.
Cuando Huang et al. comparó la actividad enzimática con las enzimas convencionales utilizadas anteriormente, observaron que FeN 5 SA / CNF mantuvo una actividad similar a la oxidasa comparativamente muy superior. De nota, la tasa catalítica de las nuevas nanozimas fue 70 veces mayor que la del Pt / C comercial. Según los resultados experimentales, Los científicos validaron que mecánicamente el átomo metálico central y la estructura axial coordinada de cinco N eran importantes para las actividades superiores de tipo oxidasa de las nanozimas de un solo átomo.
Como una aplicación práctica de la actividad catalítica de alta oxidación, las nanozimas de un solo átomo de FeN 5 SA / CNF podría generar especies reactivas de oxígeno durante la reducción catalítica de oxígeno, que puede dañar la membrana de las bacterias para acciones antibacterianas efectivas. Para evaluar la actividad antibacteriana, Huang y col. llevó a cabo experimentos in vitro y detectó las tasas de supervivencia de Escherichia coli y Staphylococcus aureus células en exposición a las nanozimas. En comparación con un grupo de control, los científicos observaron tasas de supervivencia bacteriana marcadamente reducidas; corroborar las altas actividades de tipo oxidasa del FeN 5 SA / CNF para una actividad antibacteriana significativa.
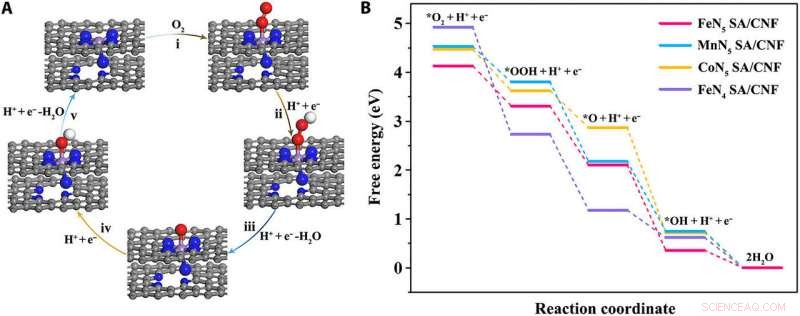
Theoretical investigation of oxidase-like activity over FeN5SA/CNF. (A) Proposed reaction pathways of O2 reduction to H2O with optimized adsorption configurations on FeN5 SA/CNF. The gray, azul, purple, rojo, and white balls represent the C, NORTE, Fe, Oh and H atoms, respectivamente. (B) Free energy diagram for oxygen reduction reaction on single-atom enzyme mimics with TMB as reductant in an acidic medium. Credit:Science Advances, doi:10.1126/sciadv.aav5490
Based on the in vitro experimental outcomes, the scientists next conducted in vivo antibacterial studies using the new nanozymes. Para esto, they used a wound infection model of mice to understand the antibacterial efficacy of FeN 5 SA/CNF. After 4-days of infecting a wound site with E. coli followed by nanozyme therapy, Huang et al. observed the clear remission of ulceration and accelerated wound healing in the treatment group.
The scientists verified the in vivo healing process using histopathology studies of the wounded tissue stained with hematoxylin and eosin. The results showed that keratinocytes migrated to the wound site from the normal tissue, to thicken the epidermis after treatment, confirming a highly biocompatible bacterial nanozyme. Como antes, Huang et al. credited the results to the architecture of atomically dispersed FeN 5 sites, as actual active centers in these catalysts.
To determine the precise origin of the enhanced oxidase-like activity of the FeN 5 SA/CNF using theoretical calculations, Huang et al. performed density functional theory (DFT) calculations. Para esto, they used the oxygen molecular reduction process of single-atom metal sites, with TMB molecules as the reducing agent in acidic conditions. The scientists showed that compared with the starting square planar FeN 4 SA/CNF, the axial-coordinated N atom used to form FeN 5 SA/CNF provided a strong push effect in the nanozymes architecture; to activate the oxygen molecule and cleave the O-O bond. This process promoted the oxidative capacity of the single atom nanozymes, to acquire acidic hydrogens from substrates such as TMB, while oxidizing them. Thereby, based on the DFT calculations, Huang et al. unmistakably credited the origin of the superior oxidase-like activity to the central metal atom and the steric configurations of single-atom nanozymes.
De este modo. Huang and colleagues reported the discovery of a new class of single-atom nanozymes with atomically dispersed enzyme-like active sites in nanomaterials. The new nanozymes showed significantly superior catalytic performance compared with conventional nanozymes in the lab. The observations resulted in uncovering their underlying mechanism during the study, using oxidase catalysis as a model reaction. Using both experimental studies and theoretical calculations, the scientists revealed the electron-push effect mechanism crucial to endow FeN 5 SA/CNF with the characteristically superior oxidase-like activity, compared to other nanozymes. This led to efficient bactericidal investigations and wound disinfection in vitro and in vivo. The scientists present a new perspective to the catalytic mechanisms and rational design of nanozymes to exhibit great potential and predict the origin of a next-generation nanozyme.
© 2019 Science X Network