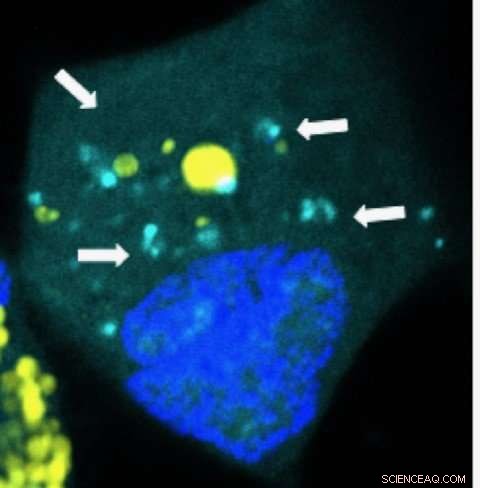
Nanopartículas que liberan microARN (azul claro) dentro de una célula cancerosa del cerebro humano. Crédito:Yuan Rui, Johns Hopkins
En un estudio de "prueba de concepto", Los científicos de Johns Hopkins Medicine dicen que han entregado con éxito paquetes de código genético de tamaño nanométrico llamados microARN para tratar tumores cerebrales humanos implantados en ratones. El contenido de los contenedores superpequeños se diseñó para apuntar a las células madre cancerosas, una especie de "semilla" celular que produce innumerables progenies y es una barrera implacable para librar al cerebro de células malignas.
Los resultados de sus experimentos se publicaron en línea el 21 de junio en Nano letras .
"El cáncer de cerebro es uno de los cánceres más conocidos en términos de su composición genética, pero aún tenemos que desarrollar un buen tratamiento para ello, "dice John Laterra, MARYLAND., Doctor., profesor de neurología, oncología y neurociencia en la Facultad de Medicina de la Universidad Johns Hopkins y científica investigadora en el Instituto Kennedy Krieger. "La resistencia de las células madre del cáncer y la barrera hematoencefálica son obstáculos importantes".
La sangre que ingresa al cerebro se filtra a través de una serie de vasos que actúan como barrera protectora. Pero esta barrera hematoencefálica bloquea los medicamentos moleculares que tienen el potencial de revolucionar la terapia del cáncer de cerebro al dirigirse a las células madre del cáncer. dice Laterra.
"Para modernizar los tratamientos de tumores cerebrales, necesitamos herramientas y métodos que eludan la barrera hematoencefálica, "dice Jordan Green, Doctor., profesor de ingeniería biomédica, oftalmología, oncología, neurocirugía, ciencia e ingeniería de materiales e ingeniería química y biomolecular en la Facultad de Medicina de la Universidad Johns Hopkins. "Necesitamos tecnología para administrar de forma segura y eficaz medicamentos genéticos sensibles directamente a los tumores sin dañar el tejido normal".
Un ejemplo de ello, Green dice:es glioblastoma, la forma de cáncer de cerebro que está luchando el senador de Arizona John McCain, que a menudo requiere cirugías repetidas. Los médicos extraen el tejido del tumor cerebral que pueden ver, pero la malignidad a menudo regresa rápidamente, dice Laterra. La mayoría de los pacientes con glioblastoma viven menos de dos años después del diagnóstico.
Los científicos han sospechado durante mucho tiempo que las células madre del cáncer son la raíz de lo que impulsa el regreso y la propagación del glioblastoma y otros cánceres. Estas células madre dan lugar a otras células cancerosas y, si evaden el bisturí del cirujano, puede conducir a un tumor completamente nuevo.
Laterra y Green, que son miembros del Centro Oncológico Johns Hopkins Kimmel, diseñó una forma de entregar de manera eficiente paquetes súper pequeños de microARN en tumores cerebrales establecidos. Los microARN se dirigen a las células madre del cáncer de cerebro para detener su capacidad de propagarse y mantener el crecimiento del tumor.
Los paquetes están hechos de plástico biodegradable similar al material utilizado para las suturas quirúrgicas y que se degrada con el tiempo. Son 1, 000 veces más pequeño que el ancho de un cabello humano y típico del tamaño y la forma de los componentes naturales que utilizan las células para comunicarse. Cuando las células cancerosas engullen los paquetes, se rompen y liberan su "carga útil" de microARN específicamente donde los microARN necesitan actuar dentro de las células cancerosas.
Encerrados en el nanopaquete hay microARN que se unen específicamente a ARN mensajeros ligados a dos genes:HMGA1 y DNMT, que funcionan juntos para regular los programas de expresión génica en las células.
Cuando los microARN se unen a estos ARN mensajeros, bloquean sus capacidades de producción de proteínas y desactivan los programas que impulsan las características parecidas a los tallos de las células cancerosas. Sin sus propiedades parecidas a tallos, las células cancerosas están más diferenciadas, pierden su capacidad de propagar tumores, y pueden ser más susceptibles a la radiación y las drogas.
Por sus experimentos, los científicos de Johns Hopkins implantaron células de glioblastoma humano en 18 ratones. Para imitar el desafío clínico de tratar un tumor existente, los científicos esperaron 45 días antes de tratar a los animales para asegurarse de que tuvieran tumores bien formados. La mitad de los animales recibieron infusiones de nanopaquetes que contienen microARN activos directamente en sus tumores cerebrales. y la otra mitad recibió nanopaquetes que contenían microARN inactivos. Para aislar el efecto de las nanopartículas, the scientists used mice that were bred without immune system T-cells that target cancer cells.
Five of the nine mice receiving inactive microRNAs (controls) died within two months, and the rest of the control mice died within 90 days. Three of the nine mice receiving active microRNAs lasted up to 80 days, and six lived to 133 days. Those six were humanely euthanized, and isolated mouse brains were examined for the presence of tumors.
All of the control mice had large tumors in their brains when they died. Four of the mice that received active microRNAs and lived to 133 days had no tumors, and two had small ones.
Green says that many genetic medicines are designed to target one gene. The type of nanoparticles the Johns Hopkins team used in this study can encapsulate multiple types of microRNAs to target multiple gene networks.
When the brain cancer stem cells internalize the nanoparticle and transition to a non-stem-cell state, Laterra says, clinicians could exploit that condition, and give radiation or other drugs to kill the now-vulnerable cells.
Green says scientific teams elsewhere are developing microRNA packets using lipid-based materials, and some standard chemotherapy is delivered in a fatty nanoparticle called a liposome.
Green and Laterra say the nanoparticles in their study are able to permeate the entire tumor because rodent brains are small. Humans, with bigger brains, may need a pump and catheter to funnel nanoparticles throughout the brain.
The Johns Hopkins team is working to scale up development of its nanoparticles and standardize their stability and quality before applying for permission to begin clinical trials on people.