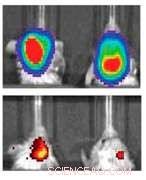
La fila superior indica ratones con glioblastoma controlado por tamaño del tumor. La fila inferior muestra su expresión de MGMT, una proteína que hace que las células tumorales sean más resistentes a la quimioterapia. La izquierda es un control mientras que el de la derecha muestra niveles significativamente reducidos de MGMT después del tratamiento con las nanopartículas. Crédito:Universidad Northwestern
Los científicos de Northwestern Medicine han desarrollado una nueva plataforma de pruebas para evaluar, en tiempo real, la eficacia de los nanomateriales en la regulación de la expresión génica. Los resultados, publicado en procedimientos de la Academia Nacional de Ciencias , podría ayudar a facilitar las investigaciones preclínicas y optimizar la nanoterapéutica para los cánceres antes de que lleguen a los ensayos clínicos.
Timothy Sita, un estudiante de séptimo año de MD / PhD en el Programa de Capacitación para Científicos Médicos, fue el primer autor del estudio, que miró la plataforma en modelos animales.
"Este es un importante paso adelante para el campo, "dijo el investigador principal Alexander Stegh, Doctor, profesor asistente de Neurología y Medicina. "La optimización muy completa que vemos en el desarrollo de fármacos convencionales había faltado en el espacio de la nanotecnología, y nos sentimos muy decididos a cambiar esto. El sistema que desarrollamos aquí realmente nos permite apoyar esos esfuerzos, y evaluar nuestras nanopartículas en los modelos más relevantes, en un entorno in vivo ".
Chad Mirkin, Doctor, el Profesor George B. Rathmann de Química en la Facultad de Artes y Ciencias de Weinberg y profesor de Medicina en la División de Hematología / Oncología, también fue autor correspondiente del artículo.
Los científicos demostraron el concepto mientras usaban nanoestructuras llamadas ácidos nucleicos esféricos (SNA) para apuntar a un gen del factor de resistencia en el glioblastoma. un agresivo, tipo incurable de tumor cerebral.
SNA, desarrollado por primera vez por Mirkin en Northwestern en 1996, consisten en hebras densas de ARN empaquetadas alrededor de un núcleo de nanopartículas. Debido a sus propiedades únicas, Los SNA son capaces tanto de cruzar la barrera hematoencefálica como de entrar en las células tumorales, donde pueden apuntar directamente a la actividad genética que estimula el crecimiento del cáncer.
Si bien estos conjugados son una herramienta prometedora en la era de la medicina de precisión, Los científicos anteriormente carecían de un método cuantitativo para evaluar cómo los ARS regulaban la actividad genética en organismos vivos, lo que proporcionaría nuevos conocimientos sobre cómo optimizar las terapias.
"Hemos visto que estas partículas básicamente pueden atacar cualquier gen del cáncer, pero no sabíamos cuándo funcionaban mejor o qué regímenes de dosificación usar, "Dijo Sita." Como tal, los ensayos preclínicos no fueron tan exitosos como podrían haber sido ".
En el estudio actual, los científicos demostraron que al usar un tipo de imágenes no invasivas en los ratones, pudieron medir en tiempo real cómo las nanopartículas afectaban los niveles de una proteína diana intratumoral.
"Ahora podemos modificar estas partículas:jugar con la forma de la nanopartícula, o cuánto ARN cargamos en la partícula, por ejemplo, y luego evaluar muy rápidamente si esos cambios son más efectivos o no, "Sita explicó." Es una plataforma para ayudar a optimizar los medicamentos en ratones antes de que vayan a los ensayos en humanos, y hacer algo que se traduzca mejor en la clínica ".
Si bien el método podría generalizarse a la investigación de nanoterapias para muchos tipos de cánceres, el estudio también tiene implicaciones clínicas exclusivas del glioblastoma.
Los científicos desarrollaron nanopartículas para eliminar la O6-metilguanina-ADN metiltransferasa (MGMT), una proteína que reduce el impacto de la quimioterapia, en ratones con glioblastoma. A través de la plataforma de imágenes, descubrieron que los ratones tenían los niveles más bajos de proteína entre 24 y 48 horas después de recibir las nanopartículas, sugiriendo el momento óptimo para administrar la quimioterapia.
"Mostramos una reducción muy significativa en el volumen del tumor cuando combinamos estas partículas con la quimioterapia, "Sita dijo." Al silenciar este gen que causa resistencia a la quimioterapia, podemos tener una respuesta mucho más profunda. Ese es el ángulo clínico clave ".