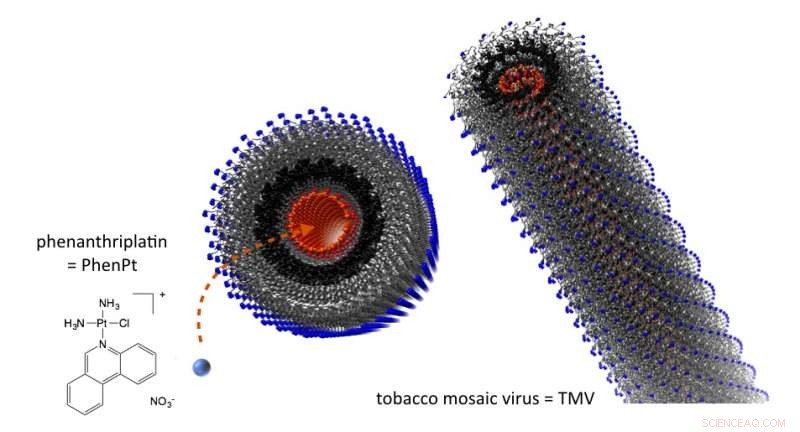
Cuando se empaqueta dentro de nanopartículas del virus del mosaico del tabaco, el fenantriplatino se administra a los tumores, donde se demostró que era más eficaz in vivo que un platino aprobado. Crédito:Universidad Case Western Reserve
En un par de primicias Investigadores de la Universidad Case Western Reserve y el Instituto de Tecnología de Massachusetts han demostrado que el fenantriplatino candidato a fármaco puede ser más eficaz que un fármaco aprobado in vivo. y que un vehículo basado en virus de plantas administra con éxito un fármaco in vivo.
Los tumores de cáncer de mama triple negativos de ratones tratados con nanopartículas portadoras de fenantriplatino eran cuatro veces más pequeños que los tratados con cisplatino, un fármaco de quimioterapia común y relacionado, o fenantriplatino libre inyectado por vía intravenosa en la circulación.
Los científicos creen que el trabajo reportado en la revista ACS Nano , es un paso prometedor hacia los ensayos clínicos.
"Es posible que hayamos encontrado el portador perfecto para este fármaco candidato en particular, "dijo Nicole Steinmetz, profesor asistente de ingeniería biomédica en Case Western Reserve, que ha pasado 10 años estudiando el uso de virus vegetales con fines médicos.
Se asoció con Stephen J. Lippard, Arthur Amos Noyes Profesor de química en el MIT, y un experto en interacciones biológicas que involucran quimioterapias a base de platino.
Los medicamentos a base de platino se utilizan para tratar a más de la mitad de los pacientes con cáncer que reciben quimioterapia. Dos de los fármacos más utilizados son el cisplatino y el carboplatino. Forman enlaces cruzados bifuncionales con el ADN en las células cancerosas, que impiden que el ADN transcriba genes y provocan la muerte celular, Lippard explicó.
A pesar de su uso generalizado, Se ha demostrado que el cisplatino cura solo el cáncer de testículo. y muchos cánceres tienen o desarrollan inmunidad al fármaco.
El laboratorio de Lippard alteró el cisplatino reemplazando un ion cloruro con fenantridina y descubrió que la nueva molécula también se une al ADN. En lugar de formar enlaces cruzados, sin embargo, El fenantriplatino se une a un solo sitio pero aún bloquea la transcripción.
De hecho, su laboratorio descubrió que el fenantriplatino es hasta 40 veces más potente que los platinos tradicionales cuando se prueba directamente contra las células cancerosas del pulmón, seno, hueso y otros tejidos. La molécula también parece evitar los mecanismos de defensa que transmiten resistencia.
Pero cuando se inyecta en modelos de cáncer de ratón, el candidato a fármaco no se comportó mejor que los platinos estándar.
Lippard se dio cuenta de que el fenantriplatino no estaba alcanzando su objetivo. Tenía un problema con la administración de medicamentos.
Encontró una solución potencial mientras visitaba el campus de Case Western Reserve y escuchó a Steinmetz explicar su trabajo de investigación del virus del mosaico del tabaco (TMV) para la administración de medicamentos hace más de un año.
"Imaginé que TMV sería el vehículo perfecto, "Dijo Lippard." Así que tomamos una cerveza y formamos una colaboración ".
El largo, Las nanopartículas delgadas del virus del mosaico del tabaco son naturales para administrar el fármaco candidato a los tumores. dijo Steinmetz, quien fue designado por la Escuela de Medicina Case Western Reserve.
Las partículas de virus que no infectará a los humanos, son huecos. Un tubo central de unos 4 nanómetros de diámetro corre a lo largo de la carcasa y el revestimiento lleva una carga negativa.
El fenantriplatino mide aproximadamente 1 nanómetro de ancho y, cuando se trata con nitrato de plata, tiene una fuerte carga positiva. Entra fácilmente y se adhiere al revestimiento central.
La forma alargada de la nanopartícula hace que se mueva a lo largo de los márgenes de los vasos sanguíneos, permanecen desapercibidos para las células inmunitarias y pasan a través de la vasculatura con fugas de los tumores y se acumulan en el interior. Poco tejido sano está expuesto a la droga tóxica.
Dentro de los tumores, las nanopartículas se acumulan dentro de los compartimentos lisosomales de las células cancerosas, Dónde están, en esencia, digesto. El pH es mucho más bajo que en la sangre circulante, Steinmetz explicó. La cáscara se deteriora y libera fenantriplatino.
La cáscara se descompone en proteínas y se elimina a través de procesos metabólicos o celulares naturales en un día mientras el candidato a fármaco comienza a bloquear la transcripción. conduciendo a mayores cantidades de muerte celular por apoptosis que los platinos reticulantes.
Los investigadores dicen que la administración del fenantriplatino en el tumor condujo a un mejor rendimiento sobre el cisplatino o el fenantriplatino libre.
Lippard y Steinmetz continúan colaborando, investigar el uso de este sistema para administrar otros fármacos o candidatos a fármacos, uso en otros tipos de cánceres, la adición de agentes en el exterior del caparazón para aumentar la acumulación dentro de los tumores y más.