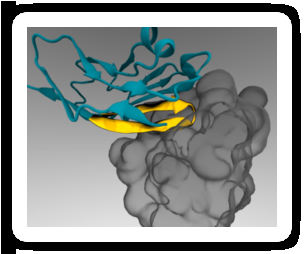
Se puede adjuntar un "pasaporte" de péptido mínimo (amarillo) a las nanopartículas terapéuticas para que se una a un receptor de células inmunitarias (gris) y evite la absorción. Crédito:Diego Pantano
Los científicos han encontrado una forma de hacer pasar nanopartículas que llevan fármacos que combaten tumores a través de las células del sistema inmunológico. que normalmente engulliría las partículas, impidiéndoles alcanzar su objetivo. La técnica aprovecha el hecho de que todas las células del cuerpo humano muestran una proteína en sus membranas que funciona como un "pasaporte" específico para instruir a las células inmunitarias para que no las ataquen. Al unir una pequeña parte de esta proteína a las nanopartículas, Los científicos pudieron engañar a las células inmunes en ratones para que reconocieran las partículas como 'propias' en lugar de extrañas, aumentando así la cantidad de medicación administrada a los tumores.
Nanotecnología del cáncer
Los enfoques actuales de la quimioterapia dejan a los pacientes con efectos secundarios graves porque los medicamentos contra el cáncer destinados a destruir tumores matan inadvertidamente las células sanas del cuerpo. Pero los científicos han desarrollado recientemente nanopartículas que pueden transportar medicamentos tóxicos directamente a los tumores sin afectar el tejido sano. Debido a su pequeño tamaño, Las nanopartículas escapan de los vasos sanguíneos con fugas que son característicos de los tumores y se acumulan en el tejido canceroso. Las células tumorales absorben las partículas que liberan su contenido tóxico una vez dentro. Este sistema de administración localizado permite a los médicos administrar a los pacientes dosis más altas de medicamentos de lo que normalmente se tolerarían.
Se han realizado intentos previos para evitar el ataque del sistema inmunológico mediante el recubrimiento de nanopartículas densamente con "cepillos" de polietilenglicol (PEG) que bloquean físicamente la adhesión de proteínas que normalmente se depositan en cuerpos extraños para atraer macrófagos. Si bien estos cepillos retrasan el inicio de la respuesta inmune, no lo impiden.
La inspiración para el trabajo revolucionario de Discher se remonta a trece años cuando un grupo de investigadores mostró con ratones modificados genéticamente que una proteína llamada CD47, que se encuentra en las membranas celulares de casi todos los mamíferos, interactúa con un receptor en los macrófagos llamado SIRPa. y, al hacerlo, indica que la célula es nativa y no debe destruirse. Los hallazgos se basaron en eliminar el CD47 del ratón y plantearon muchas preguntas, incluyendo cómo sobreviven esos ratones y si es relevante para los humanos.
Discher, que estaba diseñando nanopartículas que se autoensamblan en varias formas en el momento del descubrimiento, se dio cuenta de que el mecanismo CD47-SIRPa para el autorreconocimiento podía, en principio, ser explotado para ayudar a que las nanopartículas se escapen del sistema inmunológico. Pero también estaba claro que las versiones humanas de proteínas purificadas debían estudiarse para cualquier traducción a humanos.
En 2008, El laboratorio de Discher demostró que el CD47 humano actúa de manera similar al CD47 de ratón como un "marcador de sí mismo" a través de la señalización a través del receptor SIRPa. Poco después, un grupo de investigadores dilucidó la estructura combinada de CD47 y SIRPa humanos en detalle atómico. El laboratorio de Discher utilizó esta información para realizar simulaciones por computadora e identificar la porción más pequeña de CD47 que aún podría unirse a SIRPa. El resultado fue un péptido corto que el laboratorio de Discher sintetizó químicamente y se adhirió a nanopartículas estándar.
"Reducir el CD47 a un péptido esencial fue un paso clave, ", dijo Discher." La secuenciación de miles de genomas humanos en todo el mundo ha revelado recientemente muchas variaciones en las secuencias de CD47 y SIRPa. Necesitábamos diseñar un péptido 'universal' que pudiera unirse a SIRPa y funcionar en todos los humanos a pesar de estas diferencias ".
Las nanopartículas sigilosas evitan la respuesta inmune
Para probar si su péptido podría ayudar a las nanopartículas a evadir el sistema inmunológico, El equipo de Discher inyectó nanopartículas unidas a péptidos y nanopartículas que carecen de CD47 en ratones. Ambos tipos de nanopartículas contenían un tinte fluorescente que permitió a los científicos rastrear las partículas. En un artículo publicado el 22 de febrero, 2013 en Ciencias , los investigadores informaron que en solo treinta minutos después de la inyección de las partículas, la sangre de los ratones contenía cuatro veces más nanopartículas que contenían péptido CD47 que partículas sin el péptido, lo que sugiere que los macrófagos consideraban que las partículas unidas a CD47 eran similares a las células que pertenecían al cuerpo.
Animado por estos resultados iniciales, el equipo luego llenó sus nanopartículas unidas a CD47, así como nanopartículas recubiertas de PEG sin CD47, con el fármaco contra el cáncer paclitaxel más un anticuerpo dirigido al tumor. El equipo inyectó por separado ambos tipos de nanopartículas, así como Cremophore, el portador estándar de paclitaxel, en ratones con tumores similares a los humanos. Después de solo un día los tumores en ratones inyectados con nanopartículas unidas a CD47 tenían el 70% del tamaño de los inyectados con las nanopartículas recubiertas de PEG. Adicionalmente, Las nanopartículas unidas a CD47 fueron tan buenas o mejores para reducir los tumores como Cremophore sin causar ningún efecto secundario. El equipo pasó a documentar los cambios moleculares que ocurren dentro de los macrófagos cuando CD47 inhibe la absorción. sugiriendo que se podrían usar medicamentos adicionales para inhibir el aclaramiento.
"Actualmente se están realizando ensayos clínicos que utilizan nanopartículas para administrar medicamentos contra el cáncer, pero la autorización del sistema inmunológico sigue siendo un obstáculo importante, "dijo Karen Peterson, Doctor., Asesor Senior de Programas Extramuros en NIBIB. "El trabajo de Discher es un enfoque elegante, lo que podría permitir que otros nanoterapéuticos sean efectivos en ensayos clínicos al proporcionar una "autenticación" molecular que el cuerpo no reconoce como extraña ".
Peterson también señaló la combinación de bioingeniería y modelado informático que se utilizó para generar el péptido; La capacidad de Discher para probar la función de péptidos de diferentes tamaños mediante simulación por computadora primero, y luego producir un péptido artificial basado en estas simulaciones le permitió eliminar parte del juego de adivinanzas, ahorrando tiempo y dinero a largo plazo.
Aplicaciones futuras
Discher especula que su péptido CD47 podría usarse de manera similar para prevenir la eliminación inmunitaria de los virus utilizados para administrar genes para el tratamiento de terapia génica o para mejorar la biocompatibilidad y la durabilidad de objetos extraños más grandes, como marcapasos e implantes. cuyas partes pueden degradarse con el tiempo debido a los ataques del sistema inmunológico.