
Se muestra un campo de células de cáncer de próstata humano después de la exposición a nanopartículas de carbón activado por láser. Las muchas células verdes han adoptado un compuesto terapéutico modelo, calceína mientras que las pocas células teñidas de rojo están muertas. Cada uno de los puntos verdes o rojos es una sola celda. Crédito:Crédito:Prerona Chakravarty
Usando "nanoblastos" químicos que perforan pequeños agujeros en las membranas protectoras de las células, Los investigadores han demostrado una nueva técnica para obtener pequeñas moléculas terapéuticas, proteínas y ADN directamente en células vivas.
Las nanopartículas de carbono activadas por ráfagas de luz láser activan las pequeñas ráfagas, que abren agujeros en las membranas celulares el tiempo suficiente para admitir agentes terapéuticos contenidos en el fluido circundante. Al ajustar la exposición al láser, los investigadores administraron un compuesto marcador de molécula pequeña al 90 por ciento de las células objetivo, mientras mantenían vivas a más del 90 por ciento de las células.
La investigación fue patrocinada por los Institutos Nacionales de Salud y el Instituto de Ciencia y Tecnología del Papel de Georgia Tech. Se informará en la edición de agosto de la revista. Nanotecnología de la naturaleza .
"Esta técnica podría permitirnos administrar una amplia variedad de terapias que ahora no pueden ingresar fácilmente a las células, "dijo Mark Prausnitz, profesor de la Escuela de Ingeniería Química y Biomolecular del Instituto de Tecnología de Georgia. "Uno de los usos más importantes de esta tecnología podría ser para terapias basadas en genes, que ofrecen una gran promesa en medicina, pero cuyo progreso se ha visto limitado por la dificultad de introducir ADN y ARN en las células ".
Se cree que el trabajo es el primero en utilizar la activación de nanopartículas de carbono reactivas mediante láseres para aplicaciones médicas. Se necesitarán más investigaciones y ensayos clínicos antes de que la técnica pueda usarse en humanos.
Los investigadores han intentado durante décadas impulsar el ADN y el ARN de manera más eficiente en las células con una variedad de métodos, incluido el uso de virus para transportar material genético a las células, recubrir ADN y ARN con agentes químicos o emplear campos eléctricos y ultrasonidos para abrir las membranas celulares. Sin embargo, estos métodos anteriores generalmente han sufrido problemas de baja eficiencia o seguridad.
Con su nueva técnica, que se inspiró en trabajos anteriores sobre el llamado "efecto fotoacústico, "Prausnitz y colaboradores Prerona Chakravarty, Wei Qian y Mostafa El-Sayed esperan localizar mejor la aplicación de energía a las membranas celulares, creando un enfoque más seguro y eficiente para la administración intracelular de fármacos.
Su técnica comienza con la introducción de partículas de negro de humo de 25 nanómetros (una millonésima de pulgada) de diámetro en el líquido que rodea las células en las que se introducirán los agentes terapéuticos. Luego, se aplican ráfagas de luz infrarroja cercana de un láser de femotosegundos al fluido a una velocidad de 90 millones de pulsos por segundo. Las nanopartículas de carbono absorben la luz, lo que los calienta. Las partículas calientes luego calientan el fluido circundante para producir vapor. El vapor reacciona con las nanopartículas de carbono para formar hidrógeno y monóxido de carbono.
Los dos gases forman una burbuja que crece a medida que el láser proporciona energía. La burbuja colapsa repentinamente cuando se apaga el láser, creando una onda de choque que perfora las membranas de las células cercanas. Las aberturas permiten que los agentes terapéuticos del fluido circundante ingresen a las células. Los agujeros se cierran rápidamente para que la celda pueda sobrevivir.
Los investigadores han demostrado que pueden obtener calceína de molécula pequeña, la proteína de albúmina de suero bovino y el ADN plasmídico a través de las membranas celulares de células de cáncer de próstata humano y células de gliosarcoma de rata utilizando esta técnica. Se observó absorción de calceína en el 90 por ciento de las células a niveles de láser que dejaron vivas a más del 90 por ciento de las células.
"Podríamos conseguir que casi todas las células captaran estas moléculas que normalmente no entrarían en las células, y casi todas las celdas se mantuvieron vivas, "dijo Prerona Chakravarty, el autor principal del estudio. "Nuestro sistema de nanopartículas de carbón activado por láser permite implosiones de burbujas controladas que pueden romper las membranas celulares lo suficiente para que las moléculas entren sin causar daños duraderos".
Para evaluar cuánto tiempo permanecieron abiertos los orificios de la membrana celular, los investigadores dejaron la terapéutica simulada fuera del fluido cuando las células fueron expuestas a la luz láser, luego agregó los agentes un segundo después de apagar el láser. No vieron casi ninguna absorción de las moléculas, sugiriendo que las membranas celulares se volvieron a sellar rápidamente.
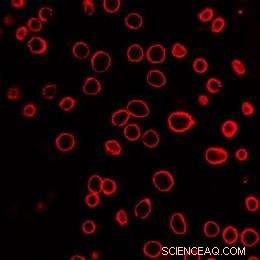
Se muestra un campo de células de cáncer de próstata humano después de la exposición a nanopartículas de carbón activado por láser. Las membranas celulares se tiñeron de rojo para ayudar en la visualización. Cada uno de los círculos rojos es una sola celda. Crédito:Crédito:Prerona Chakravarty
Para confirmar que la reacción carbono-vapor era un factor crítico que impulsaba los nanoblastos, los investigadores sustituyeron nanopartículas de oro por nanopartículas de carbono antes de la exposición a la luz láser. Debido a que carecían del carbono necesario para la reacción, las nanopartículas de oro produjeron poca absorción de las moléculas, Señaló Prausnitz.
Similar, los investigadores sustituyeron las nanopartículas de carbono por nanotubos de carbono, y también midió poca absorción, lo que explicaron señalando que los nanotubos son menos reactivos que las partículas de negro de humo.
La experimentación mostró además que el ADN introducido en las células a través de la técnica activada por láser seguía siendo funcional y capaz de impulsar la expresión de proteínas. Cuando se introdujo ADN plasmídico que codificaba la expresión de luciferasa en las células cancerosas, la producción de luciferasa aumentó 17 veces.
Para el futuro, Los investigadores planean estudiar el uso de un láser de nanosegundos menos costoso para reemplazar el instrumento ultrarrápido de femtosegundos utilizado en la investigación. También planean optimizar las nanopartículas de carbono para que casi todas se consuman durante la exposición a la luz láser. Las nanopartículas de carbono sobrantes en el cuerpo no deberían producir efectos nocivos, aunque el cuerpo no pueda eliminarlos, Señaló Prausnitz.
"Este es el primer estudio que muestra una prueba de principio para la activación con láser de nanopartículas de carbono reactivas para la administración de fármacos y genes, ", dijo." Hay un camino considerable por delante antes de que esto pueda llevarse a la medicina, pero somos optimistas de que este enfoque puede proporcionar en última instancia una nueva alternativa para administrar agentes terapéuticos en las células de manera segura y eficiente ".