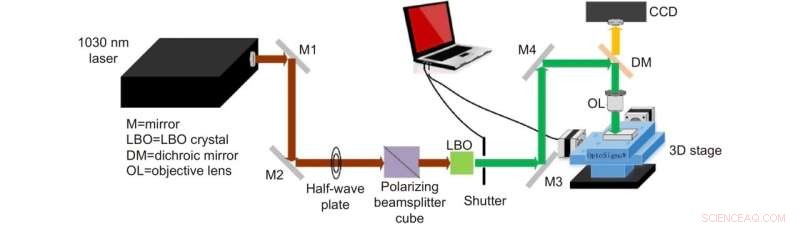
Figura 1. Esquema del sistema de fabricación láser para chips SERS de microfluidos. Crédito:Compuscript Ltd
Una nueva publicación de Opto-Electronic Advances analiza la detección de trazas sin etiqueta de biomoléculas mediante dispersión Raman mejorada en superficie asistida por interfaz líquida utilizando un chip de microfluidos.
La dispersión Raman mejorada en superficie (SERS) ha atraído la atención en biotecnología. Se debe a su alta sensibilidad a la resonancia de plasmones de superficie localizada de metales nanoestructurados. La detección de trazas de biomoléculas con gran peso molecular sigue siendo un desafío porque se requiere tratar el sustrato SERS con agentes de acoplamiento o reticulación. Los investigadores aplicaron SERS asistido por interfaz líquida para realizar la detección de trazas de biomoléculas sin etiquetas. Los resultados sugieren que es prometedor para el diagnóstico en etapa temprana de la infección por virus y la enfermedad de Alzheimer.
La dispersión Raman mejorada en superficie (SERS), basada en un efecto óptico de campo cercano inducido por el plasmón superficial de nanopartículas de metales nobles o nanoestructuras excitadas por radiación láser, amplifica las señales Raman hasta 10 14 veces en comparación con el Raman normal. Debido a su mayor intensidad, la técnica SERS continúa atrayendo un interés creciente en la detección y el análisis de biomateriales a nivel de trazas. Ha aumentado el interés en campos como la obtención de imágenes de orgánulos en una sola célula, el seguimiento de células cancerosas y la identificación de biomarcadores.
La técnica SERS se puede utilizar en el campo biomédico para el diagnóstico de enfermedades en una etapa temprana y también en la terapia de tumores. Aunque el factor de mejora de SERS normalmente oscila entre 10 6 – 10 8 debido al uso de métodos y sustratos SERS novedosos, la detección de una sola molécula mediante SERS sin etiquetas es impracticable debido al parpadeo de SERS, y el origen de este fenómeno se debe al escape de moléculas de analito de los puntos críticos. Además, las biomoléculas, incluido el ácido desoxirribonucleico (ADN) y las proteínas, son difíciles de detectar directamente mediante SERS. Se necesitan tratamientos adicionales con un sustrato SERS para unir las biomoléculas.
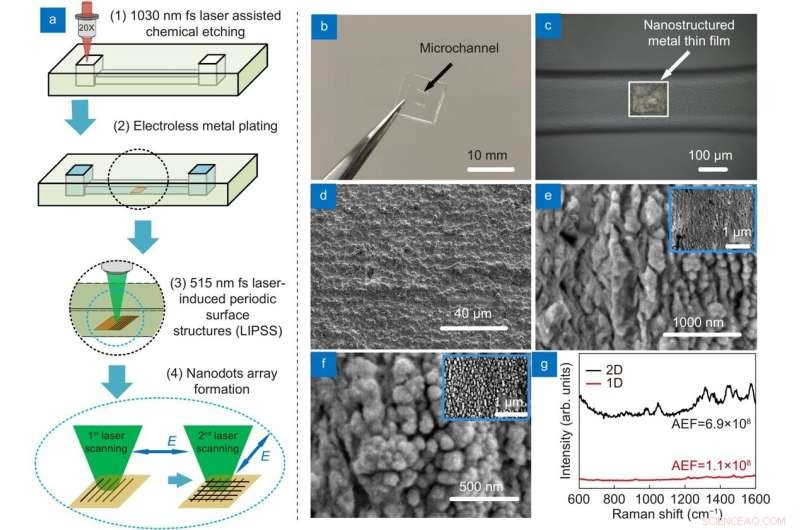
Figura 2. (a) Esquema de la fabricación (b) Fotografía del chip microfluídico SERS (c) Imagen de microscopio óptico que muestra el sustrato SERS. Imágenes SEM de (d) película de metal original, (e) ondas generadas por el primer escaneo láser y (f) nanopuntos generados por el segundo escaneo láser (Insertar:aumento bajo de la imagen SEM). ( g ) Espectros Raman de rodamina 6G (R6G) 10-9 M en sustratos SERS nanoestructurados 2-D (negro) y 1-D (rojo). Crédito:Compuscript Ltd
El equipo de investigación propuso LI-SERS, que logra un factor de mejora de SERS superior a 10 14 , mucho más alto que el método SERS normal. El chip microfluídico SERS presentaba un sustrato Ag-Cu SERS integrado en un microcanal de vidrio incrustado. El procesamiento láser híbrido de femtosegundos (fs) creó el microcanal de hierba.
El procesamiento láser híbrido fs permite la creación de estructuras 3D más complicadas con funcionalidades mejoradas para biochips, sensores y dispositivos microelectrónicos. Cuando la interfaz entre la solución de analito y el aire en el sustrato de SERS en el canal de microfluidos fue irradiada por el láser de excitación Raman, la intensidad de LI-SERS aumentó en seis órdenes de magnitud en comparación con SERS normal. El mecanismo de LI-SERS se atribuyó al efecto sinérgico del flujo de Marangoni inducido por la irradiación láser y el atrapamiento óptico. Esa irradiación láser dirigiría las moléculas del analito a los puntos calientes donde las moléculas recolectadas quedan atrapadas por la fuerza óptica. En consecuencia, las moléculas del analito se inmovilizaron en el sustrato SERS con el logro de una fuerte dispersión Raman.
Este estudio demostró que el método LI-SERS es aplicable para un uso más práctico. Es específicamente útil para la detección de trazas de biomoléculas sin etiquetas con grandes masas moleculares, incluidas bases de ADN, secuencias de ADN y β-amiloide (Aβ). Debido a la ultra alta sensibilidad y autoinmovilización de LI-SERS, se obtuvo discriminación de bases de ADN y secuencias de ADN con un límite de detección de 1 fM sin necesidad de tratamientos adicionales con agentes de acoplamiento o de entrecruzamiento. Además, la técnica LI-SERS puede detectar Aβ libre de etiquetas, un biomarcador de la enfermedad de Alzheimer, a niveles inferiores a 1 pM, y consiguiendo una correlación lineal entre la señal Raman y la concentración de Aβ en el rango de 1 nM-1 pM. La capacidad de biodetección sin etiquetas de LI-SERS ofrece un gran potencial para el diagnóstico de enfermedades en etapas tempranas en las clínicas.
En conclusión, los investigadores han proporcionado una descripción general del alcance del método LI-SERS para la detección de trazas de biomoléculas en chips SERS de microfluidos con especial referencia a la detección de ultratrazas de bases de ADN y Aβ. Se permitió que se formara una interfaz líquida en el microcanal. El flujo de Marangoni y los efectos de atrapamiento óptico inducidos por LI-SERS demostraron un límite de detección de 1 fM para bases de ADN sin etiquetas. Las características notables del método LI-SERS, incluida la sensibilidad ultraalta y la versatilidad asociadas con la recolección y la autoinmovilización de moléculas de analitos en los puntos calientes, serán beneficiosas para el diagnóstico de enfermedades en etapas tempranas, como infecciones virales y la enfermedad de Alzheimer. Nuevo método SERS desarrollado para capturar moléculas diana