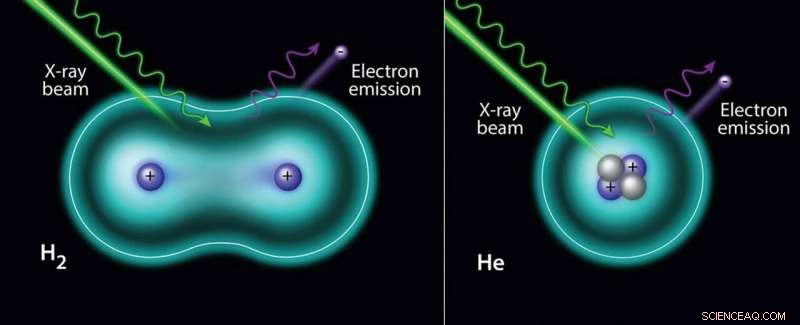
El haz de rayos X induce la fotoeyección de un electrón de hidrógeno (izquierda) y helio (derecha). Crédito:Departamento de Energía de EE. UU.
Por primera vez, los científicos midieron la estructura vibratoria de los átomos de hidrógeno y helio mediante rayos X. Los resultados refutan la idea errónea de que es imposible obtener espectros de espectroscopía de fotoelectrones de rayos X (XPS) de hidrógeno y helio, los dos elementos más ligeros de la tabla periódica. Se pensó que este era el caso debido a las bajas probabilidades de expulsión de electrones de estos elementos inducida por rayos X.
El brillo incomparable del rayo en la Fuente de Luz Nacional Sincrotrón II aumenta significativamente la probabilidad de que un fotón choque con un átomo de gas a presiones ambientales. La línea de luz permite utilizar XPS para estudiar directamente los dos elementos más abundantes del universo.
También, este trabajo ayuda a describir los límites de XPS, abriendo un campo más amplio para una de las técnicas más útiles en la ciencia de los materiales.
La espectroscopia de fotoelectrones de rayos X (XPS) es una de las técnicas más poderosas en la ciencia de los materiales. Sin embargo, la literatura está llena de afirmaciones que afirman que es imposible usar XPS para estudiar los dos elementos más ligeros y abundantes del universo, hidrógeno y helio.
Este trabajo demostró que se pueden obtener espectros de fotoelectrones de rayos X de presión ambiental de hidrógeno y helio cuando se utiliza una fuente de rayos X lo suficientemente brillante. como en el National Synchrotron Light Source II.
En el caso del gas helio, el espectro muestra un pico simétrico desde su único orbital. En el caso de moléculas de gas hidrógeno, se observa un pico asimétrico, que se relaciona con los diferentes modos vibracionales posibles del estado final. La estructura vibratoria de la molécula de hidrógeno es evidente en el H 2 Espectro de 1s.