Las reacciones químicas se describen comúnmente como transiciones de reactivos a productos. Sin embargo, tales reacciones involucran muchas moléculas, y las moléculas individuales sufren cambios estructurales frecuentes a medida que se transforman de reactivos a productos.
Incluso en las reacciones químicas más sencillas, los cambios reales observables que ocurren durante la reacción son mucho más rápidos y complejos de lo que se puede observar con cualquier tecnología existente, similar a cómo los objetos que se mueven rápidamente aparecen borrosos en fotografías tomadas con una velocidad de obturación lenta. .
Un equipo de investigación en Japón, dirigido por el profesor Tamiki Komatsuzaki en el Instituto de Diseño y Descubrimiento de Reacciones Químicas (ICReDD) de la Universidad de Hokkaido, ha desarrollado un marco que describe con precisión cómo aparecen las reacciones de primer orden dependiendo del intervalo de tiempo utilizado para medir la reacción. . Su trabajo fue descrito en la revista Proceedings of the National Academy of Sciences. .
"Durante una reacción, los átomos de los reactivos y productos sufren una serie de reordenamientos estructurales, o isomerización, hasta que la reacción se completa", explica Tamiki. "La velocidad a la que se producen estas isomerizaciones significa que normalmente sólo obtenemos una comprensión simplificada del proceso en un punto determinado, a través de un proceso llamado de grano grueso".
Yutaka Nagahata, primer autor del estudio, dice:"Formulamos un proceso de grano grueso que satisface las condiciones de 'agrupación exacta':la coincidencia exacta de una versión simplificada de una ecuación con su contraparte detallada original, una teoría propuesta durante medio siglo. hace, centrándose en los intervalos de observación, que pueden considerarse como la "velocidad de obturación" de una observación científica.
"Para adoptar esta coincidencia, formulamos un criterio para la indistinguibilidad del comportamiento estadístico de formas moleculares estables (isómeros) en función de la 'velocidad de obturación' de observación".
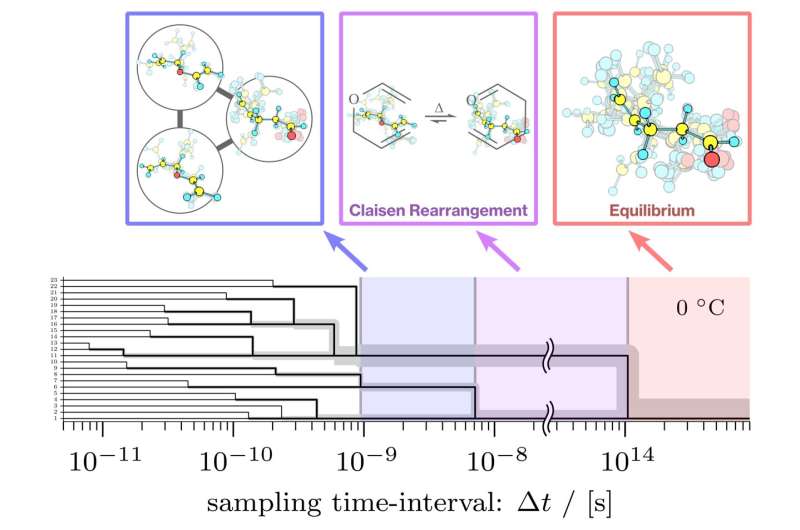
El equipo identificó intervalos de observación clave en los que diferentes formas moleculares "se desdibujan" y el sistema parece volverse más simple. Crearon un "diagrama sistemático" que muestra cómo el proceso de reacción parece cada vez más simplificado a medida que aumenta el intervalo de observación, y eventualmente aparece como un proceso de un solo paso (los reactivos se transforman directamente en productos) en largos intervalos de observación.
Utilizando este "diagrama sistemático", es posible determinar inmediatamente grupos indistinguibles y obtener la ecuación de tasas entre los grupos aplicando la agrupación exacta desarrollada.
"Al desarrollar la aproximación exacta, hemos superado las teorías de aproximación actuales, que contienen muchas omisiones que las hacen bastante inexactas", dice el profesor Mikito Toda de la Escuela de Graduados en Ciencias de la Información de la Universidad de Hyogo y coautor del estudio. estudio.
El equipo utilizó la reacción de reordenamiento de Claisen del alil vinil éter para demostrar que el grano grueso exacto podría explicar todas las rutas de reacción posibles. El trabajo futuro se centrará en ampliar este estudio a otras reacciones de primer orden. En última instancia, los investigadores esperan que su trabajo proporcione un respaldo matemático a la teoría del estado de transición.
Más información: Komatsuzaki, Tamiki, Una representación abarcada de jerarquías de escala de tiempo en una red de reacción de primer orden, Actas de la Academia Nacional de Ciencias (2024). DOI:10.1073/pnas.2317781121
Información de la revista: Actas de la Academia Nacional de Ciencias
Proporcionado por el Instituto de Diseño y Descubrimiento de Reacciones Químicas (ICReDD)