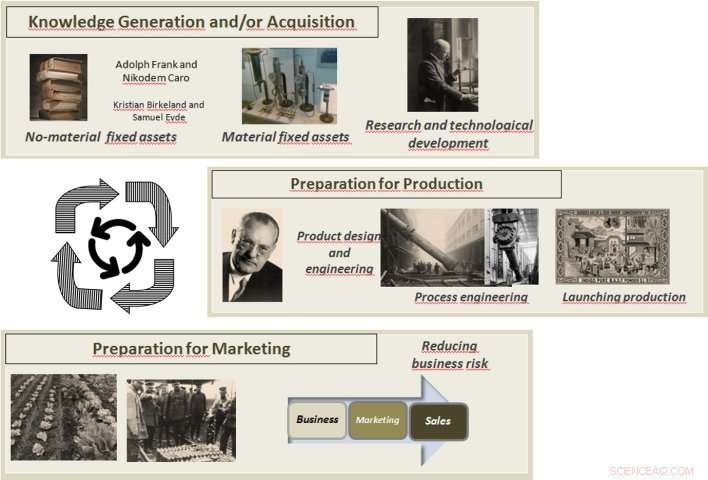
Adaptación de los pasos de innovación implicados en la síntesis de amoniaco. Crédito:A. Barona et al./ Sci. Ing. Ética (Fotos del Archiv der Max-Planck-Gesellschaft, Berlina
Además de ser un producto de limpieza muy conocido, el amoniaco es fundamental en la fabricación de fertilizantes. El proceso químico para sintetizar amoníaco apenas ha cambiado en 100 años, y sigue siendo imprescindible, aunque los científicos no saben cómo mitigar sus consecuencias negativas sobre el medio ambiente.
Cuando, durante el verano de 1909, el químico alemán Fritz Haber logró la síntesis de amoníaco a partir de nitrógeno e hidrógeno, Poco podía prever el enorme significado de su innovación. Años después, su compatriota Carl Bosch pudo producirlo a escala industrial utilizando catalizadores y reactores de alta presión.
Haber y Bosch, que fueron galardonados con el Premio Nobel por su investigación, dieron sus nombres al proceso de producción de amoníaco que se ha estado utilizando desde entonces. De hecho, el proceso Haber-Bosch es quizás la innovación más significativa del siglo XX.
Así lo recoge el estudio que investigadores de la Universidad del País Vasco han publicado en la revista Ética de la ciencia y la ingeniería , en el cual presentan una revisión histórica y detallan las tres actividades involucradas en cualquier proceso de innovación:adquisición y / o generación de conocimiento, producción industrial, y marketing.
"Cuando terminó la Primera Guerra Mundial, el amoníaco surgió como un producto químico insustituible para la producción de fertilizantes a gran escala, que contribuyó de manera decisiva al aumento de la producción de alimentos y la población mundial; y, incluso hoy, todavía dependemos de este proceso, "dice Astrid Barona, uno de los autores.
Pero a pesar de su importancia, el uso masivo de fertilizantes nitrogenados implica una gran paradoja. Por un lado, son fundamentales para asegurar la gran cantidad de alimento, pero en la otra mano, tienen un impacto negativo en el medio ambiente.
La razón es que el uso eficiente del nitrógeno que se emplea en la síntesis industrial de fertilizantes es muy pobre, lo que significa que la gran cantidad restante contribuye a la contaminación ambiental que causa la eutrofización del agua, pérdida de biodiversidad y alteración negativa del equilibrio atmosférico.
"Aunque el proceso Haber-Bosch, que consume mucha energía, no cumple con los requisitos actuales de sostenibilidad, no hay alternativa de reemplazo, "Barona dice, "y el equilibrio entre las necesidades humanas y los recursos naturales aún está pendiente".