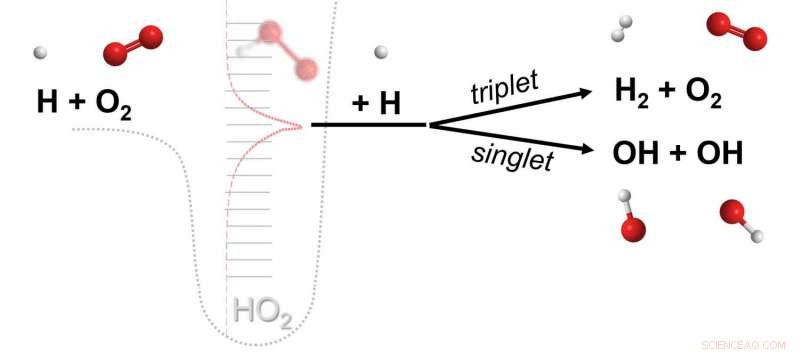
Una reacción química en la que tres moléculas diferentes (por ejemplo, H, O2, H) cada uno participa en la ruptura y formación de enlaces químicos. La reacción está mediada por un complejo de colisión efímero (HO2 **) formado por la colisión de dos moléculas (H, O2) que luego reacciona al chocar con una tercera molécula (H). Los datos de cálculos avanzados revelan que las reacciones de esta clase, hipotetizado hace casi un siglo y luego asumido que no es importante, son las principales vías químicas. Crédito:Michael P. Burke / Columbia Engineering
Un nuevo estudio dirigido por Michael P. Burke, profesor asistente de ingeniería mecánica en Columbia Engineering, ha identificado la importancia de una nueva clase de reacciones químicas que involucran a tres moléculas, cada una de las cuales participa en la ruptura y formación de enlaces químicos. La reacción de tres moléculas diferentes es posible gracias a un "complejo de colisión efímero, "formado por la colisión de dos moléculas, que vive lo suficiente como para chocar con una tercera molécula.
Esta cuarta clase, que los investigadores han denominado "reacciones químicamente termoleculares, "fue la primera hipótesis de Cyril Hinshelwood y Nikolay Semenov en sus estudios de reacciones en cadena en las décadas de 1920 y 1930 (ganaron el Premio Nobel de Química de 1956 por este trabajo). Durante décadas, Los investigadores han considerado que estas reacciones no son importantes, si es que ocurrieron, y hasta ahora, nadie los ha estudiado. Burke, que explora una variedad de problemas en la interfaz entre la química física fundamental y los dispositivos prácticos de ingeniería, decidió investigar estas reacciones después de darse cuenta de que las situaciones de combustión comunes, como los que se encuentran en muchos motores, tienen fracciones suficientemente altas de moléculas altamente reactivas conocidas como radicales libres para hacer posibles estas reacciones. El nuevo estudio se publica hoy en Química de la naturaleza .
"La combustión siempre ha sido un punto de partida para comprender todo tipo de otros mecanismos químicos, "dice Burke, quien también es miembro del Data Science Institute. "Potencialmente podría haber innumerables reacciones de esta nueva clase que impactan en cómo modelamos la química en fase gaseosa, desde diseñar nuevos tipos de motores hasta comprender la química planetaria responsable de las formaciones de nubes, cambio climático, evolución de contaminantes, incluso quizás la secuencia de reacciones que podrían afectar las condiciones para la vida extraterrestre. Nuestro descubrimiento abre un nuevo mundo de posibilidades ".
Por ejemplo, Los vehículos espaciales experimentan temperaturas muy altas y fracciones radicales en su descenso de regreso a la Tierra. Burke especula que esta cuarta clase de reacciones podría afectar el flujo de calor al vehículo, con implicaciones significativas para el diseño de sistemas de protección térmica para mantener seguros a los astronautas y / o cargas útiles cuando bajan a la Tierra.
Trabajando con Stephen J. Klippenstein, (División de Ingeniería y Ciencias Químicas, Laboratorio Nacional Argonne), Burke utilizó métodos computacionales de última generación, combinando cálculos químicos cuánticos que simulan la ruptura y formación de enlaces químicos entre moléculas que reaccionan con cálculos de transporte cinético que simulan las reacciones y los movimientos de los gases a granel que gobiernan el rendimiento de los dispositivos de ingeniería.
"El poder de estos métodos computacionales de última generación, "dice Burke, "es que pueden proporcionar una lente única en entornos químicos hostiles inadecuados para técnicas experimentales para estudiar la dinámica de reacción individual. Nuestros cálculos se basan en datos computacionales producidos a partir de primeros principios:la ecuación de Schrödinger, la ecuación fundamental de la mecánica cuántica. La combinación de estos datos con otros modelos basados en la física nos permite identificar directamente el impacto de una sola reacción entre muchas, de una manera que es muy difícil de hacer en el laboratorio ".
Usando métodos teóricos, incluidos los que desarrollaron para este estudio, Los investigadores demostraron que estas reacciones químicamente termoleculares (es decir, de tres moléculas) no solo son vías químicas importantes, sino que también impactan las velocidades de propagación de la llama. una medida de la reactividad global del combustible que rige el rendimiento, estabilidad, y eficiencia de muchos motores modernos.
La química de muchos sistemas, incluidas las atmósferas de combustión y planetarias, se rige por complejos mecanismos químicos, donde la conversión general de un conjunto de reactivos iniciales a un conjunto de productos finales pasa por muchas moléculas químicas intermedias con muchas reacciones químicas individuales que ocurren a nivel molecular. Nuestro conocimiento actual de los complejos mecanismos de combustión y atmósferas planetarias se ha basado en las clases de reacciones que se sabe que tienen lugar. Hasta ahora, solo se han considerado tres clases de reacciones:
El gas del baño generalmente se considera inerte, o no reactivo, molécula que no participa en ninguna ruptura o formación de enlaces, sino que quita algo de energía del otro complejo molecular (que tendría suficiente energía cinética interna para descomponerse espontáneamente si no se quitara energía).
Si en cambio el complejo molecular choca con una molécula reactiva, entonces la tercera molécula puede participar en el proceso de ruptura / formación de enlaces, produciendo lo que Burke y Klippenstein llaman un producto de "reacción químicamente termolecular". "En nuestro periódico, mostramos la importancia de las reacciones que involucran complejos H + O2 con otras especies de radicales, p.ej. H + O2 + H, en ambientes de combustión, ", señala." Sin embargo, dado el hecho de que las moléculas reactivas, como radicales libres y oxígeno molecular, son componentes principales en la combustión y ciertos entornos planetarios, existe un potencial significativo para que se produzcan otras reacciones termoleculares químicas y que desempeñen un papel importante en otros entornos ".
William H. Green, profesor de ingeniería química en el MIT, dice del estudio, "Se sabe desde hace mucho tiempo que muchas reacciones de asociación en fase gaseosa tienen tasas de eficacia muy bajas, debido a que el aducto energizado inicial no vive lo suficiente para ser estabilizado por la transferencia de energía por colisión, y simplemente se deshace de nuevo a los reactivos. Esto ha llevado al campo a pensar que estos aductos transitorios pueden ignorarse por completo. Este artículo revela que incluso si las reacciones unimoleculares de los aductos energizados son insignificantes, todavía pueden participar en reacciones bimoleculares, con consecuencias sorprendentemente importantes ".
Burke planea a continuación generalizar estas teorías y métodos para calcular las velocidades de reacción químicamente termoleculares para permitir cálculos similares en entornos de mayor presión, donde las colisiones entre moléculas son aún más frecuentes, importante para los diseños de motores de vanguardia. También explorará las implicaciones del hallazgo para otras reacciones y entornos químicos, como los implicados en la formación y reducción de contaminantes o la química de atmósferas planetarias.