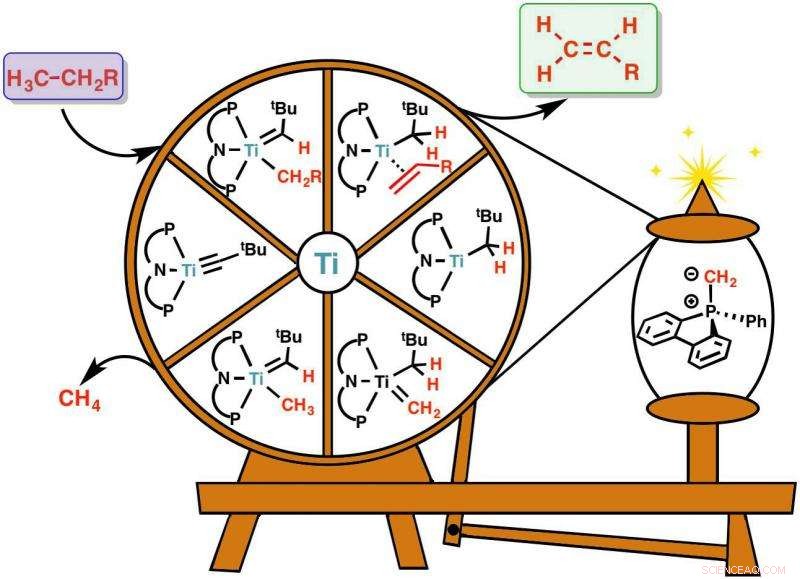
Representación de la reacción de ruptura carbono-hidrógeno con un husillo. Olefinas, es decir, moléculas con un doble enlace entre carbonos (C =C, caja verde) se generan a partir de moléculas no reactivas de gases naturales (caja violeta). La reacción incluye un catalizador basado en titanio (Ti) cuidadosamente elegido, representado por la rueda y una molécula aditiva, representada en el carrete. El aditivo ayuda a que la rueda gire, para reciclar el catalizador a su forma original, por lo que se puede volver a utilizar para facilitar otra reacción. Las olefinas son la materia prima química para una variedad de otras sustancias químicas, como los plásticos, polímeros conductores, medicamentos, etc. Esta reacción se puede realizar a bajas temperaturas y es la primera vez que se puede realizar de forma económica. Crédito:Instituto de Ciencias Básicas
¡Están a tu alrededor! La mayoría de los plásticos polímeros conductores, e incluso los medicamentos derivan de moléculas con un doble enlace entre dos átomos de carbono, C =C. Estas moléculas se denominan olefinas y se producen principalmente a partir de combustibles fósiles a través de un proceso contaminante y de gran consumo de energía conocido como craqueo al vapor. Requiere temperaturas de 800 ° C y produce dióxido de carbono, un gas de efecto invernadero. Innecesario hoy Las alternativas a este proceso que podrían traer beneficios ambientales y económicos son muy buscadas.
Un equipo de investigadores del Centro de Funcionalizaciones de Hidrocarburos Catalíticos, dentro del Instituto de Ciencias Básicas (IBS), en colaboración con el Prof.Daniel J. Mindiola de la Universidad de Pennsylvania, logró una reacción que antes no era posible; produjeron olefinas con ingredientes baratos fácilmente disponibles y a baja temperatura (75 ° C). Este resultado de la investigación, publicado en Química de la naturaleza , allana el camino para un uso eficiente de los gases naturales para sintetizar importantes productos químicos.
Gases naturales, como el metano y el etano, tienen fuertes enlaces carbono-hidrógeno (C-H) que son difíciles de romper. El equipo de investigación logró transformar esas moléculas no reactivas en olefinas, la materia prima química de una gran variedad de productos que utilizamos en nuestra vida diaria.
Este tipo de método de producción de olefinas se basa en la deshidrogenación, que es la eliminación de hidrógenos que conduce a la creación del enlace C =C, la marca de las olefinas. Dado que la energía requerida para romper los fuertes enlaces C-H es demasiado alta, la reacción solo se puede lograr con la ayuda de otras moléculas, llamados catalizadores. Previamente, la deshidrogenación solo era posible con catalizadores basados en metales caros, como el iridio.
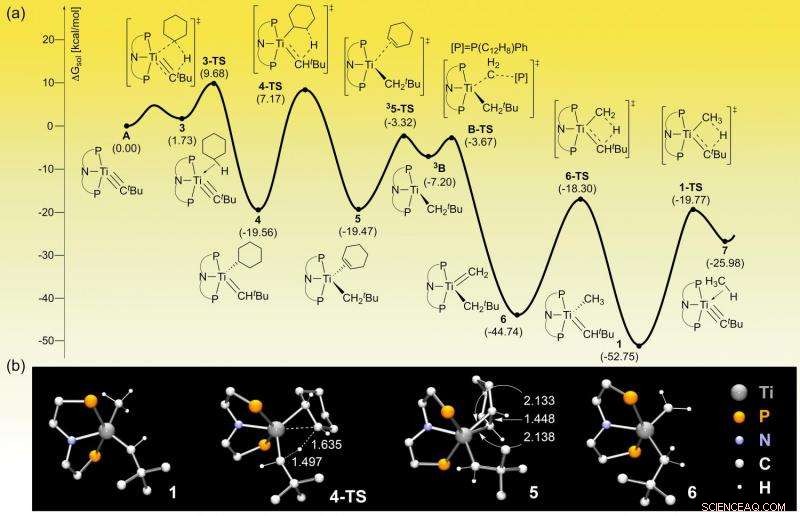
Perfil energético de la reacción generado por ordenador. Las simulaciones por computadora pueden predecir los componentes intermedios de la reacción química y cuánta energía se requiere para obtenerlos. Crédito:Instituto de Ciencias Básicas
El estudio logró la producción barata de olefinas gracias a un trabajo en equipo sinérgico entre informáticos y químicos experimentales. Simulando todo el proceso químico, Los químicos informáticos del IBS aconsejaron a sus colegas de la Universidad de Pensilvania sobre un catalizador barato a base de titanio para probar.
"Pasamos del iridio, que es tan raro y caro que está etiquetado como 'el elemento de los dioses', a un metal absolutamente barato, titanio; un elemento con el que todos estamos familiarizados, ya que se usa ampliamente como pigmento blanco para cerámica, papel, y blanqueador de dientes, "explica BAIK Mu-Hyun, el autor principal de IBS. "La simulación por computadora predice el movimiento de cada electrón y cómo las moléculas van a interactuar, por lo que nos permitió acortar el tiempo de desarrollo ".
Para resumir, el estudio demostró que fabricar olefinas de forma barata Es posible una forma energéticamente eficiente. La reacción se puede realizar a baja temperatura y el catalizador de titanio se puede reciclar parcialmente, por lo que se puede volver a utilizar para deshidrogenar más gas natural. El próximo desafío del equipo de investigación es hacer que el catalizador a base de titanio sea más eficiente.