
Los químicos de Brookhaven Lab, Ping Liu y José Rodríguez, ayudaron a caracterizar los detalles estructurales y mecánicos de un nuevo catalizador de baja temperatura para producir gas hidrógeno de alta pureza a partir de agua y monóxido de carbono. Crédito:Laboratorio Nacional Brookhaven
Los científicos han desarrollado un nuevo catalizador de baja temperatura para producir gas hidrógeno de alta pureza y, al mismo tiempo, utilizar monóxido de carbono (CO). El descubrimiento descrito en un artículo que se publicará en línea en la revista. Ciencias el jueves, 22 de junio, 2017:podría mejorar el rendimiento de las pilas de combustible que funcionan con combustible de hidrógeno pero que pueden envenenarse con CO.
"Este catalizador produce una forma más pura de hidrógeno para alimentar la celda de combustible, "dijo José Rodríguez, químico del Laboratorio Nacional Brookhaven del Departamento de Energía de EE. UU. (DOE). Rodríguez y sus colegas de la División de Química de Brookhaven, Ping Liu y Wenqian Xu, se encontraban entre el equipo de científicos que ayudaron a caracterizar los detalles estructurales y mecánicos del catalizador. que fue sintetizado y probado por colaboradores de la Universidad de Pekín en un esfuerzo dirigido por el profesor de química Ding Ma.
Debido a que el catalizador opera a baja temperatura y baja presión para convertir agua (H2O) y monóxido de carbono (CO) en gas hidrógeno (H2) y dióxido de carbono (CO2), también podría reducir el costo de ejecutar esta reacción llamada "cambio de gas de agua".
"Con baja temperatura y presión, el consumo de energía será menor y la configuración experimental será menos costosa y más fácil de usar en entornos pequeños, como pilas de combustible para coches, "Dijo Rodríguez.
La conexión de oro-carburo
El catalizador consta de grupos de nanopartículas de oro en capas sobre un sustrato de carburo de molibdeno. Esta combinación química es bastante diferente de los catalizadores a base de óxidos utilizados para impulsar la reacción de cambio de gas de agua en las instalaciones industriales de producción de hidrógeno a gran escala.
"Los carburos son más reactivos químicamente que los óxidos, "dijo Rodríguez, "y la interfaz de oro-carburo tiene buenas propiedades para la reacción de cambio de gas de agua; interactúa mejor con el agua que los metales puros".
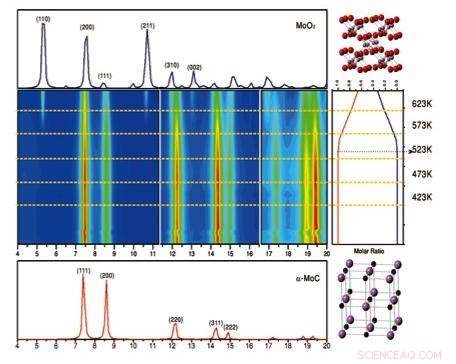
Wenqian Xu y José Rodríguez de Brookhaven Lab y Siyu Yao, entonces estudiante en la Universidad de Pekín pero ahora investigador postdoctoral en Brookhaven, realizó estudios operando de difracción de rayos X del catalizador de oro-molibdeno-carburo en un rango de temperaturas (423 Kelvin a 623K) en la Fuente de Luz Nacional Sincrotrón (NSLS) en Brookhaven Lab. El estudio reveló que a temperaturas superiores a 500 K, el carburo de molibdeno se transforma en óxido de molibdeno, con una reducción de la actividad catalítica. Crédito:Laboratorio Nacional Brookhaven
"El grupo de la Universidad de Pekín descubrió un nuevo método sintético, y eso fue un gran avance, ", Dijo Rodríguez." Encontraron una manera de obtener una fase específica, o configuración de los átomos, que es muy activa para esta reacción ".
Los científicos de Brookhaven jugaron un papel clave en descifrar las razones de la alta actividad catalítica de esta configuración. Rodríguez, Wenqian Xu, y Siyu Yao (entonces estudiante en la Universidad de Pekín pero ahora investigador postdoctoral en Brookhaven) realizaron estudios estructurales utilizando difracción de rayos X en la Fuente de Luz Nacional Sincrotrón (NSLS) mientras el catalizador operaba en condiciones industriales o técnicas. Estos experimentos de operando revelaron detalles cruciales sobre cómo cambió la estructura bajo diferentes condiciones de operación, incluso a diferentes temperaturas.
Con esos detalles estructurales en la mano, Zhijun Zuo, profesor invitado en Brookhaven de la Universidad de Tecnología de Taiyuan, Porcelana, y el químico de Brookhaven Ping Liu ayudaron a desarrollar modelos y un marco teórico para explicar por qué el catalizador funciona como lo hace, utilizando recursos computacionales en el Centro de Nanomateriales Funcionales (CFN) de Brookhaven.
"Modelamos diferentes interfaces de oro y carburo de molibdeno y estudiamos el mecanismo de reacción para identificar exactamente dónde tienen lugar las reacciones:los sitios activos donde los átomos se unen, y cómo se rompen y reforman los lazos, " ella dijo.
Estudios adicionales en el Centro de Ciencias de Materiales Nanofásicos del Laboratorio Nacional de Oak Ridge (CNMS), la fuente de luz avanzada (ALS) en el Laboratorio Nacional Lawrence Berkeley, y dos instalaciones de investigación de sincrotrón en China contribuyeron al conocimiento de los científicos.
"Esta es una reacción compleja de varias partes, "dijo Liu, pero señaló un factor esencial:"La interacción entre el oro y el sustrato de carburo es muy importante. El oro generalmente une las cosas muy débilmente. Con este método de síntesis conseguimos una adherencia más fuerte del oro al carburo de molibdeno de forma controlada".
Esa configuración estabiliza el intermedio clave que se forma a medida que avanza la reacción, y la estabilidad de ese intermedio determina la tasa de producción de hidrógeno, ella dijo.
El equipo de Brookhaven continuará estudiando este y otros catalizadores de carburo con nuevas capacidades en National Synchrotron Light Source II (NSLS-II), una nueva instalación que abrió en Brookhaven Lab en 2014, reemplazando NSLS y produciendo rayos X que son 10, 000 veces más brillante. Con estas radiografías más brillantes, los científicos esperan capturar más detalles de la química en acción, incluyendo detalles de los intermedios que se forman a lo largo del proceso de reacción para validar las predicciones teóricas hechas en este estudio.