La activación excesiva de los inflamasomas se asocia con diversas enfermedades, como la gota, la enfermedad de Alzheimer, la aterosclerosis y la diabetes tipo 2. Dado el papel fundamental de los macrófagos tanto en la activación del inflamasoma como en la fagocitosis de nanopartículas, el descubrimiento de nanopartículas antiinflamatorias dirigidas específicamente a los macrófagos podría modular de manera más efectiva la respuesta inflamatoria y al mismo tiempo minimizar los efectos no deseados en otros tipos de células.
Sin embargo, se ha descubierto que la mayoría de los nanomateriales reportados actualmente promueven en lugar de inhibir la activación del inflamasoma.
Un estudio publicado en la revista National Science Review demostraron que los nanocristales de aleación de níquel-cobalto exhiben una eficacia notable en la supresión de la activación de tres inflamasomas, a saber, NLRP3, NLRC4 y AIM2, en macrófagos primarios. Posteriormente, los investigadores emplearon dos modelos de enfermedad, colitis y peritonitis aguda, para evaluar el impacto de los nanocristales de aleación de níquel-cobalto en el tratamiento de la sobreactivación del inflamasoma.
Los hallazgos revelaron que los nanocristales de aleación de níquel-cobalto mejoraron eficazmente los síntomas de la enfermedad en ratones en el modelo de colitis, incluida la mitigación de la pérdida de peso, la restauración de la longitud del colon y el alivio del daño al epitelio de la mucosa intestinal. Además, en el modelo de peritonitis aguda, estos nanocristales atenuaron significativamente la quimiotaxis de los neutrófilos dentro de la cavidad peritoneal de los ratones.
Para confirmar si los nanocristales de aleación de níquel-cobalto requieren internalización celular para ejercer sus efectos antiinflamatorios, los autores realizaron experimentos utilizando un inhibidor de la endocitosis ampliamente utilizado, la citocalasina D. El tratamiento con citocalasina D redujo significativamente la internalización de los nanocristales de aleación de níquel-cobalto por parte de los macrófagos.
Además, la inhibición de la internalización de los nanocristales por los macrófagos condujo a una disminución de sus efectos antiinflamatorios, lo que indica que la acción antiinflamatoria de los nanocristales de aleación de níquel-cobalto depende de su absorción celular.
Para investigar si los efectos antiinflamatorios de los nanocristales de aleación de níquel-cobalto se atribuyen a su morfología geométrica o composición elemental, los autores sintetizaron nanopartículas de níquel y nanopartículas de cobalto en condiciones idénticas a las de los controles, que exhibieron morfologías distintas en comparación con los nanocristales de aleación de níquel-cobalto. . Sin embargo, tanto las nanopartículas de níquel como las nanopartículas de cobalto también inhibieron significativamente la activación del inflamasoma.
Por lo tanto, los autores atribuyeron el efecto inhibidor de los nanocristales de aleación de níquel-cobalto a la composición elemental más que a su forma geométrica. Estos hallazgos sugieren que los nanomateriales que contienen níquel y cobalto pueden ofrecer oportunidades para diseñar nanofármacos con propiedades antiinflamatorias.
Revelar los mecanismos biológicos que subyacen a la acción de los nanomateriales es crucial para sus posibles aplicaciones médicas. Sin embargo, dilucidar el mecanismo biológico mediante el cual estos nanocristales antiinflamatorios de amplio espectro inhiben la activación del inflamasoma plantea desafíos importantes utilizando enfoques experimentales biológicos convencionales.
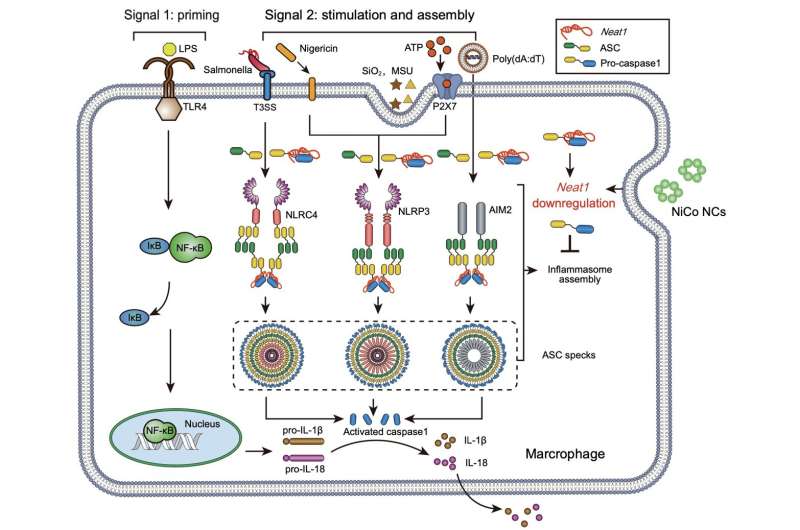
Para abordar esto, los investigadores realizaron la secuenciación del ARN y el ensayo de cromatina accesible a transposasa con secuenciación (ATAC-Seq), lo que llevó a la identificación de un ARN no codificante previamente informado, Neat1, que se sabe que está involucrado en el ensamblaje del inflamasoma. Tras el tratamiento con nanocristales de aleación de níquel-cobalto, la expresión de Neat1 se redujo significativamente.
Estudios anteriores han demostrado que la regulación negativa de la expresión de Neat1 por sí sola inhibe significativamente la activación de los inflamasomas NLRP3, NLRC4 y AIM2. Los resultados de ATAC-Seq revelaron una reducción significativa en la accesibilidad a la cromatina del cuerpo del gen y las regiones promotoras de Neat1 en el grupo tratado con nanocristales de aleación de níquel-cobalto, lo que sugiere que la inhibición de la activación del inflamasoma por los nanocristales de aleación de níquel-cobalto se logra a través de la supresión de la transcripción de Neat1 en lugar de promover su degradación.
Este estudio fue realizado en colaboración por el Dr. Shu-Hong Yu, el Dr. Long-Ping Wen y el Dr. Kun Qu de la Universidad de Ciencia y Tecnología de China, junto con el profesor Yang Lu de la Universidad Tecnológica de Hefei.
Más información: Jun Lin et al, Los nanocristales de aleación de níquel-cobalto inhiben la activación de los inflamasomas, National Science Review (2023). DOI:10.1093/nsr/nwad179
Proporcionado por Science China Press