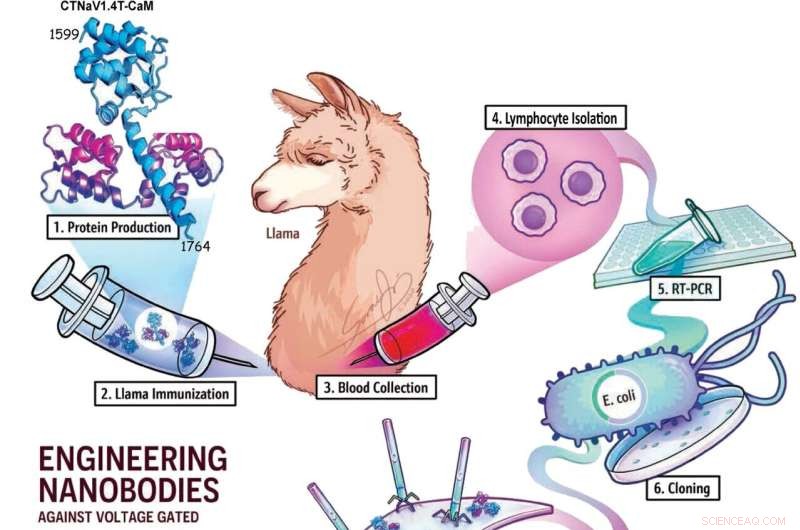
Resumen gráfico. Crédito:Sora Ji
En experimentos de "prueba de concepto" con células y tejidos humanos y de ratón, los investigadores de Johns Hopkins Medicine afirman que han diseñado proteínas diminutas, llamadas nanocuerpos, derivadas de anticuerpos de llama, que podrían usarse para administrar medicamentos dirigidos a las células musculares humanas. Los investigadores dicen que la capacidad de apuntar con mayor precisión a dichos tejidos podría avanzar en la búsqueda de formas más seguras y eficientes de aliviar el dolor durante la cirugía, tratar los ritmos cardíacos irregulares y controlar las convulsiones.
Los resultados de los experimentos se publicaron el 21 de febrero en el Journal of Biological Chemistry .
Los nanocuerpos son versiones pequeñas de proteínas llamadas anticuerpos que marcan patógenos potenciales para que el sistema inmunitario los destruya. Los científicos no saben por qué existen solo en algunas especies, como los camélidos y los tiburones, pero desde su descubrimiento en la década de 1980, los investigadores los han estudiado para usarlos como herramienta de investigación y sistema de administración de medicamentos contra el cáncer con resultados mixtos.
Conscientes de tales experimentos, los investigadores de Johns Hopkins sospecharon que los nanocuerpos podrían ser útiles como herramienta para unirse a los canales de iones de sodio de una célula, que actúan como una especie de interruptor que puede conducir señales químicas que encienden o apagan las células musculares.
En el cuerpo humano aparecen nueve variedades de estos interruptores, cada uno específico de un tipo de tejido, como un músculo o un nervio. Debido a que las proteínas del canal solo tienen pequeñas diferencias entre sí, la mayoría de los medicamentos no pueden diferenciarlas, lo que presenta riesgos de seguridad cuando se intenta usar con fármacos como los anestésicos. Los medicamentos existentes, dicen los investigadores, bloquean el dolor y sedan a un paciente al "apagar" los canales de iones de sodio en los nervios y el músculo esquelético, pero también pueden reducir peligrosamente la frecuencia cardíaca e interferir con los ritmos cardíacos.
Otros estudios, dicen los investigadores de Johns Hopkins Medicine, han demostrado que los nanocuerpos se pueden usar para transportar una carga, una capacidad que podría impulsar los esfuerzos para administrar medicamentos a canales de iones de sodio específicos, eliminando tales efectos secundarios.
"Esta es la razón por la cual los médicos y las compañías farmacéuticas están interesados en encontrar medicamentos que puedan modular estos canales, ya sea para activarlos o desactivarlos, de manera distinta", dice Sandra Gabelli, Ph.D., profesora asociada de medicina en la Facultad de Medicina de la Universidad Johns Hopkins. .
Gabelli reconoció que el pequeño tamaño de los nanocuerpos podría permitirles unirse a áreas que son inaccesibles para moléculas más grandes, como anticuerpos más grandes que a menudo se usan para aplicaciones similares.
En sus experimentos de prueba de concepto, el equipo de investigación de Gabelli analizó una gran biblioteca de 10 millones de nanocuerpos para desarrollarlos como proteínas biológicas que podrían diferenciar potencialmente entre los canales de iones de sodio en los músculos y los de los nervios.
En colaboración con Manu Ben-Johny de la Universidad de Columbia, los investigadores adhirieron una molécula "reportera" fluorescente a los nanocuerpos que se ilumina cuando interactúa con el canal de sodio. Al monitorear el brillo, los investigadores encontraron que dos nanocuerpos, Nb17 y Nb82, se unieron a los canales de iones de sodio que son específicos del músculo esquelético y del corazón.
Los investigadores también probaron la estabilidad de los nanocuerpos a diferentes temperaturas, un factor clave en el desarrollo y suministro de fármacos a las clínicas. El equipo de investigación descubrió que los nanocuerpos Nb17 y Nb82 eran resistentes a temperaturas de hasta 168,8 y 150,8 grados Fahrenheit, respectivamente, lo que indica que estos nanocuerpos permanecerían estables en condiciones normales.
A continuación, los investigadores planean obtener imágenes del nanocuerpo y los canales de iones de sodio unidos para revelar más sobre cómo funciona esta interacción. Los anticuerpos de llama en miniatura podrían ayudar a combatir las variantes del SARS-CoV-2