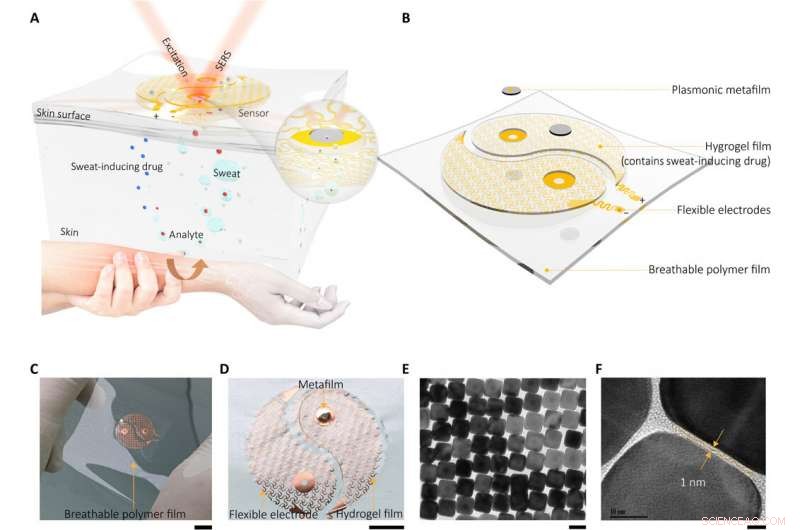
Dispositivo sensor SERS portátil integrado con metamaterial plasmónico. (A) Dibujo esquemático que muestra el principio de funcionamiento y el diseño del dispositivo, (B) que constaba de dos componentes principales (componente de extracción de sudor y componente de detección de SERS) y estaba diseñado para que pareciera un símbolo de yin-yang. La figura insertada destaca la interfaz de detección clave cerca del metafilm. (C) Imagen óptica del dispositivo y (D) imagen óptica ampliada del componente de extracción de sudor. Una fina capa de hidrogel cargada con moléculas (cloruro de acetilcolina) que estimulan las secreciones de las glándulas sudoríparas está montada en el electrodo de malla fractal en espiral. Tenga en cuenta que para resaltar el contraste para la exposición, sólo uno de los electrodos se montó con la capa de hidrogel y la metafilm plasmónica. Crédito de la foto:Yingli Wang, Universidad de Zhejiang. (E y F) Imágenes de microscopía electrónica de transmisión (TEM) de alta resolución del componente sensor SERS montado en el centro del electrodo, que es la metapelícula plasmónica formada por una superrejilla de nanocubos de plata (NC) ordenada. Barras de escala, 1 cm (C), 5 mm (profundidad), 50 nm (E), y 5 nm (F). Crédito:Science Advances, doi:10.1126 / sciadv.abe4553
La tecnología de detección portátil es un vínculo esencial en la medicina personalizada, donde los investigadores deben rastrear múltiples analitos dentro del cuerpo simultáneamente, para obtener una imagen completa de la salud humana. En un nuevo informe sobre Avances de la ciencia , Yingli Wang y un equipo de científicos en biosistemas, ingeniería y ciencias de la información en la Universidad de Cambridge y la Universidad de Zhejiang en el Reino Unido y China, presentó un sensor electrónico plasmónico portátil con capacidad de reconocimiento molecular "universal". El equipo introdujo metasuperficies plasmónicas flexibles con actividad de dispersión Raman mejorada en la superficie (SERS) como componente de detección fundamental. El sistema contenía un proceso de extracción de sudor flexible para extraer de forma no invasiva y tomar huellas dactilares de los analitos dentro del cuerpo en función de sus espectros de dispersión Raman únicos. Como prueba de concepto, controlaron con éxito cantidades variables de trazas de fármacos dentro del cuerpo para obtener un perfil metabólico de fármacos individual. El sensor cubrió la brecha en la tecnología de detección portátil para proporcionar un universal, proceso de seguimiento molecular sensible para evaluar la salud humana.
Tecnología de sensor portátil
Wang y col. presentó una plataforma de detección integrada electrónica plasmónica portátil con una capacidad de reconocimiento casi "universal". La detección portátil proporciona un vínculo con el futuro de la medicina personalizada, pero tales sensores deben superar un desajuste fundamental entre una superficie elástica rígida y blanda para laminar en biointerfaces como la piel, ojo, nervio y diente para evaluar sin problemas la salud humana. Los dispositivos permiten a los investigadores evaluar continuamente los signos vitales, incluida la frecuencia cardíaca y la temperatura corporal, transpiración y actividades físicas. A pesar del éxito de los sensores físicos portátiles, Aún no se han realizado técnicas de seguimiento de moléculas no invasivas que proporcionen información sobre la dinámica del cuerpo humano a nivel molecular. Estas capacidades son vitales para la medicina de precisión personalizada. En este caso, Wang y col. tenía como objetivo desarrollar una nueva estrategia con especificidad de objetivo universal en lugar de tener un objetivo solo para realizar un seguimiento simultáneo de varios objetivos. El equipo desarrolló una nueva plataforma utilizando una metasuperficie plasmónica activa de espectroscopia Raman mejorada en superficie flexible (SERS) para que sirva como el componente de detección clave y un sistema electrónico flexible para extraer automáticamente el sudor y los analitos del cuerpo.
Caracterización del componente sensor SERS del dispositivo. (A) Ilustración esquemática que muestra el principio de detección SERS de la metafilm NC. Los analitos en el sudor extraído se llevaron al punto de acceso EM en la metafilm NC desde la parte inferior, que puede detectarse in situ mediante la técnica SERS a partir de la metafilm del reverso (excitación y recogida hacia atrás). (B) Simulación FDTD de la mejora del campo eléctrico local para el punto de acceso EM en la metasuperficie NC. (C) Espectros SERS de la metafilm NC sumergida en la solución de la molécula sonda (CV) con varias concentraciones (un promedio de 20 ubicaciones seleccionadas al azar para cada concentración con un tiempo de adquisición de 1 s y utilizando un objetivo de 10 × y una potencia láser de 0,33 mW). (D) Mapa de intensidad Raman (~ 1621 cm − 1) de la metafilm NC después del tratamiento con la sonda Raman (CV, 10-5 M). (E) Comparación de las respuestas de SERS (~ 1621 cm − 1) a varias soluciones de CV utilizando enfoques de recopilación hacia atrás y hacia adelante. (F) Espectros SERS de las muestras de sudor humano que contienen diferentes fármacos (lidocaína 0,2 M, 10-3 M de cocaína, y metotrexato 10−5 M) y la muestra de sudor en blanco (utilizando un objetivo de 10 × o 50 × y un láser de potencia de 0,15 a 0,66 mW, con tiempos de adquisición de 6 a 30 s). Crédito:Science Advances, doi:10.1126 / sciadv.abe4553 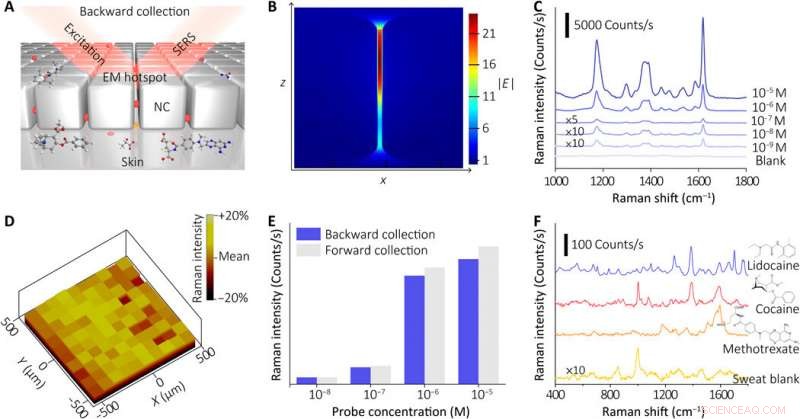
El equipo tomó las huellas digitales del espectro único de SERS utilizando el sensor portátil. Como prueba de concepto, detectaron la variación de las concentraciones de fármacos en el cuerpo humano para obtener el perfil metabólico de fármacos de un individuo. El sensor portátil integrado cubrió la brecha existente en el diagnóstico personalizado para el seguimiento en tiempo real de importantes compuestos bioquímicos. Los científicos utilizaron la plataforma de detección para monitorear señales fisiológicas o concentraciones de fármacos en el cuerpo humano para obtener el perfil metabólico de fármacos de un individuo. Luego, usando el sensor portátil integrado, controlaron las señales fisiológicas o las concentraciones de fármacos en un sistema de suministro de fármacos de retroalimentación de circuito cerrado.
El dispositivo sensor portátil integrado con metamaterial plasmónico contenía dos componentes principales, incluida una fina capa de hidrogel cargada con moléculas para estimular las secreciones de las glándulas sudoríparas. El equipo adjuntó estas construcciones a dos electrodos de malla fractal en espiral para que sirvan como componente de extracción de sudor. Wang y col. utilizó el proceso de iontoforesis (administración transdérmica de fármacos) para esta extracción; ampliamente utilizado como método de muestreo de sudor no invasivo en dispositivos con fines diagnósticos y terapéuticos. Formaron una metapelícula plasmónica usando una superrejilla de nanocubos de plata ordenados para servir como el componente sensor montado en la configuración experimental. Los fuertes campos electromagnéticos localizados en el nanocubo dieron lugar al efecto SERS (dispersión Raman mejorada en la superficie) para detectar moléculas que se acercan a la superficie de la metafilm. Colocaron los dos componentes en una delgada película de polímero de módulo ultrabajo para formar una delgada Soporte transpirable y físicamente resistente para una adhesión cutánea no irritante. Usando los electrodos, El equipo aplicó una corriente eléctrica suave para administrar cloruro de acetilcolina en la capa de hidrogel a las glándulas sudoríparas secretoras para un rápido, Generación de sudor localizada.
Características mecánicas del dispositivo. (A) Imágenes ópticas del sensor deformado. (B) Análisis de distribución de deformación FEM del área del anillo de protección del electrodo estirable bajo varias distorsiones, indicando que el anillo de protección puede aislar grandes deformaciones al elastómero blando, evitando así deformaciones plásticas potencialmente destructivas para el componente sensor de SERS. (C) Respuestas SERS del sensor bajo diversas deformaciones. (D) Características del sensor SERS después de la prueba de estiramiento cíclico. (E) Cambios de resistencia en el electrodo bajo diversas deformaciones. (F) Cambios de resistencia en el electrodo después de la prueba de estiramiento cíclico. (G) Fotografías del sensor montado en piel humana y (H) en diversas condiciones. Crédito de la foto:Xiangjiang Liu, Universidad de Zhejiang. Barras de escala, 1 mm (B) y 1 cm (G y H). Las barras de error se definen como ± SD. Crédito:Science Advances, doi:10.1126 / sciadv.abe4553 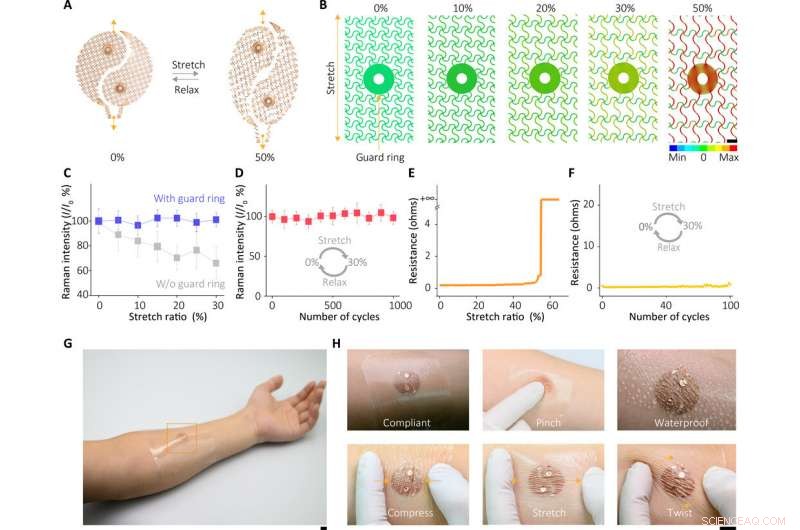
El sensor del dispositivo portátil dependía del efecto SERS generado por la metapelícula de superrejilla de nanocubos de plata ordenada, en base a lo cual el equipo detectó el objetivo de interés en el sudor extraído. En primer lugar, ensamblaron una sola capa de la matriz de nanocubos empaquetados cerrados en la interfaz líquido / aire y, posteriormente, transformaron la construcción en un soporte de polímero delgado y flexible. Luego, los científicos verificaron el tamaño promedio de la brecha entre los nanocubos utilizando imágenes de microscopía electrónica de transmisión (TEM) de alta resolución y realizaron simulaciones numéricas de dominio de tiempo de diferencia finita (FDTD). La distensibilidad mecánica y el contacto con la piel de la metafilm permitieron mediciones de alta fidelidad. Luego, el equipo desarrolló la película SERS y la transfirió a un hidrogel cargado con un agente agonista unido a electrodos de malla fractal. Utilizaron un diseño en espiral ultradelgado para aumentar la tolerancia del sistema inductor de sudor a las deformaciones mecánicas y lo lograron desarrollando una etapa de diseño de "isla interconectada" para formar una película SERS quebradiza con un sistema electrónico suave y elástico. El equipo confirmó la durabilidad de la electrónica después de 100 ciclos de prueba. sin ninguna degradación de señal observable para cumplir perfectamente con las funciones requeridas de un sensor portátil.
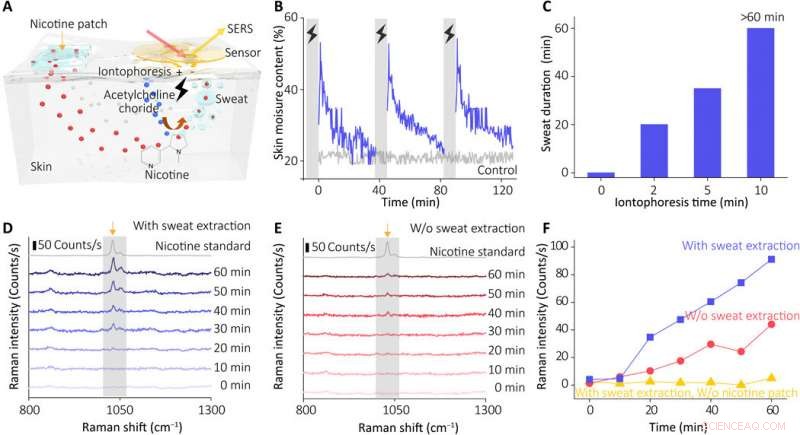
Rendimiento de detección in vivo de nuestro sensor. (A) Ilustración esquemática que muestra el principio de funcionamiento del sistema de extracción de sudor. (B) Variación en el contenido de humedad de la piel después de la inducción periódica del sudor (usando el hidrogel que contiene 10% de cloruro de acetilcolina, corriente de iontoforesis de 0,5 mA durante 5 min). (C) Características de secreción de sudor inducida en respuesta a diferentes tiempos de iontoforesis (0 a 10 min). La duración de la secreción representa el tiempo total de conductancia de la piel por encima de la línea de base (las mediciones se detuvieron a los 60 minutos). (D) Monitoreo en tiempo real de la nicotina en la piel humana usando nuestro sensor integrado (con extracción de sudor) y grupos de control (E) (sin encender la corriente de iontoforesis para la extracción de sudor). Los espectros se recogieron utilizando una potencia láser de 0,33 mW y un objetivo de 10 × (tiempo de adquisición, 1 s). (F) Evolución del pico Raman característico de nicotina después de la extracción de sudor del grupo de prueba y del grupo de control (sin encender la corriente o sin colocar el parche de nicotina). Crédito:Science Advances, doi:10.1126 / sciadv.abe4553
Aplicación de detección biológica
Wang y col. Luego reclutó voluntarios sanos para mediciones in vivo (fisiológicas) para demostrar la capacidad de extracción de sudor del dispositivo. Los científicos utilizaron la nicotina como fármaco modelo y controlaron la concentración real del fármaco en la piel en relación con la administración del fármaco. absorción y tasa metabólica por individuo. Durante los experimentos, utilizaron un sensor SERS portátil acoplado a una fuente de alimentación compacta y una unidad de control inalámbrica en el antebrazo de los voluntarios. El dispositivo mostró el espectro SERS de nicotina en el sudor para coincidir con el espectro del estándar de nicotina. Los resultados indicaron cómo el sensor entrenaba el comportamiento metabólico de la nicotina para permitir la capacidad del sensor portátil de monitorear la farmacocinética dinámica de los medicamentos y su perfil metabólico. El sensor sin embargo, sólo los objetivos detectados de forma eficaz almacenados en la subepidermis poco profunda; por lo tanto, los investigadores deberán comprender cómo este valor se correlaciona con las concentraciones de fármaco en la sangre o en el líquido intersticial durante más estudios.
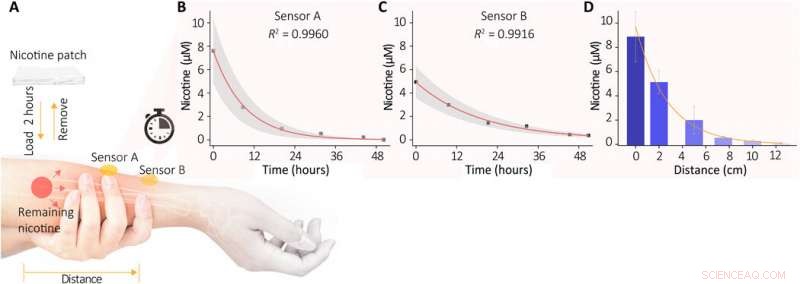
Monitorización in vivo del proceso de metabolización de la nicotina en la piel humana. (A) Ilustración esquemática del experimento. Se colocó un parche de nicotina que contenía ~ 10 mg en el antebrazo de los voluntarios durante 2 horas y luego se retiró. Después de que la piel se haya limpiado a fondo, la nicotina restante en la piel fue extraída y analizada por nuestro sensor. (B y C) Se midieron las evoluciones de las concentraciones de nicotina restantes en las dos ubicaciones (el sensor A directamente en el área parcheada; el sensor B está conectado a unos 2 cm de distancia). Cada medición se tomó después de 20 min de extracción de sudor (corriente de iontoforesis de 0,5 mA, Hidrogel cargado con cloruro de acetilcolina al 10%), y se recogieron continuamente las respuestas del sensor de los siguientes 10 minutos. Los niveles de nicotina promedio obtenidos se muestran en la figura. Las áreas de sombra indican ± SD de las mediciones. (D) Dependencia de la distancia de las concentraciones de nicotina en el sudor extraído después del parche. Se colocaron seis sensores a lo largo del brazo a una distancia de 0 a 12,5 cm del área de parche. Crédito:Science Advances, doi:10.1126 / sciadv.abe4553
panorama
De este modo, Yingli Wang y sus colegas mostraron un sensor integrado plasmónico-electrónico portátil como un dispositivo portátil de próxima generación. En comparación con los sensores electroquímicos portátiles existentes, este sensor mostró una especificidad de objetivo más amplia y una mayor estabilidad. El dispositivo integrado cubrió la brecha existente en el diagnóstico personalizado y la medicina de precisión para rastrear moléculas importantes dentro del cuerpo en tiempo real. El equipo propuso aplicaciones para monitorear señales fisiológicas y concentraciones de fármacos en un sistema de suministro de fármacos de retroalimentación de circuito cerrado y espera que el sensor portátil inspire una variedad de aplicaciones multidisciplinarias.
© 2021 Science X Network