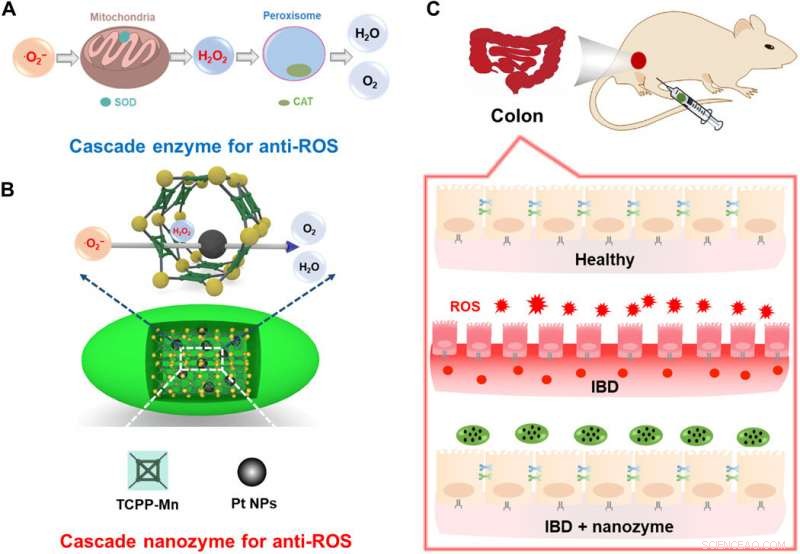
Ilustración esquemática del diseño de una nanozima integrada con actividad anti-ROS en cascada para la terapia de la EII. (A) Enzimas en cascada celular para anti-ROS. La eficacia terapéutica de tal sistema es limitada debido a las diferentes ubicaciones subcelulares de las enzimas SOD y CAT y la estabilidad extracelular limitada. (B) Construcción de una nanozima en cascada para la terapia anti-ROS mediante la incorporación de NP de Pt dentro de PCN222-Mn MOF. La proximidad a nanoescala de los sitios catalíticos activos promueve las reacciones en cascada. (C) La EII de los ratones se puede aliviar eficazmente mediante el tratamiento con la nanozima en cascada integrada. Crédito:Science Advances, doi:10.1126 / sciadv.abb2695
En un informe reciente, Yufeng Liu y un equipo de investigadores interdisciplinarios en China desarrollaron una cascada de nanozimas integradas para eliminar el exceso de especies reactivas de oxígeno (ROS; radicales libres de oxígeno). La nanozima imitaba a la superóxido dismutasa (un grupo de enzimas) e incorporó una estructura organometálica (MOF) a base de manganeso (Mn) para transformar los radicales de oxígeno en peróxido de hidrógeno (H 2 O 2 ). Usando experimentos en el laboratorio e in vivo, el equipo mostró el potencial de eliminación de ROS de las nanozimas en cascada integradas. Como prueba de concepto, aliviaron dos formas de trastorno inflamatorio intestinal (EII):la colitis ulcerosa y la enfermedad de Crohn utilizando nanozimas en cascada como tratamientos eficaces. El estudio proporcionó un nuevo método para construir sistemas en cascada similares a enzimas e ilustra la promesa de su terapia eficaz para tratar la EII in vivo. El trabajo ahora está publicado en Avances de la ciencia .
Durante las reacciones catalíticas en cascada que ocurren en organismos vivos, Se combinan múltiples enzimas dentro de los compartimentos subcelulares para una transducción de señales precisa y un metabolismo eficaz. Tales reacciones en cascada confinadas son ventajosas en comparación con las reacciones de múltiples etapas convencionales debido a las barreras de difusión reducidas y las concentraciones locales mejoradas de intermedios para mejorar la economía del átomo y las reacciones en total. Los científicos han hecho esfuerzos sustanciales para imitar tales sistemas en cascada en andamios, pero su alto costo y baja estabilidad tienen amplias aplicaciones prácticas limitadas. Como resultado, Los investigadores han explorado los imitadores de enzimas para comprender y construir reacciones en cascada en el laboratorio. En este trabajo, Liu e al. detallaron un sistema de reacción en cascada basado en nanozimas de un solo componente con alta actividad y demostraron su papel durante la terapia in vivo de la enfermedad inflamatoria intestinal (EII) asociada a especies reactivas de oxígeno (ROS).
Diseño, síntesis y caracterización del andamio enzimático
El equipo diseñó y sintetizó una nanozima en cascada mimética de superóxido dismutasa (SOD) y catalasa (CAT) integrada y la designó como Pt @ PCN222-Mn. Para construir el andamio, introdujeron una fracción similar a SOD de porfirina de manganeso (Mn) (III) y una nanopartícula de platino similar a CAT dentro de un marco de metal orgánico (MOF) a base de circonio (Zr) a nanoescala llamado PCN222. La construcción integrada (Pt @ PCN222-Mn) mostró una actividad de eliminación de ROS mejorada para proteger a los ratones de la EII relacionada con ROS, una enfermedad crónica incurable hasta ahora, y de ese modo ampliar el potencial de las nanozimas en cascada para aplicaciones biomédicas in vivo.
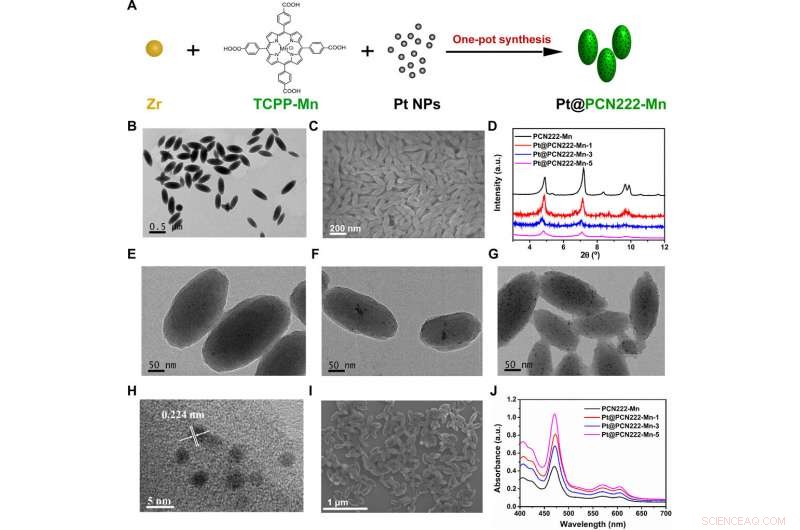
Síntesis y caracterización estructural de Pt @ PCN222-Mn y materiales relacionados. (A) Procedimiento de síntesis de Pt @ PCN222-Mn. (B) Imágenes de microscopía electrónica de transmisión (TEM) y (C) Imágenes de microscopía electrónica de barrido (SEM) de PCN222-Mn. (D) Patrones de difracción de rayos X en polvo (PXRD) de PCN222-Mn, Pt @ PCN222-Mn-1, Pt @ PCN222-Mn-3, y Pt @ PCN222-Mn-5. Imágenes TEM de (E) Pt @ PCN222-Mn-1, (F) Pt @ PCN222-Mn-3, y (G) Pt @ PCN222-Mn-5. (H) Imágenes TEM de alta resolución y (I) SEM de Pt @ PCN222-Mn-5. (J) Espectros de absorción de PCN222-Mn, Pt @ PCN222-Mn-1, Pt @ PCN222-Mn-3, y Pt @ PCN222-Mn-5. a.u., unidades arbitrarias. Crédito:Science Advances, doi:10.1126 / sciadv.abb2695
Durante los experimentos, Liu y col. confirmó la síntesis exitosa de las construcciones preliminares basadas en manganeso usando resonancia magnética nuclear, Espectroscopía infrarroja por transformada de Fourier y mediciones espectroscópicas ultravioleta visible. El equipo sintetizó el componente que contiene un MOF a nanoescala y confirmó su formación con microscopía electrónica de transmisión (TEM) y microscopía electrónica de barrido (SEM). Luego, los científicos desarrollaron tres nanozimas en cascada y las denominaron Pt @ PCN222-Mn-1, Pt @ PCN222-Mn-3 y Pt @ PCN222-Mn-5, respectivamente. De estos, Pt @ PCN222-Mn-5 tenía un área de superficie más alta en comparación con otras nanozimas anti-ROS investigadas hasta ahora.
Investigando la actividad catalítica de las nanozimas en cascada
Eliminación de radicales de oxígeno ( • O 2 - ) es el paso inicial de la reacción en cascada anti-ROS, por lo tanto, el equipo investigó la actividad catalítica de las construcciones sintéticas para monitorear su capacidad para eliminar de manera similar los radicales de oxígeno. El trabajo destacó el papel clave del manganeso en la porfirina para imitar las actividades similares a la superóxido dismutasa (SOD) de las diferentes construcciones enzimáticas, donde las construcciones de Pt @ PCN222-Mn-5 mostraron la actividad similar a SOD más alta entre los imitadores de enzimas. El equipo confirmó los resultados mediante espectroscopia de resonancia paramagnética electrónica (EPR).
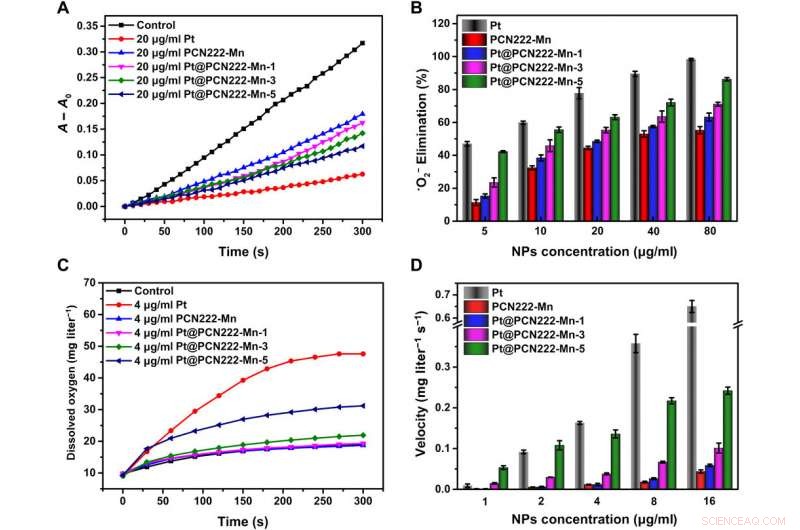
Actividades de captación de ROS de Pt @ PCN222-Mn y materiales relacionados. (A) Curvas cinéticas típicas de A - A0 (550 nm) para monitorear la reducción de NBT con X y XO en ausencia y presencia de Pt, PCN222-Mn, Pt @ PCN222-Mn-1, Pt @ PCN222-Mn-3, y Pt @ PCN222-Mn-5. (B) Dependencia entre la eficiencia de eliminación de • O2− y las concentraciones de nanozimas. (C) Curvas cinéticas típicas de la generación de oxígeno a partir de la descomposición de H2O2 (50 mM) en presencia de Pt, PCN222-Mn, Pt @ PCN222-Mn-1, Pt @ PCN222-Mn-3, y Pt @ PCN222-Mn-5. (D) Dependencia entre las velocidades de producción de oxígeno en los primeros 60 sy las concentraciones de nanozimas. Los datos se muestran como medias ± DE (n =3). Crédito:Science Advances, doi:10.1126 / sciadv.abb2695
Como segundo paso crucial en la cascada de eliminación de ROS en entornos biológicos, la enzima CAT (catalasa) catalizó la descomposición del peróxido de hidrógeno (H 2 O 2 ) en agua y oxígeno. Liu y col. por lo tanto, monitoreó las actividades de tipo CAT de las nanozimas monitoreando el oxígeno generado a partir de la descomposición del peróxido de hidrógeno. Como antes, Pt @ PCN222-Mn-5 mostró la mayor actividad similar a CAT entre los imitadores de enzimas basados en MOF. Según los resultados, Liu y col. confirmó que la actividad similar a la SOD resulta de la fracción de la construcción enzimática unida al manganeso, mientras que las nanopartículas integrales de platino fueron las principales responsables de la actividad de tipo CAT.
Enfoque de la enzima Pt @ PCN222-Mn-5 y terapia antiinflamatoria in vivo
Para comprender completamente la actividad de la nanozima en cascada Pt @ PCN222-Mn-5, El equipo investigó su actividad enzimática sinérgica similar a SOD y CAT y observó efectos sinérgicos pronunciados para este último. El equipo eligió la nanozima para realizar más investigaciones y probó su funcionalidad con una línea celular durante los estudios de citotoxicidad. A una concentración por debajo de 80 µg / mL, la nanozima no mostró ninguna citotoxicidad y demostró un excelente potencial de exploración de especies reactivas de oxígeno.
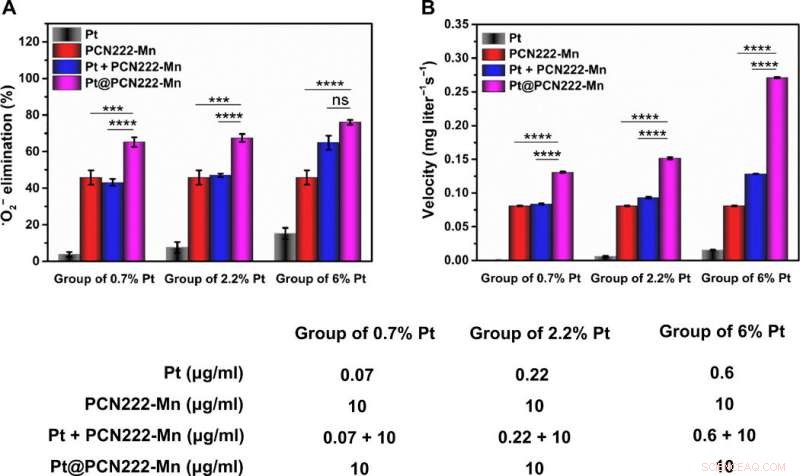
Actividad sinérgica de captación de ROS de Pt @ PCN222-Mn-5. (A) Eficiencia de eliminación de • O2− con diferentes concentraciones de Pt, PCN222-Mn, Pt + PCN222-Mn, y Pt @ PCN222-Mn. (B) Velocidades de producción de oxígeno en los primeros 60 s, con diferentes concentraciones de Pt, PCN222-Mn, Pt + PCN222-Mn, y Pt @ PCN222-Mn. Los datos se muestran como medias ± DE (n =3). *** P <0,005 y **** P <0,001; ns, insignificante; prueba t. Crédito:Science Advances, doi:10.1126 / sciadv.abb2695
Según los resultados experimentales, Liu y col. realizaron terapias in vivo para tratar la colitis ulcerosa (CU) y la enfermedad de Crohn (EC) en modelos de ratón de la enfermedad. Dado que la CU es una forma de trastorno inflamatorio intestinal que suele ir acompañada de especies reactivas de oxígeno sobreproducidas, los científicos probaron los efectos terapéuticos de Pt @ PCN222-Mn-5 junto con los medicamentos existentes para el tratamiento de la EII. El equipo administró el tratamiento mediante inyección intraperitoneal a cada ratón y observó efectos terapéuticos exitosos de Pt @ PCN222-Mn-5 para aliviar el estado de la enfermedad de UC en ratones. El equipo optimizó las dosis de la nanozima en cascada utilizando varios grupos de tratamiento y encontró que la enzima de interés de interés era la más favorable. Cuando exploraron el CD de manera similar, otro tipo de EII usando un modelo de ratón inducido por enfermedad, la estrategia de tratamiento indicó una mayor eficacia para las nanozimas en cascada en comparación con los medicamentos tradicionales de molécula pequeña utilizados en el tratamiento de la EII.
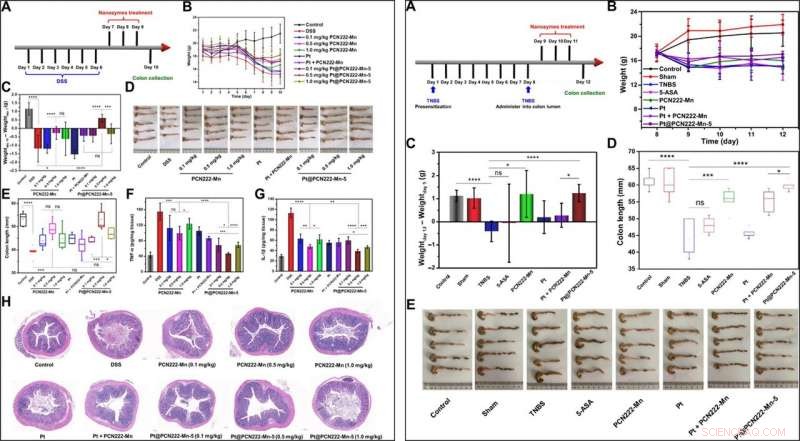
IZQUIERDA:Terapia de CU con Pt @ PCN222-Mn-5. (A) Procedimiento general del experimento con animales (colitis inducida por DSS). (B) Desarrollo diario del peso corporal durante 10 días. (C) Cambios en el peso corporal de los ratones antes (día 7) y después de los tratamientos indicados (día 10). (D) Imágenes de los dos puntos y (E) las longitudes de los dos puntos correspondientes en los grupos indicados. (F) Niveles de IL-1β y (G) TNF-α en homogeneizados de colon de los grupos indicados. (H) Secciones de colon teñidas con H &E de ratones de los grupos indicados el día 10. Los datos se muestran como medias ± DE (n =5). * P <0,05, ** P <0,01, *** P <0,005, y **** P <0,001; ns, insignificante; prueba t. Crédito de la foto (D):Yufeng Liu, Facultad de Ingeniería y Ciencias Aplicadas, Universidad de Nanjing. DERECHA:Terapia de CD con Pt @ PCN222-Mn-5. (A) Procedimiento general del experimento con animales [2, 4, Colitis inducida por ácido 6-trinitrobencenosulfónico (TNBS)]. (B) Desarrollo diario del peso corporal después de administrar la solución de TNBS en la luz del colon. (C) Cambios en el peso corporal de los ratones antes (día 9) y después de los tratamientos indicados (día 12). (D) Longitudes de los dos puntos y (E) las imágenes correspondientes de los dos puntos de los grupos indicados. Los datos se muestran como medias ± DE (n =5). * P <0,05, *** P <0,005, y **** P <0,001; ns, insignificante; prueba t. Crédito de la foto (E):Yuan Cheng, Facultad de Ingeniería y Ciencias Aplicadas, Universidad de Nanjing. Crédito:Science Advances, doi:10.1126 / sciadv.abb2695
De este modo, Yufeng Liu y sus colegas desarrollaron una nanozima integrada para catalizar reacciones en cascada y eliminar las especies reactivas de oxígeno (ROS). La nanozima integrada tenía dos sitios activos separados espacialmente para imitar la superóxido dismutasa (SOD) y la catalasa (CAT). Usando experimentos en el laboratorio, mostraron la destacada actividad de eliminación de ROS de la nanozima en cascada, su excelente biocompatibilidad y buena dispersabilidad acuosa. El equipo estableció un modelo animal inflamatorio para probar la capacidad anti-ROS de la nanozima en cascada en un organismo biológico y determinó su potencial terapéutico superior hacia los modelos de colitis ulcerosa (CU) y enfermedad de Crohn (EC) de trastorno inflamatorio intestinal (EII). El equipo optimizó la concentración de la nanozima para lograr un alivio efectivo de la EII en modelos animales. El trabajo mostró excelentes actividades de eliminación de ROS para el tratamiento inflamatorio y proporciona un método prometedor para construir nanozimas con múltiples sitios activos para aplicaciones adicionales en biomedicina.
© 2020 Science X Network