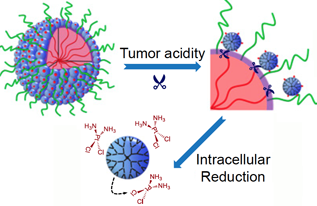
Las partículas comienzan siendo grandes (100 nm) para permitir un transporte suave al tumor a través de vasos sanguíneos con fugas. Luego, en condiciones ácidas que se encuentran cerca de los tumores, las partículas descargan bombitas de 5 nm de tamaño. Dentro de las células tumorales, un segundo paso químico activa el cisplatino. Crédito:Jinzhi Du / Wallace H. Coulter Departamento de Ingeniería Biomédica de Georgia Tech y Emory
Los científicos han ideado un sistema de "bomba de racimo" de tres etapas para administrar el fármaco de quimioterapia cisplatino, a través de diminutas nanopartículas diseñadas para romperse cuando llegan a un tumor.
Los detalles del diseño de las partículas y su potencia contra el cáncer en ratones se publicaron el 28 de marzo en PNAS . No se han probado en humanos, aunque se han realizado ensayos clínicos con formas similares de empaquetar cisplatino.
Lo que hace que estas partículas sean distintivas es que comienzan siendo relativamente grandes (100 nanómetros de ancho) para permitir un transporte suave al tumor a través de los vasos sanguíneos con fugas. Luego, en condiciones ácidas que se encuentran cerca de los tumores, las partículas descargan "minibombitas" de tan solo 5 nanómetros de tamaño.
Dentro de las células tumorales, un segundo paso químico activa el cisplatino a base de platino, que mata entrecruzando y dañando el ADN. Los médicos han usado cisplatino para combatir varios tipos de cáncer durante décadas, pero efectos secundarios tóxicos - para los riñones, nervios y oído interno:puede limitar su eficacia.
los PNAS El artículo es el resultado de una colaboración entre un equipo dirigido por el profesor Jun Wang, Doctorado en la Universidad de Ciencia y Tecnología de China, e investigadores dirigidos por el profesor Shuming Nie, Doctorado en el Departamento de Ingeniería Biomédica Wallace H. Coulter en Georgia Tech y Emory. Nie es miembro del programa de investigación Discovery and Developmental Therapeutics en Winship Cancer Institute of Emory University. Los autores principales son el estudiante de posgrado Hong-Jun Li y los becarios postdoctorales Jinzhi Du, PhD y Xiao-Jiao Du, Doctor.
"Los efectos secundarios negativos del cisplatino son una limitación de larga data para la quimioterapia convencional, ", dice Jinzhi Du". En nuestro estudio, el sistema de administración pudo mejorar la penetración del tumor para llegar a más células cancerosas, así como liberar los medicamentos específicamente dentro de las células cancerosas a través de su propiedad de transición de tamaño ".
Los investigadores demostraron que sus nanopartículas podrían mejorar la acumulación del fármaco cisplatino en los tejidos tumorales. Cuando a los ratones con tumores pancreáticos humanos se les administraron las mismas dosis de cisplatino libre o cisplatino revestido con nanopartículas sensibles al pH, el nivel de platino en los tejidos tumorales fue siete veces mayor con las nanopartículas. Esto sugiere la posibilidad de que la administración de nanopartículas de una dosis limitada de cisplatino pueda contener los efectos secundarios tóxicos durante el tratamiento del cáncer.
Los investigadores también demostraron que las nanopartículas eran eficaces contra un modelo de cáncer de pulmón resistente al cisplatino y un modelo de cáncer de mama metastásico invasivo en ratones. En el modelo de cáncer de pulmón, una dosis de cisplatino libre produjo solo un 10 por ciento de inhibición del crecimiento, mientras que la misma dosis revestida de nanopartículas produjo una inhibición del crecimiento del 95 por ciento, los investigadores informan.
En el modelo de cáncer de mama metastásico, el tratamiento de ratones con cisplatino revestido con nanopartículas prolongó la supervivencia del animal en semanas; El 50 por ciento de los ratones sobrevivieron a los 54 días con nanopartículas en comparación con los 37 días con la misma dosis de cisplatino libre. La eficacia mejorada en tres modelos de tumores diferentes demuestra que esta estrategia puede ser aplicable a varios tipos de cáncer, Dice Jinzhi Du.