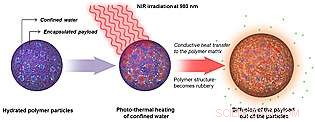
En esta representación esquemática, una nanopartícula polimérica hidratada se expone a la luz del infrarrojo cercano. El NIR calienta bolsas de agua dentro de la nanopartícula, haciendo que el polímero se ablande y permitiendo que las moléculas encapsuladas se difundan en el entorno circundante. Crédito:Facultad de Medicina de UC San Diego
Investigadores de la Universidad de California, Facultad de Farmacia y Ciencias Farmacéuticas San Diego Skaggs, en colaboración con científicos de materiales, ingenieros y neurobiólogos, han descubierto un nuevo mecanismo para usar la luz para activar nanopartículas que liberan fármacos y otras sustancias terapéuticas específicas dentro del cuerpo.
Este descubrimiento representa una gran innovación, dijo Adah Almutairi, Doctor, profesor asociado y director del Centro de Excelencia en Nanomedicina conjunto UC San Diego-KACST. Hasta ahora, ella dijo, sólo se ha informado de un puñado de estrategias que utilizan la liberación de nanopartículas activada por la luz.
El mecanismo, descrito en el 1 de abril, 2014 edición en línea de ACS Nano , emplea luz de infrarrojo cercano (NIR) de un láser de baja potencia para calentar bolsas de agua atrapadas dentro de nanopartículas poliméricas no fotosensibles infundidas con fármacos. Las bolsas de agua absorben la energía luminosa en forma de calor, que ablanda el polímero encapsulante y permite que el fármaco se libere en el tejido circundante. El proceso se puede repetir varias veces, con control preciso de la cantidad y dispersión del fármaco.
"Una ventaja clave de este mecanismo es que debería ser compatible con casi cualquier polímero, incluso aquellos que están disponibles comercialmente, "dijo Mathieu Viger, becario postdoctoral en el laboratorio de Almutairi y coautor principal del estudio. "Hemos observado atrapamiento de agua dentro de partículas compuestas por todos los polímeros biodegradables que hemos probado hasta ahora".
El método, señaló Viger, por tanto, muchos laboratorios biológicos podrían adoptarla fácilmente.
El uso combinado de polímeros hidratados y luz del infrarrojo cercano parece resolver una serie de barreras tecnológicas y de salud que han obstaculizado a anteriores, enfoques similares. Los esfuerzos anteriores para utilizar la liberación activada por NIR no han sido ampliamente explotados porque requerían polímeros de diseño especiales, costosos láseres de alta potencia y / o la encapsulación conjunta de partículas inorgánicas cuya seguridad en el cuerpo sigue siendo cuestionable.
El nuevo método descrito por Almutairi y sus colegas en los departamentos de Ingeniería Mecánica y Aeroespacial, Neurociencia y Química y Bioquímica en UC San Diego usa NIR en una longitud de onda vibratoria indicada para excitar moléculas de agua, que absorben la energía óptica y la convierten en calor. NIR es capaz de penetrar tejidos biológicos a mayores profundidades que la luz visible o ultravioleta.
El coautor principal Wangzhong Sheng, un estudiante de posgrado en el Departamento de Ingeniería Mecánica y Aeroespacial, explicó la selectividad del calentamiento comparando el agua atrapada dentro de las partículas con un vaso de agua y el agua circundante dentro de la solución o tejido con una bañera. La menor cantidad de agua se calienta mucho más rápidamente debido a la enorme diferencia de volumen.
Un uso obvio del método, dijo Almutairi, es la administración de fármacos activada por la luz, pero con más investigación, Ella anticipa que el nuevo método podría proporcionar una variedad de aplicaciones médicas y científicas, incluyendo "cualquier aplicación tecnológica que requiera que la química se controle en el tiempo y en el espacio, como en catálisis o materiales autorreparables o protectores solares activados por la luz o dosificación de pesticidas ".