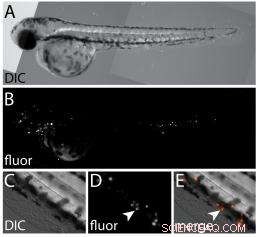
Un conjunto de imágenes muestra:A) una imagen de luz blanca de contraste de interferencia diferencial (DIC) de un embrión de pez cebra marcado con células fluorescentes de cáncer de próstata humano; B) una imagen fluorescente del embrión en A, revelando las células cancerosas xenoinjertadas; C) una imagen DIC de gran aumento de la aleta caudal ventral; D) una imagen fluorescente de la misma región en C que revela células xenoinjertadas (punta de flecha); y E) una imagen fusionada de C y D. (Crédito:Wagner Lab / Rice University)
(PhysOrg.com) - El físico de la Universidad de Rice, Dmitri Lapotko, ha demostrado que las nanoburbujas plasmónicas, generado alrededor de nanopartículas de oro con un pulso láser, puede detectar y destruir células cancerosas en vivo creando pequeños, Burbujas de vapor brillantes que revelan las células y las hacen explotar selectivamente.
Un artículo en la edición impresa de octubre de la revista. Biomateriales detalla el efecto de la teranóstica de nanoburbujas plasmónicas en el pez cebra implantado con células humanas vivas de cáncer de próstata, demostrando la ablación guiada de células cancerosas en un organismo vivo sin dañar al huésped.
Lapotko y sus colegas desarrollaron el concepto de teranóstica celular para unir tres etapas importantes del tratamiento:diagnóstico, terapia y confirmación de la acción terapéutica - en un procedimiento conectado. La capacidad de sintonización única de las nanoburbujas plasmónicas hace posible el procedimiento. Su modelo animal, el pez cebra, es casi transparente, lo que lo hace ideal para dicha investigación in vivo.
Los Institutos Nacionales de Salud han reconocido el potencial de la técnica inspirada de Lapotko al financiar más investigaciones que tienen un enorme potencial para la teranóstica del cáncer y otras enfermedades a nivel celular. Laboratorio de nanoburbujas plasmónicas de Lapotko, un laboratorio conjunto estadounidense-bielorruso de nanofotónica fundamental y biomédica, ha recibido una subvención por valor de más de $ 1 millón durante los próximos cuatro años para continuar desarrollando la técnica.
En una investigación anterior en el laboratorio doméstico de Lapotko en la Academia Nacional de Ciencias de Bielorrusia, nanoburbujas plasmónicas demostraron su potencial teranóstico. En otro estudio sobre aplicaciones cardiovasculares, Se filmaron nanoburbujas abriéndose paso a través de la placa arterial. Cuanto más fuerte sea el pulso del láser, cuanto más dañina es la explosión cuando las burbujas estallan, haciendo que la técnica sea altamente sintonizable. Las burbujas varían en tamaño desde 50 nanómetros hasta más de 10 micrómetros.
En el estudio del pez cebra, Lapotko y sus colaboradores en Rice dirigieron nanopartículas de oro marcadas con anticuerpos en las células cancerosas implantadas. Un pulso de láser corto sobrecalentó la superficie de las nanopartículas y evaporó un volumen muy delgado del medio circundante para crear pequeñas burbujas de vapor que se expandieron y colapsaron en nanosegundos; esto dejó las células intactas pero generó una fuerte señal de dispersión óptica que fue lo suficientemente brillante como para detectar una sola célula cancerosa.
Un segundo, pulso más fuerte generó nanoburbujas más grandes que explotaron (o, como lo llamaron los investigadores, "ablación mecánicamente") la célula diana sin dañar el tejido circundante en el pez cebra. La dispersión de la luz láser por la segunda burbuja "asesina" confirmó la destrucción celular.
Que el proceso sea de naturaleza mecánica es clave, Lapotko dijo. Las nanoburbujas evitan las trampas de la quimioterapia o la terapia de radiación que pueden dañar los tejidos sanos y los tumores.
"No es una partícula que mata la célula cancerosa, pero un evento pasajero y corto, ", dijo." Estamos convirtiendo la energía luminosa en energía mecánica ".
La nueva subvención permitirá a Lapotko y sus colaboradores estudiar los efectos biológicos de las nanoburbujas plasmónicas y luego combinar sus funciones en una sola secuencia que tardaría un mero microsegundo en detectar y destruir una célula cancerosa y confirmar los resultados. "Al ajustar su tamaño de forma dinámica, sintonizaremos su acción biológica desde la detección no invasiva hasta la administración intracelular localizada de fármacos y la eliminación selectiva de células específicas, " él dijo.
"Siendo un sigiloso, sonda bajo demanda con función sintonizable, la nanoburbuja plasmónica se puede aplicar a todas las áreas de la medicina, Dado que el mecanismo de nanoburbujas es universal y se puede emplear para detectar y manipular moléculas específicas, o para microcirugía precisa ".
Los coautores de Lapotko sobre el Biomateriales papel son Daniel Wagner, profesor asistente de bioquímica y biología celular; Mary "Cindy" Farach-Carson, vicerrector asociado de investigación y profesor de bioquímica y biología celular; Jason Hafner, profesor asociado de física y astronomía y de química; Nikki Delk, asociado de investigación postdoctoral; y Ekaterina Lukianova-Hleb, investigador en el Plasmonic Nanobubble Lab.