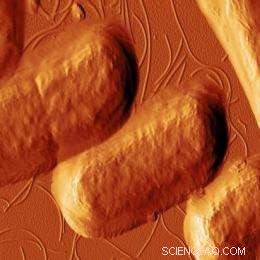
Esta imagen, tomada con microscopía de fuerza atómica, muestra bacterias E. coli después de haber sido expuestas al péptido antimicrobiano CM15. Los péptidos han comenzado a destruir las paredes celulares de las bacterias. Imagen:Georg Fantner
Durante dos décadas, Los científicos han estado buscando una nueva forma potencial de tratar las infecciones bacterianas, utilizando proteínas naturales conocidas como péptidos antimicrobianos (AMP). Ahora, Los científicos del MIT han registrado las primeras imágenes microscópicas que muestran los efectos mortales de los AMP, la mayoría de los cuales matan haciendo agujeros en las membranas de las células bacterianas.
Los investigadores dirigidos por la profesora del MIT Angela Belcher modificaron un técnica extremadamente sensible conocida como microscopía de fuerza atómica de alta velocidad (AFM) que les permite obtener imágenes de las bacterias en tiempo real. Su método, descrito en la edición en línea del 14 de marzo de Nanotecnología de la naturaleza , representa la primera forma de estudiar células vivas utilizando imágenes de alta resolución grabadas en rápida sucesión.
El uso de este tipo de AFM de alta velocidad podría permitir a los científicos estudiar cómo responden las células a otros medicamentos y a la infección viral. dice Belcher, el profesor Germeshausen de Ciencia e Ingeniería de Materiales e Ingeniería Biológica y miembro del Instituto Koch para la Investigación Integrativa del Cáncer en el MIT.
También podría ser útil para estudiar la muerte celular en células de mamíferos, como la muerte de las células nerviosas que ocurre en los pacientes de Alzheimer, dice Paul Hansma, profesor de física en la Universidad de California en Santa Bárbara que ha estado desarrollando tecnología AFM durante 20 años. “Este documento es un avance muy significativo en la obtención de imágenes de vanguardia de los procesos celulares, "Dice Hansma, que no participó en la investigación.
Alta velocidad
Fuerza atómica microscópica, inventado en 1986, se utiliza ampliamente para obtener imágenes de materiales a nanoescala. Su resolución (unos 5 nanómetros) es comparable a la de la microscopía electrónica, pero a diferencia de la microscopía electrónica, no requiere vacío y, por lo tanto, se puede utilizar con muestras vivas. Sin embargo, AFM tradicional requiere varios minutos para producir una imagen, por lo que no puede registrar una secuencia de eventos que ocurren rápidamente.
En años recientes, Los científicos han desarrollado técnicas AFM de alta velocidad, pero no los optimicé para las células vivas. Eso es lo que se propuso hacer el equipo del MIT, basándose en la experiencia del autor principal Georg Fantner, un asociado postdoctoral en el laboratorio de Belcher que había trabajado en AFM de alta velocidad en la Universidad de California en Santa Bárbara.
La microscopía de fuerza atómica utiliza un voladizo equipado con una punta de sonda que "siente" la superficie de una muestra. Las fuerzas entre la punta y la muestra se pueden medir a medida que la sonda se mueve a través de la muestra, revelando la forma de la superficie. El equipo del MIT utilizó un voladizo de aproximadamente 1, 000 veces más pequeñas que las que se utilizan normalmente para AFM, lo que les permitió aumentar la velocidad de la imagen sin dañar las bacterias.
Las mediciones se realizan en un ambiente líquido, otro factor crítico para mantener viva la bacteria.
Con la nueva configuración, el equipo pudo tomar imágenes cada 13 segundos durante un período de varios minutos después del tratamiento con un AMP conocido como CM15. Descubrieron que la muerte celular inducida por AMP parece ser un proceso de dos pasos:un breve período de incubación seguido de una rápida "ejecución". Se sorprendieron al ver que el inicio del período de incubación varió de 13 a 80 segundos.
"No todas las células comenzaron a morir al mismo tiempo, a pesar de que eran genéticamente idénticos y estaban expuestos al péptido al mismo tiempo, ”Dice Roberto Barbero, estudiante de posgrado en ingeniería biológica y autor del artículo.
La mayoría de los AMP actúan perforando las membranas celulares bacterianas, que destruye el delicado equilibrio entre la bacteria y su entorno. Otros parecen apuntar a la maquinaria dentro de la celda. Ha habido un gran interés en desarrollar AMP como medicamentos que podrían complementar o reemplazar a los antibióticos tradicionales, pero ninguno ha sido aprobado todavía.
Hasta hace unos años, se pensaba que las bacterias no podían volverse resistentes a AMPS, pero estudios recientes han demostrado que pueden. El nuevo trabajo del MIT podría ayudar a los investigadores a comprender cómo se desarrolla esa resistencia.