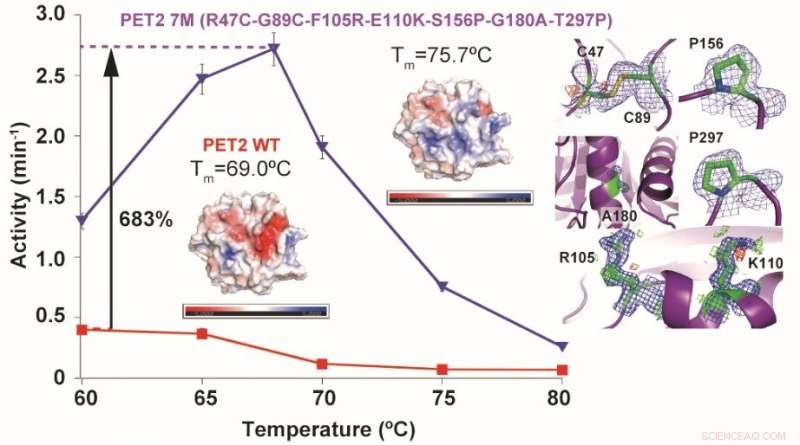
Las mutaciones de una enzima de hidrolización de PET PET2 dieron como resultado un aumento de 6,7 grados C en la estabilidad térmica y un aumento de 6,8 veces en la actividad hidrolítica de PET. T metro representa la temperatura de fusión (desnaturalización) y los colores de las estructuras enzimáticas muestran sus cargas superficiales (azul:positivo, rojo:negativo). Crédito:NINS / IMS
Barato de producir y anhelante de degradar, el plástico fue una vez un milagro de fabricación. Ahora, el plástico es una plaga medioambiental, obstruyendo los vertederos y asfixiando las vías fluviales. Un equipo de investigación con sede en Japón ha vuelto a la naturaleza para desarrollar un enfoque para degradar la obstinada sustancia. Similar a cómo una proteína se une a la celulosa en las plantas o a la quitina en los crustáceos para iniciar la descomposición, una proteína diseñada está en camino de unirse a las partículas de plástico en un esfuerzo por descomponerlas de manera más eficiente.
Publicaron sus resultados el 29 de junio en Catálisis ACS .
"El tereftalato de polietileno (PET) se produce y utiliza en grandes cantidades en la sociedad moderna debido a su bajo costo y facilidad de procesamiento, "dijo el autor del artículo Ryota Iino, profesor del Instituto de Ciencias Moleculares (IMS) de los Institutos Nacionales de Ciencias Naturales (NINS). "Sin embargo, en años recientes, desde la perspectiva de hacer realidad una sociedad sostenible, el reciclaje completo de PET en la industria y la eliminación del PET del entorno natural se han convertido en problemas mundiales. Para resolver estos problemas, es muy importante comprender cómo degradar el PET de manera eficiente ".
Los investigadores investigaron y diseñaron una enzima clonada de una biblioteca de materiales genéticos recolectados de la naturaleza. Se descubrió que esta enzima, llamada PET2, facilita la degradación del PET al acelerar la reacción entre los componentes químicos del PET y el agua.
Usando análisis de imágenes de una sola molécula, el equipo descubrió que la forma en que la enzima se une a la superficie del PET en realidad limitaba la tasa de degradación.
"También revelamos que al introducir cargas positivas en la superficie de la enzima que degrada el PET, se puede aumentar la tasa de unión a la superficie del PET, "Dijo Iino.
Las cargas positivas reaccionan favorablemente a la superficie del PET, por lo que una mayor cantidad de enzima puede unirse y degradar más eficazmente el PET. Los investigadores también encontraron que aunque el PET2 diseñado mostró una alta estabilidad térmica y una actividad más alta a 68 grados Celsius, un poco más baja de lo que pueden soportar la mayoría de los hornos de cocina residenciales, puede ser más efectivo a temperaturas más altas donde los enlaces moleculares del PET se vuelven más flexibles y rompibles.
"Nuestro objetivo final es crear una bacteria que pueda detectar el PET en el medio ambiente, muévete hacia él, y degradarlo, "Dijo Iino. Una bacteria así podría convertir el PET degradado en energía útil para otros organismos, actuando eficazmente como un centro de reciclaje automatizado de plástico. "En naturaleza, la quitina y la celulosa se reciclan de esta manera ".
Iino también está afiliado a la Facultad de Ciencias Físicas de la Universidad de Graduados de Estudios Avanzados (SOKENDAI). Otros contribuyentes incluyen Akihiko Nakamura, Departamento de Ciencias de la Vida Aplicadas, Facultad de Agricultura, Universidad de Shizuoka, y el Instituto de Shizuoka para el Estudio de Biología y Química Marinas; y Naoya Kobayashi y Nobuyasu Koga, Centro de Investigación Exploratoria sobre Vida y Sistemas Vivos (ExCELLS), NINS. Koga también está afiliado a IMS, NINS, y SOKENDAI.
La iniciativa líder para investigadores jóvenes excelentes, el Ministerio de Educación, Cultura, Deportes, Ciencias, y tecnología de Japón, la Fundación Sumitomo, y el Programa de Colaboración Especial ExCELLS apoyó esta investigación.