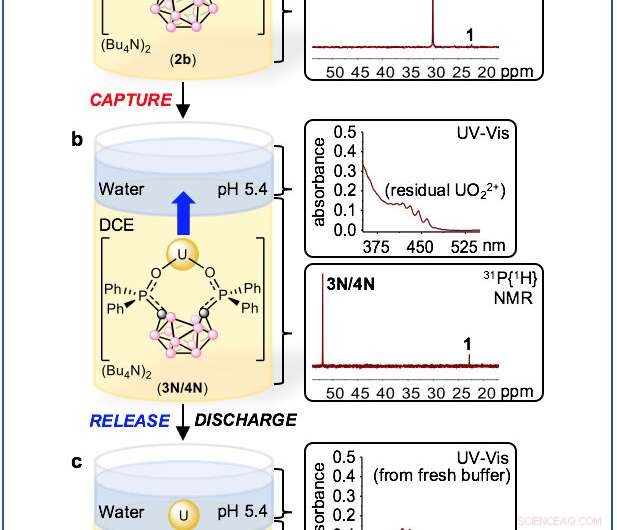
Una ilustración del método de conmutación electroquímica para capturar y liberar iones de uranio. Crédito:Universidad de California - Santa Bárbara
Hace cincuenta años, los científicos dieron con lo que pensaban que podría ser el próximo combustible para cohetes. Carboranos:moléculas compuestas de boro, Los átomos de carbono e hidrógeno agrupados en formas tridimensionales se vieron como la posible base para los propulsores de próxima generación debido a su capacidad para liberar cantidades masivas de energía cuando se queman.
Era una tecnología que en ese momento tenía el potencial de aumentar o incluso superar el combustible tradicional de hidrocarburos para cohetes. y fue objeto de fuertes inversiones en las décadas de 1950 y 1960.
Pero las cosas no salieron como se esperaba.
"Resulta que cuando quemas estas cosas, en realidad formas una gran cantidad de sedimentos, "dijo Gabriel Ménard, profesor asistente en el Departamento de Química y Bioquímica de la Universidad de California en Santa Bárbara. Además de otros problemas encontrados al quemar este llamado "combustible zip, "sus residuos también engomaron los trabajos de los motores de cohetes, y así el proyecto fue descartado.
"Así que hicieron estas enormes reservas de estos compuestos, pero en realidad nunca los usaron, "Dijo Ménard.
Avance rápido hasta hoy, y estos compuestos han vuelto a estar de moda con una amplia gama de aplicaciones, de la medicina a la ingeniería a nanoescala. Para Ménard y el profesor de química de UCSB Trevor Hayton, así como el profesor de química de la Universidad de Tel Aviv Roman Dobrovetsky, los carboranos podrían ser la clave para una extracción de uranio más eficiente. Y eso, Sucesivamente, podría permitir cosas como un mejor reprocesamiento de desechos nucleares y la recuperación de uranio (y otros metales) del agua de mar.
Su investigación, el primer ejemplo de aplicación de procesos electroquímicos de carborano a la extracción de uranio, se publica en un artículo (enlace) que aparece en la revista. Naturaleza .
La clave de esta tecnología es la versatilidad de la molécula de racimo. Dependiendo de su composición, estas estructuras pueden parecerse a jaulas cerradas, o nidos más abiertos, debido al control de la actividad redox del compuesto:su disposición a donar o ganar electrones. Esto permite la captura y liberación controladas de iones metálicos, que en este estudio se aplicó a los iones de uranio.
"El gran avance aquí es esta estrategia de 'captura y liberación' en la que puedes cambiar entre dos estados, donde un estado une el metal y otro estado libera el metal, "Dijo Hayton.
Procesos convencionales, como el popular proceso PUREX que extrae plutonio y uranio, dependen en gran medida de los disolventes, extractantes y procesamiento extensivo.
"Básicamente, se podría decir que es un desperdicio, "Dijo Ménard." En nuestro caso, podemos hacer esto electroquímicamente:podemos capturar y liberar el uranio con solo tocar un interruptor.
"¿Qué sucede realmente, "agregó Ménard, "es que la jaula se abre". Específicamente, el orto-carborano anteriormente cerrado se convierte en un nido- ("nido") carborano abierto capaz de capturar el ión uranio cargado positivamente.
Convencionalmente la liberación controlada de iones de uranio extraídos, sin embargo, no es tan sencillo y puede ser algo complicado. Según los investigadores, tales métodos están "menos establecidos y pueden ser difíciles, caro o destructivo para el material inicial ".
Pero aquí, Los investigadores han ideado una forma de alternar entre carboranos abiertos y cerrados de manera confiable y eficiente. usando electricidad. Aplicando un potencial eléctrico usando un electrodo sumergido en la porción orgánica de un sistema bifásico, los carboranos pueden recibir y donar los electrones necesarios para abrir y cerrar y capturar y liberar uranio, respectivamente.
"Básicamente, puedes abrirlo, capturar uranio, ciérrelo de nuevo y luego suelte uranio, "Dijo Ménard. Las moléculas se pueden usar varias veces, añadió.
Esta tecnología podría utilizarse para varias aplicaciones que requieran la extracción de uranio y, por extensión, otros iones metálicos. Un área es el reprocesamiento nuclear, en el que el uranio y otros elementos radiactivos "trans-uranio" se extraen del material nuclear gastado para su almacenamiento y reutilización (el proceso PUREX).
"El problema es que estos elementos trans-uranio son muy radiactivos y necesitamos poder almacenarlos durante mucho tiempo porque son básicamente muy peligrosos". "Dijo Ménard. Este método electroquímico podría permitir la separación del uranio del plutonio, similar al proceso PUREX, él explicó. A continuación, el uranio extraído podría enriquecerse y devolverse al reactor; los otros desechos de actividad alta se pueden transmutar para reducir su radiactividad.
Adicionalmente, el proceso electroquímico también podría aplicarse a la extracción de uranio del agua de mar, lo que aliviaría la presión sobre las minas terrestres de las que actualmente se obtiene todo el uranio.
"Hay unas mil veces más uranio disuelto en los océanos que en todas las minas terrestres, "Dijo Ménard. Del mismo modo, el litio, otro metal valioso que existe en grandes reservas en el agua de mar, podría extraerse de esta manera, y los investigadores planean tomar esta dirección de investigación en un futuro próximo.
"Esto nos da otra herramienta en la caja de herramientas para manipular iones metálicos y procesar desechos nucleares o capturar metales de los océanos". ", Dijo Hayton." Es una nueva estrategia y un nuevo método para lograr este tipo de transformaciones ".
La investigación en este estudio también fue realizada por Megan Keener (autora principal), Camden Hunt y Timothy G. Carroll en UCSB; y Vladimir Kampel en la Universidad de Tel Aviv.